QCM
Chimie, biochimie, UE1 Paces, médecine, Paris 2020.
En
poursuivant votre navigation sur ce site, vous acceptez l’utilisation
de Cookies vous proposant des publicités adaptées à vos centres
d’intérêts.
..
..
|
.
.
|
..
..
......
...
|
1.
On fait réagir en phase gazeuse de l'éthylène et de la vapeur d'eau
pour produire de l'éthanol. Cette réaction conduit à l'équilibre :
C2H4 (g) + H2O(g) = C2H6O(g)
à 300 K sous P°.
DrH=-45
kJ mol-1 ; DrS=-100
J mol-1 K-1.
DrG = DrH-TDrS = -45-300
x(-0,100) = -45+30 = -15 kJ / mol.
DrG = -RT ln K ; ln K = 15 103 /(8,31
x300) = 6. K ~400.
K est grand, la réaction est totale dans le sens direct (1).
A. La réaction a
lieu majoritairement dans le sens 1. Vrai.
B. La
réaction a lieu majoritairement dans le sens 1. Faux.
C. On ne peut pas
savoir le sens de la réaction car il manque DrU. Faux.
D. On ne peut pas savoir le sens de
la réaction car il manque l'entropie du solvant. Faux.
E. Aucune des
propositions précédentes n'est exacte. Faux.
2.
On considère un système thermodynamique. Lors d'une réaction chimique à
300 K, on mesure Q la quantité de chaleur liée à la réaction et on
trouve -600 J / mol. On désire étudier la variation d'entropie molaire
liée à cette transformation.
A. La
variation de l'entropie molaire est positive car l'entropie augmente
toujoure. Faux.
B. La
variation d'entropie molaire vaut -2 J / mol. Vrai.
Q / T =-600 / 300 = -2 J / mol.
C. La variation d'entropie molaire est supérieure à
-2 J / mol. Faux.
D. La variation
d'entropie molaire est inférieure à -2 J / mol. Faux.
E. Aucune des propositions
précédentes n'est exacte. Faux.
3. On considère la réaction chimique
4Fe3O4 +O2 = 6Fe2O3.
Parmi les valeurs suivantes, laquelle correspond à DrG en kJ / mol ?
On donne 3Fe +2O2 = Fe3O4 DG1 = -1000 kJ /
mol.
4Fe +3O2 =2 Fe2O3
DG2
= -900 kJ / mol.
4 fois {
Fe3O4 = 3Fe +2O2 } 4000 kJ / mol
3 fois {4Fe +3O2 =2 Fe2O3
}. -2700 kJ / mol.
-2700+4000 = 1300 kJ /mol. Réponse D.
4. A propos du
modèle de l'atome.
A. Deux électrons ne peuvent pas
avoir les quatre nombres quantiques identiques. Vrai.
B. Trois
électrons dans la même case quantique ont de spin opposé. Faux ( maxi 2 électrons par case quantique)
C. Le chlore 3717Cl a 17
protons et 20 neutrons.Vrai.
D. Le
recouvrement entre une orbitale 2py et 2px est un recouvrement latéral. Faux.
E. Aucune des propositions précédentes n'est exacte. Faux.
5. On considère les éléments
Ni (Z=28), Cu ( Z=29) et Zn ( Z=30).
A. Ces trois éléments ont le même
nombre d'électrons sur leur couche d à l'état fondamental. Faux
Ni : [Ar] 3d8 4s2 ou [Ar] 3d9
4s1.
Cu : [Ar] 3d10
4s1.
Zn : [Ar] 3d10
4s2.
Ar : [Ne] 3s2 3s6.
B. Ces trois élément possèdent
chacun deux électrons avec les nombres quantiques n=3, l=0 et m=0 à
l'état fondamental. Vrai.
C. L'énergie de première ionisation (EI1) évolue
selon EI1(Ni) > EI1(Cu) > EI1(Zn) . Faux.
L'énergie d'ionisation
augmente dans une période car la charge du noyau croît.
D. Cu+
et Zn2+ présentent la même configuration électronique. Vrai.
( [Ar] 3d10
).
E. Aucune des propositions précédentes n'est exacte. Faux.
6. A propos de la liaison chimique :
A. Lors de la formation d'une
liaison ionique, l'atome le plus électronégatif perd ses électrons.
Faux.
B. Dans
la molécule BF3, l'atome de bore comporte une case vide. Vrai.
C. Le recouvrement latéral d'une orbital s et d'une
orbitale p conduit à une orbitale moléculaire p. Faux.
D. Une triple
liaison implique la mise en commun de six électrons dans une orbitale
moléculaire. Faux.
( six électrons dans
trois orbitales moléculaires ).
E. Aucune des propositions
précédentes n'est exacte. Faux.
7.
Concernant le cobalt 2763Co :
A. Cet
atome est constitué de 27 neutrons, 36 protons, 36 électrons. Faux.
B. Cet atome est constitué de 63 nucléons, 27
protons, 27 électrons. Vrai.
C. Cet atome est constitué de 27 neutrons, 63
nucléons, 36 électrons. Faux.
D. Cet atome est constitué de 36 neutrons, 63
nucléons, 27 protons. Vrai.
E. Aucune des propositions
précédentes n'est exacte. Faux.
8. On donne Z(Fe) =
26. [Ar]4s23d6.
A. L'ion
Fe3+ a 6 électrons dans ces orbitales d. Faux. [Ar]4s03d5.
B. L'ion Fe2+ a 6 électrons dans ces
orbitales d. Vrai.
C. La configuration
de l'ion Fe2+ est [Ar]4s13d5. Faux.
D. La
configuration de l'ion Fe3+ est [Ar]4s03d6. Faux.
E. Aucune des propositions
précédentes n'est exacte. Faux.
9.Soit la molécule
d'oxychlorure de phosphore POCl3. p( Z=15) ; O(Z=8) ;
Cl(Z=17).
Indiquer la structure de Lewis la plus probable pour POCl3.
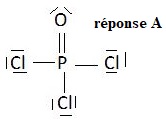
10. A l'aide de la
théorie VSEPR et en utilisant le modèle de Lewis pour POCl3 :
A. La structure est une bipyramide
trigonale. Faux.
B. La structure est tétraèdrique. Vrai.
C. Les angles ne
sont pas standards car la structure est déformée. Vrai.
D. Les angles sont standards car la structure
est déformée.. Faux.
E. Aucune des propositions
précédentes n'est exacte. Faux.
11.
Parmi les séries de composés suivants, indiquer laquelle ( lesquelles)
est ( sont) composéée(s) uniquement de réactifs électrophiles :
A. Mg2+,
BF3, H3CCOCH3. Faux.
B. Ca2+, AlCl3, (C2H5)4N+. Vrai.
C. H2S,
CH3-CH2-OH, C6H6. Faux.
D. CH3-O-CH2-CH3,
CH3-CHI-CH2-CH3, (CH3)2N-. Faux.
E. Li+, FeBr3,
CH3-S-CH3. Faux.
12. A propos de la réaction
endothermique suivante :
acide acétique + méthanol = acétate de méthyle + eau.
Indiquer quelle(s) condition(s) expérimentale(s) peut(peuvent) déplacer
l'équilibre vers la formation de l'ester.
A.
Présence d'un catalyseur. Faux ( l'équilibre
est atteint plus rapidement, sa composition reste inchangée).
B. Utiliser un excès de méthanol. Vrai.
C.Diluer le milieu
réactionnel avec de l'eau hautement purifiée. Faux.
D. Elever la température du milieu réactionnel. Faux.
E. Ajouter un peu d'ester pour
initier la réaction. Faux.
13.
Parmi les trois composés suivants :
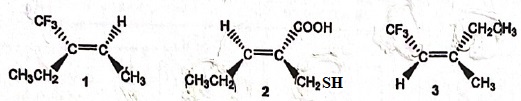
A. 1 est de configuration E. Vrai.
B. 1 est de configuration Z. Faux.
C. 2 est de configuration E. Vrai.
D. 3 est de
configuration Z. Vrai
E. Aucune des propositions
précédentes n'est exacte.
Un atome de numéro atomique plus élevé a priorité sur un atome de
numéro atomique plus faible.
Lorsque deux atomes de premier rang ont même priorité, on passe aux
atomes de second rang.
1 : CF3
> CH2-CH3 > CH3 > H, donc E.
2 : COOH
> CH2-SH. > CH2-CH3 > H, donc E.
3 : CF3
> CH2-CH3 > CH3 > H, donc Z.
14.
Parmi les 5 structures suivantes, laquelle (lesquelles) est ( sont)
chirale(s) ?
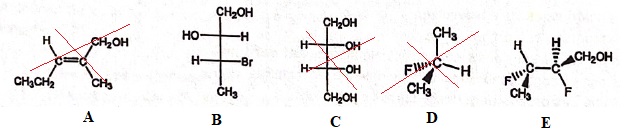
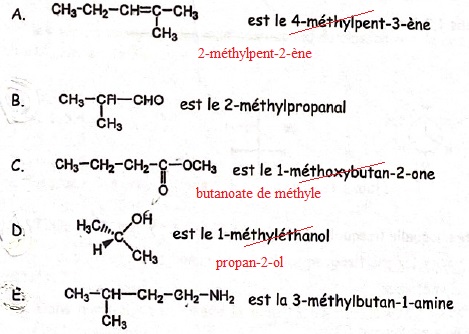
15. Parmi les structures A et E
suivantes, laquelle ( lesquelles) représente(nt) l'énantiomère du
composé 1 ?
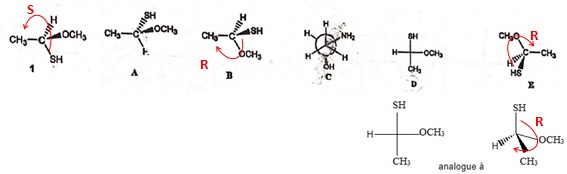
16. Quelles est
(sont ) la ( les) proposition(s) exacte(s) ?
17.
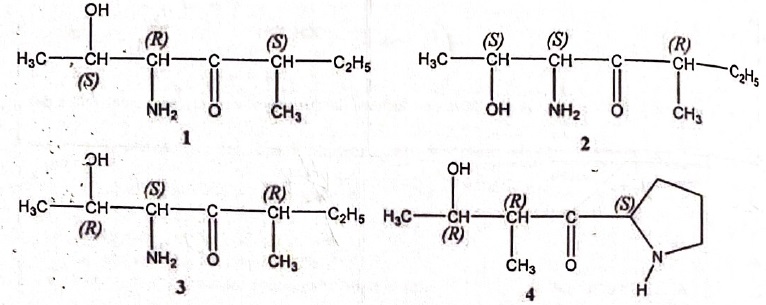
A. 1 et 2 sont
diastéréoisomères. Vrai.
B. 1 et 3 sont
énantiomères. Vrai.
C. 1 et 4 sont isomères de
constitution. Faux ( formules brutes
différentes).
D. 2 et 3 sont
isomères de constitution. Faux. ( même
structure carbonée, même formule brute )
E. Aucune
proposition exacte.
18.
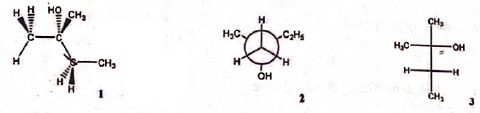
A.
1
contient un atome de carbone asymétrique. Faux.
B. 2
contient un atome de carbone asymétrique. Faux.
C. 2 est une représentation de
Cram. Faux ( Newman).
D. 2 et 3
représentent le même composé. Vrai.
E. Aucune
proposition exacte.
19.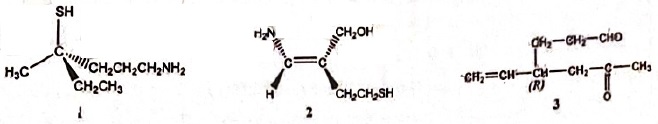
A. 1
est le (R)-6 amino-3-méthylhexane-3-thiol. Vrai.
B. 1 est le (R)-5
amino-2-éthylpentane-2-thiol. Faux.
C. 1 est de configuration S. Faux.
D. 2 est de configuration Z. Vrai.
E. 3 est la (R)
-4-(3-oxopropyl) hex-5-én-2-one. Faux. ( la plus longue chaine carbonée compte 7
atomes de carbone).
20. Soient les
conformères du 1,2-dibromo-1,2 dichlorométhane :
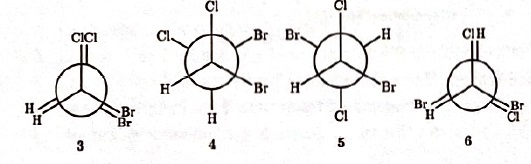
Parmi les séries suivantes, laquelle correspond au classement de ces
conformères dans l'ordre de stabilité croissante ?
A. 3 ; 4 ; 5 ; 6 ; B. 3 ; 5 ; 6 ; 4. C. 3 ; 6 ; 4 ; 5.Vrai.
D. 6 ; 3 ; 5 ; 4. E. Aucune propositions exactes.
5 est le plus stable ( Br et Cl décalés ) suivi de 4 ; suivi de 6 ;
suivi de 3.
|
...
|
....
|
21.
A propos des effets électroniques.
A. Dans une liaison polarisée la
densité électronique est plus forte du côté de l'atome le plus
électropositif. Faux.
B. Les atomes d'halogènes
n'ont pas d'effet inductif. Faux..
C. Les effets
inductifs et électrodonneurs stabilisent les carbocations. Vrai.
D. Le 6
-méthylhepta-2,4-diène ne présente pas d'effet mésomère. Faux ( 2 doubles liaisons conjuguées).
E. Aucune
propositions exactes.
22. 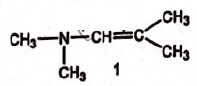
A. La structure
suivante est la forme mésomère de 1.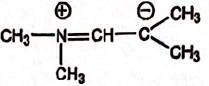 Vrai. Vrai.
B.
La structure suivante est la forme mésomère de 1.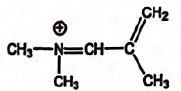 Faux. Faux.
C. 1 contient une double liaison
stéréogène. Faux. ( pas de centre
chiral )
D. La structure
suivante est la forme tautomère de 1.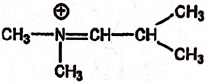 Faux ( pas
d'hydrogène sur N) Faux ( pas
d'hydrogène sur N)
E. Aucune propositions exactes.
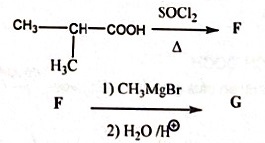
23. Soit le schéma de synthèse
suivant :
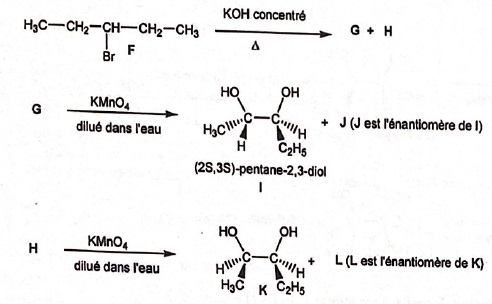
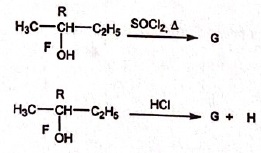
A. le composé F est
un dérivé halogéné tertiaire. Faux.( secondaire)
B. La réaction F
donne G+H est une élimination E2. Faux ( l'élimination E1 donne
deux isomères Z et E ; l'élimination E2 donne seul le
composé E)
C. Les composés G
et H sont isomères de configuration. Vrai.
D. Les composés L
et K sont diastéréoisomères. Faux ( L
et K sont énantiomères ).
E. Aucune des
propositions précédentes n'est exacte.
24. Soit le schéma
de synthèse suivant :
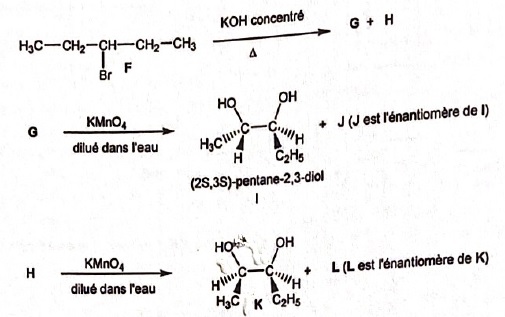
A.
Le composé G est un acide carboxylique.
B. Le composé G est un
aldehyde.
C. Le composé F posède la structure suivante :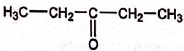
D. Le
composé H possède la structure suivante : H3C-CH2-COOH.
E. Aucune des
propositions précédentes n'est exacte.
25. Soit le schéma de
synthèse suivant :
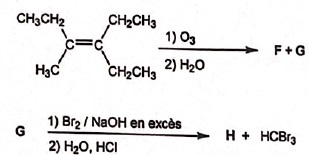
A. Le composé G est un acide carboxylique. Faux. ( G est une cétone CH3-CH2-CO-CH2-CH3 ou
bien CH3-CH2-CO-CH3).
B. Le composé G est un
aldehyde. Faux.
C. Le composé F à la structure suivante :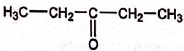
ou
bien CH3-CH2-CO-CH3
D. Le composé H à la
structure suivante : H3C-CH2-COOH
Réaction haloforme à
partir de CH3-CH2-CO-CH3.
E. Aucune des
propositions précédentes n'est exacte.
26. Soit la suite de
réaction suivante :
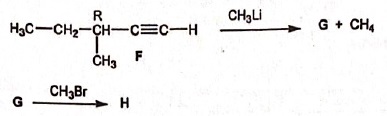
A. La réaction F donnant G est une substitution nucléophile.
CH3Li
est une base forte qui déprotone l'alcyne vrai.
B. L'hydrogène lié au carbone sp de F porte
une charge partielle -d.
Faux ( cet hydrogène est acide)
C. La réaction G donnant H est une réaction acide-base.
D. La structure de H est 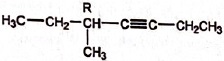 Faux, on obtient Faux, on obtient
E. Aucune des
propositions précédentes n'est exacte.
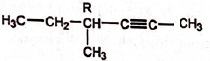
27.
Soit la réaction suivante :
A.
Le composé G est un alcène. Faux (G
est un chloroalcane)
B. La réaction F donne G+H est une addition
nucléophile. Faux. ( substitution
nucléophile).
C. G et H sont énantiomères. Vrai.
(l'intermédiaire est un carbocation
plan tertiaire, l'attaque
nucléophile de ce carbocation par Cl-
peut se faire d'un côté ou de l'autre du plan)
D. Le composé H possède un carbone
asymétrique de configuration S.Vrai.
E. Aucune des
propositions précédentes n'est exacte.
28. Soit la suite de
réactions suivantes :
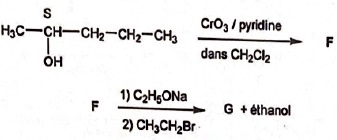
A. Le composé F est un aldehyde. Faux (F est une cétone)
B. La réaction F donne G est une réaction
d'alkylation. Vrai.
C. Le composé G possède deux carbones asymétriques. Faux.
D. Le composé G possède la structure
suivante 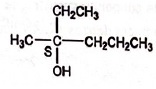 Faux. Faux.
L'intermédiaire est un
carbocation plan, attaque possible d'un côté ou de l'autre du plan.
E. Aucune des
propositions précédentes n'est exacte.
29.
Soit la suite de réactions suivante :
A. F est un alcool
primaire. Faux ( F est un
chlorure d'acyle)
B. G est une
cétone. Faux.
On obtient une cétone qui
réagit rapidement avec l'organomagnésien ; on obtient finalement un
alcool tertiaire.
C. Le carbone lié
au magnésium dans CH3MgBr est nucléophile. Vrai.
D. G possède la
structure suivante :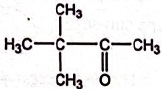 Faux. Faux.
Cette
cétone qui réagit rapidement avec l'organomagnésien ;on obtient finalement un alcool tertiaire.
E. Aucune des propositions
précédentes n'est exacte.
30.
Soit la suite de réactions suivantes :
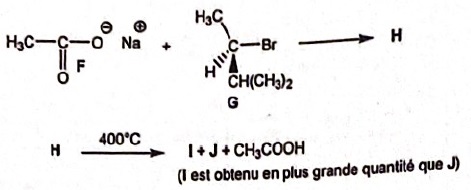
A. La réaction H
donne I+J +CH3COOH est une réaction d'ozonolyse. Faux.
H est un ester qui, par
chauffage ( pyrolyse) donne deux alcènes.
B. I et J sont
régioisomères. Faux.
C.
I et J sont isomères de configuration. Vrai.
D. I possède la structure suivante :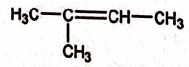 Vrai. Vrai.
L'alcène le plus
substitué est majoritaire.
E.
Aucune des propositions précédentes n'est exacte.
31.
Soit la suite de réactions suivantes :

A.
G est un dérivé halogéné secondaire. Vrai.
B. F est un acide carboxylique. Faux
( F est un carboxylate de sodium)
C.
La réaction F+G donne H est une SN1. Vrai.
La molécule de départ est
très encombrée.
D. H possède un carbone asymétrique de configuration R. Faux.
Le carbocation plan peut
être attaqué d'un côté ou de l'autre.
E.
Aucune des propositions précédentes n'est exacte.
32.
Soit la suite de réactions suivantes :
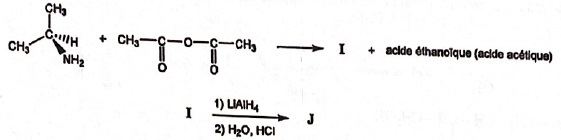
A.
I est un ester. Faux ( I est un amide).
B. I est un amide. Vrai.
C.
I possède la structure suivante :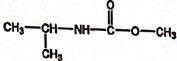 Faux. Faux.
(CH3)2CH-NH-CO-CH3.
D. J possède la structure suivante :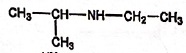 Vrai. Vrai.
E. Aucune des propositions
précédentes n'est exacte.
33.
Soit la suite de réactions suivantes :
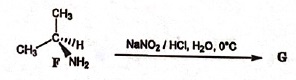
A.
F est une amine secondaire. Faux. (amine primaire)
B. G est un alcool secondaire. Vrai. (le carbocation (CH3)2CH+
peut conduire à un alcool secondaire).
C.
G est le propan-2-ol. Vrai.
D. G est une nitrosoamine. Faux.
E. Aucune des propositions
précédentes n'est exacte.
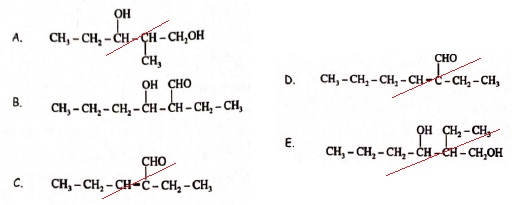
34. On considère
l'aldolisation du butanal. Parmi les composés suivants, lequel
(lesquels) peut ( peuvent ) être obtenu(s) ?
35. Concernant la
suite de réactions suivantes :
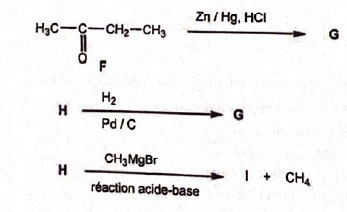
A. H est un alcyne.
Faux.
Un alcyne + catalyseur de
Lindlar donne un alcène.
B. H est un alcène.
Vrai.
C. G est un alcool
secondaire. Faux.
La réduction de
Clemmensen donne un alcane, le butane
D. H possède la
structure suivante H3C- C=C-CH3. Faux.
E.
Aucune des propositions précédentes n'est exacte.
36. Concernant la
réaction suivante :
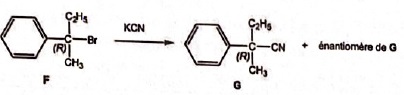
A. Une des étapes
de son mécanisme réactionnel est :
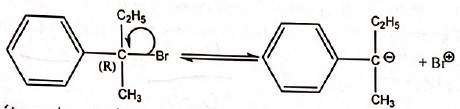 Faux. Faux.
B.
Une des étapes de son mécanisme réactionnel est :
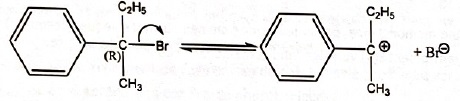 Vrai
( carbocation stabilisé par
résonnance) Vrai
( carbocation stabilisé par
résonnance)
C. C'est une
réaction de substitution nucléophile SN2. Faux.
D. C'est
une réaction de substitution nucléophile SN1. Vrai.
E.
Aucune des propositions précédentes n'est exacte.
|
|