Ondes
sonores, cellule photovoltaïque, pile saline, Bac Sti2d 2021.
En
poursuivant votre navigation sur ce site, vous acceptez l’utilisation
de Cookies vous proposant des publicités adaptées à vos centres
d’intérêts.
..
..
|
|
Exercice 1. Ondes sonores.
Partie A.
Une personne souhaite assister au décollage de la fusée Ariane sans
protection auditive.
L'intenité acoustique du bruit généré par le décollage vaut 100 W m-2
à 100 m de la rampe de lancement.
1. A
quelle distance minimale de la rampe de lancement, la personne
doit-elle se trouver pour que le bruit ne présente aucun risque pour
l'audition.
On considère que l'oreille ne subit pas de dommage pour
un son de niveau d'intensité sonore inférieur à 100 dB pendant une
durée d'exposition ne dépassant pas 4 minutes par jour.
Niveau sonore lié au décollage à 100 m de la rampe : L = 10 log(100 / 10-12)
= 10 log 1014 = 140 dB.
Le niveau d'intensité sonore diminue de 20 dB lorsque la distance par
rapport à la source est multipliée par 10.
Niveau sonore lié au décollage à 1000 m de la
rampe : 140-20=120 dB.
Niveau sonore lié au décollage à 10 000 m = 10 km de la rampe : 120 -20 =100 dB.
La personne doit se trouver à une distance minimale de 10 km.
Partie B.
1. On rappelle que L = 10 log (I / I0).
Montrer que I = I0 x10L /10.
log (I / I0) =L /10 ; I / I0 =10L /10.
I = I0 x10L /10.
2.
Calculer l'intensité sonore pour l = 50 dB.
I = 10-12 x105 =10-7
W m-2.
3.
L'intensité sonore doublet-elle lorsque l'on double le niveau
d'intensité sonore L ?
L = 10 log (I / I0) ; I = I0 x10L /10.
2L =L' = 20 log (I' / I0) ; I' = I0 x10L' /10
; I' = I0 x102L /10 = I0 x102L /10 =I0 x10L /10 x10L /10 .
I' = I x10L
/10 .
L'intensité sonore ne double pas si le niveau d'intensité sonore double.
4. Montrer que
l'intensité sonore est divisée par 100 lorsque la distance à la source
est multipliée par 10.
A la distance d1 de la source L1 = 10 log (I1
/ 10-12).
A la distance d2 =10 d1
de la source L2 =L1-20= 10 log (I2 / 10-12).
10 log (I1 / 10-12)-20 =
10 log (I2 / 10-12).
10[ log (I1 / 10-12)-log (I2
/ 10-12)] = 20 ;
log (I1 / I2 )= 20 /10 = 2 ; I1 / I2 = 100 ; I2
= I1 / 100.
Exercice 2. Voiture solaire miniature.
Etude expérimentale de la
cellule photovoltaïque.
On trace la caractéristique courant tension de la cellule.
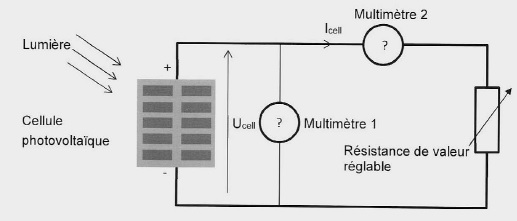
1.
Indiquer les fonctions des deux multimètres.
Multimètre 1 en dérivation : voltmètre.
Multimètre 2 en série : ampèremètre.
2. Indiquer le rôle de la résistance
de valeur réglable.
Cette résistance permet de faire varier l'intensité du courant.
3.
Compléter le diagramme énergétique.
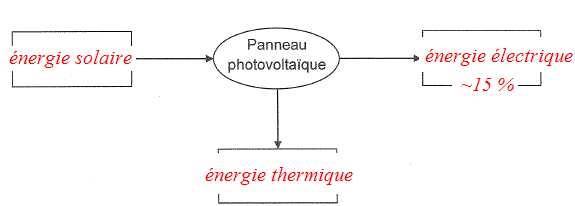
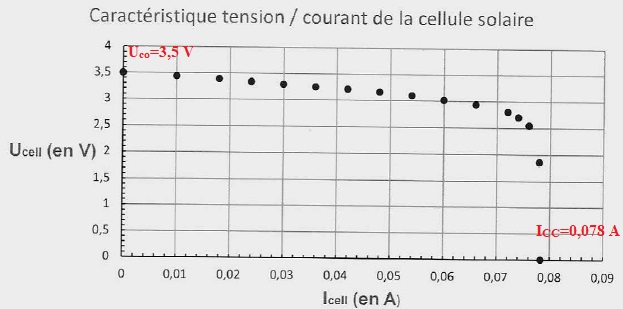
4. Indications du constructeur :
Intenité de court-circuit Icc = 70 mA ; tension à vide UCO
=3,0 V.
Indications relevées expérimentalement : Intenité
de court-circuit Icc = 78 mA ; tension à vide UCO
=3,5 V.
A 15 % près ces indications concordent.
5.
On s'intéresse à la puissance électrique Pélec délivrée par
la cellule. Donner la relation liant la puissance, l'intensité et la
tension.
P = U I ; P (watt) ; U(volt) et I(ampère).
6.
Déterminer la puissance crète et la tension correspondante.
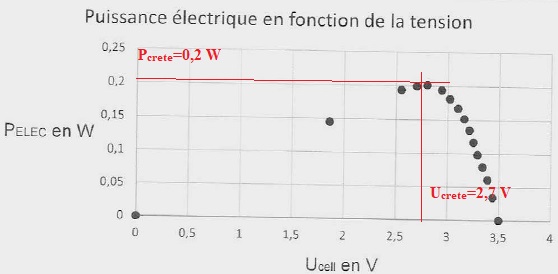
7. En déduire
l'intensité correspondante.
Icrete = Pcrete / Ucrete = 0,2 / 2,7
~0,074 A.
8. Montrer que le
rendement de la cellule est de l'ordre de 17 %.
Puissance solaire reçue par unité de surface : 800 W / m2.
Surface de la cellule : S =60 10-3 x25 10-3
=0,0015 m2.
Puissance solaire : 800 x 0,0015 =1,2 W.
Rendement = puissance électrique crète / puissance solaire = 0,2 / 1,2
~0,17 (17 %).
|
Pile saline.
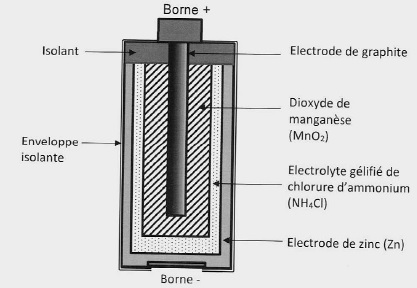
Quand la pile fonctionne, l'électroode de zinc est le siège de la transformation chimique : Zn(s) --> Zn2+aq +2e-.
L'électrode de graphite est le siège de la transformation chimique : MnO2(s) +H+aq +e- --> MnO(OH) (s).
La pile est reliée à un conducteur par des fils électriques.
10.
Quand la pile débite un courant électrique, préciser la nature des
porteurs de charge électrique dans le circuit extérieur.
Les électrons.
11. Indiquer si le zinc subit une oxydation ou une réduction. Justifier.
Le zinc, réducteur, libère des électrons ; c'est un réducteur qui s'oxyde.
12. Préciser si le zinc joue de rôle decathode ou d'anode.
Une oxydation a lieu à l'anode en zinc.
13. Ecrire le couple oxydant / réducteur auquel appartient le dioxyde de manganèse.
MnO2 (s) / MnO(OH) (s).
14. Ecrire l'équation de fonctionnement de la pile.
Zn(s) --> Zn2+aq +2e-.
2MnO2(s) +2H+aq +2e- --> 2MnO(OH) (s).
Ajouter : 2MnO2(s) +2H+aq +2e- +Zn(s) --> 2MnO(OH) (s) + Zn2+aq +2e-.
Simplifier : 2MnO2(s) +2H+aq +Zn(s) --> 2MnO(OH) (s) + Zn2+aq .
|
|




