Boissons
énergétiques ou énergisantes, bac S polynésie 2020.
En
poursuivant votre navigation sur ce site, vous acceptez l’utilisation
de Cookies vous proposant des publicités adaptées à vos centres
d’intérêts.
..
..
|
.
.
|
..
..
......
...
|
Les boissons énergétiques.
Leur analyse met en évidence trois constituants principaux : l'eau, des glucides ( sucres) et des sels minéraux.
1.1. Le glucose et le fructose.
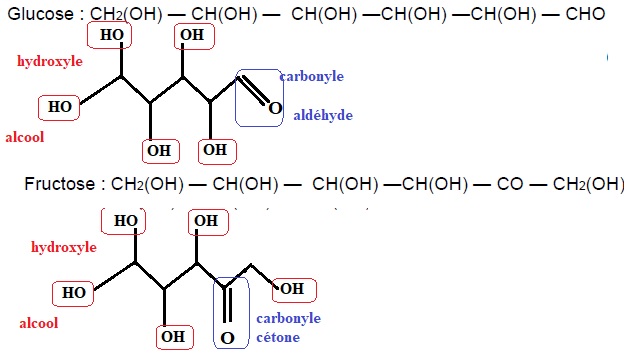
1.1.1. Donner la
représentation topologique des molécules de glucose et de fructose.
Entourer les groupes caractéristiques, nommer les familles des
fonctions associées.
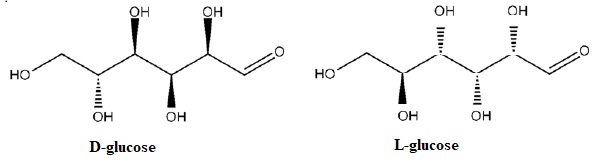
1.1.2. Dans la
nature, le glucose se présente sous forme de D-glucose, molécule
chirale. QSu'est ce que cela signifie ? représenter l'énantiomère du
D-glucose.
Une molécule chirale n'est pas superposable à son image dans un miroir plan.
1.1.3. Il est
possible de transformer du glucose en fructose. S'agit-il d'une
modification de chaîne ou d'une modification de groupe caractéristique
? Justifier.
La chaîne linéaire à 6 atomes de carbone n'est pas modifiée. La
fonction aldehyde du glucose se retrouve en fonction cétone dans le
fructose.
1.2 Etude cinétique de l'hydrolyse du saccharose.
L'hydrolyse du saccharose, en solution aqueuse acide, donne du glucose et du fructose.
Le saccharose présent dans les boissons énergétiques, subit une
hydrolyse dans le corps humain, à 37°C et à un pH de 7,4. Une enzyme,
l'hydrolase augmente la vitesse de la réaction.
1.2.1. Définir le terme catalyseur.
Un catalyseur est un facteur cinétique, il augmente la vitesse d'une
réaction chimique. Il est régénéré lors de la dernière étape du
mécanisme réactionnel et de ce fait, n'apparaît pas dans le bilan.
1.2.2. Lors de l'hydrolyse dans un tube à essais, de quelle catalyse s'agit-il ?.
Catalyse chimique, homogène, en solution aqueuse acide.
On prépare une solution aqueuse de saccharose de concentration c = 4,0 10-2 mol / L. L'évolution de la concentration du saccharose est suivie par dosage successifs.
1.2.3 Déterminer sur le graphe suivant, le temps de demi-réaction de cette hydrolyse.
1.2.4. Tracer sur ce graphe, l'allure d'une courbe correspondant à l'hydrolyse de la même solution en présence d'hydrolase.
L'hydrolyse enzymatique en présence d'hydrolase est beaucoup plus rapide que la catalyse chimique.
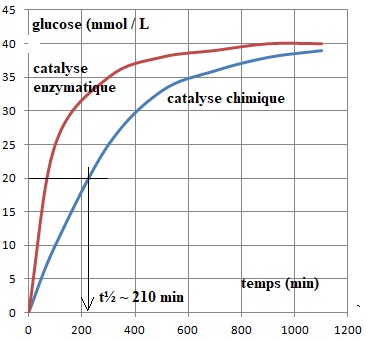
A t½, l'avancement est égal à la moitié de l'avancement final.
1.2.5 Ces résultat expérimentaux confirment-ils que la réaction d'hydrolyse du saccharose en milieu acide est totale.
La concentration finale du glucose étant égale à la concentration initiale du saccharose, l'hydrolyse est totale.
|
...
|
....
|
2. Les boissons énergisantes.
En plus des sucres cités ci-dessus, elles contiennent de la taurine, du
glucuronolactone et de la caféine ( 80 mg pour une canette de 250
mL).
2.1. Identification de la formule chimique de la caféine à partir de son spectre RMN.
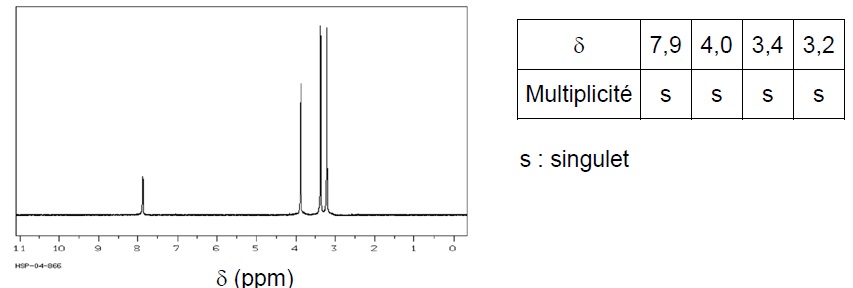
2.1.1 Identifier, parmi les molécules représentées ci-dessous, celle qui correspond à la caféine.
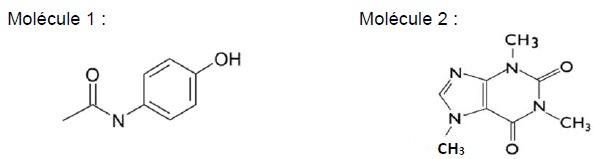
La molécule 2 convient. La présence de singulets signifie que les atomes de carbone voisins ne portent pas d'atome d'hydrogène.
Pour la molécule 1, on observerait un multiplet correspondant aux protons du cycle.
2.1.2. A l'issue
d'une exctraction de la caféine d'une boisson énergisante, comment
vérifier, en absence de spectromètre RMN, que la poudre obtenue est
bien de la caféine pure ? Quelle observation permettrait de conclure à
la présence de caféine ?
Chromatographie ( CCM), l'étalon étant de la caféine pure ; sur le
chromatogramme on observait, pour chaque espèce, une seule tache avec
le même rapport frontal.
2.2.Dosage par étalonnage de la caféine contenue dans une tasse de café.
On enregistre le spectre d'absorption de la caféine et on trace
une courbe d'étalonnage. On prépare une tasse de café contenant 75 mL
de boisson. On dilue 20 fois cette boisson et on mesure l'absorbance de
la solution obtenue. On trouve A = 0,68.
2.2.1. Donner les 4
étapes principales de la démarche expérimentale permettant d'obtenir la
courbe d'étalonnage à partir de la caféine commerciale en poudre.
Etape 1. Tracer le spectre d'absorption de la caféine en solution aqueuse.
Etape 2. Préparer une gamme de solutions étalons de différentes concentrations.
Etpae 3. Mesurer l'absorbance de chaque solution et tracer la coube A = f(c).
Etape 4. Mesurer l'absorbance de la boisson.
2.2.2. Le spectrophotomètre n'émet que des radiatons de longueur d'onde comprises entre 230 nm et 650 nm.
Déterminer une valeur possible de longueur d'onde utilisée lors du dosage. La couleur du café est-elle génante ?
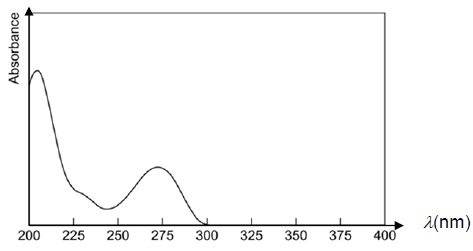
Pour un maximum de précision, on choisit une longueur d'onde correspondant à un maximum d'absorption ( 275 nm).
270 nm se situe dans l'U.V, la couleur du café n'est pas génante.
2.2.3 Evaluer le
nombre de tasse de café qui apporteraient la même quantité de caféine
que celle présente dans une canette de 250 mL de boisson énergisante.
Commenter.
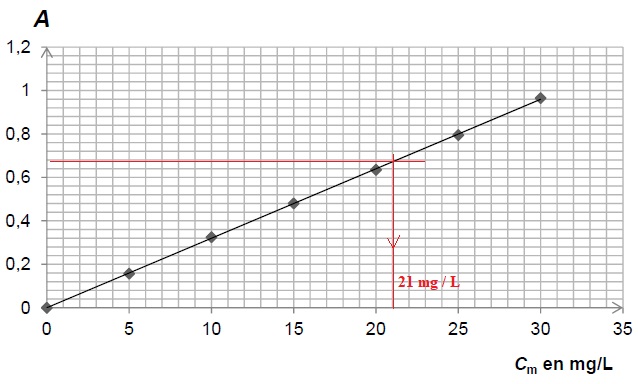
Tenir compte de la dilution.
21 x20 = 420 mg / L = 0,42 g/ L de caféine.
Soit 420 / 4 =105 mg de caféine dans la canette de 250 mL.
Une tasse de café de 50 mL contient environ 100 mg de caféine
Pour un adulte, la dose
maximale journalière varie de 200 à 400 mg par jour ( soit 2,5 à 5
canettes de cette boisson ou entre 2 et 4 tasses ).
|
|