Prťparation
d'une biŤre brune aromatisťe, bac Centres ťtrangers 2021.
En
poursuivant votre navigation sur ce site, vous acceptez l’utilisation
de Cookies vous proposant des publicitťs adaptťes ŗ vos centres
d’intťrÍts..
...
.
|
.
.
|
..
..
......
...
|
Exercice1 ( 10 points).
Partie 1. SynthŤse d'un ester au laboratoire.
L'ester est notť E. On donne sa formule semi-dťveloppťe.
1. Nommer E et reprťsenter sa formule topologique.
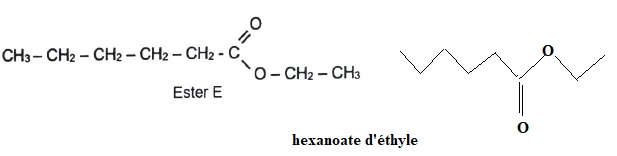
2. Ecrire
les formules semi-dťveloppťes de l'acide carboxylique A et de l'alcool
B intervenant dans la synthŤse de E. Nommer chacun d'eux.
CH3-CH2-CH2-CH2-CH2-COOH acide hexanoÔque
CH3-CH2OH ťthanol.
Pour obtenir E, on chauffe ŗ reflux un volume d'alcool Valcool = 20,0 mL avec un volume d'acide carboxylique Vacide = 43,0 mL en prťsence d'acide sulfurique. On obtient mE = 33,1 g d'ester E.
3. Justifier le double intťrÍt du chauffage ŗ reflux.
La tempťrature est un facteur cinťtique. En travaillant ŗ tempťrature
modťrťe, on accťlŤre la rťaction en ťvitant les pertes de matiŤre. Les
vapeurs se condensent dans le rťfrigťrant et retombent dans le milieu
rťactionnel.
4. L'acide sulfurique est un catalyseur. Citer la dťfinition d'un catalyseur.
Un catalyseur augmente la vitesse de la rťaction. La composition du mťlange ŗ l'ťquilibre n'est pas modifiťe.
Le catalyseur intervient lors d'une ťtape de la rťaction et se trouve rťgťnťrť lors de la derniŤre ťtape.
5. Montrer que les rťactifs sont en proportions pratiquement stoechiomťtriques et calculer le rendement de cette synthŤse.
Acide A : masse volumique 0,930 g / mL.
Masse = 0,93 x 43,0 =39,99 g.
M(acide) = 116,2 g /mol ; n(A) = 39,99 / 116,2 ~0,344 mol.
Alcool B : mase volumique ; 0,789 g / mL.
masse : 0,789 x 20,0 =15,78 g.
M(B) = 46,1 g / mol ; n(B) ~0,342 mol.
Quantitť de matiŤre d'ester si la rťaction est totale : 0,34 mol.
M(E) =144,2 g / mol.
Mase thťorique d'ester = 0,34 x144,2 ~49,4 g.
Rendement = masse rťelle / masse thťorique = 33,1 / 49,2 ~0,67 ( 67 %).
Pour amťliorer le rendement, on rťalise trois synthŤses en faisant
varier diffťrents paramŤtres. Pour chaque synthŤse, un suivi temporel
de la concentration en acide carboxylique est rťalisť par titrage.
|
Volume d'acide (mL)
|
volume d'alcool (mL)
|
catalyseur
|
tempťrature (įC)
|
synthŤse 1
|
43
|
20
|
oui
|
50
|
synthŤse 2
|
43
|
25
|
oui
|
50
|
synthÁse 3
|
43
|
20
|
oui
|
70
|
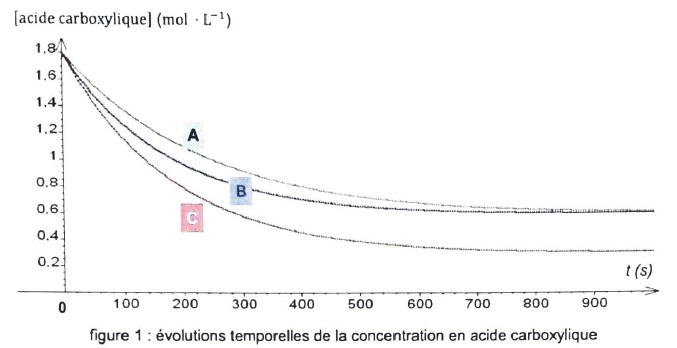
6.
Identifier les conditions expťrimentales, en prťcisant le numťro de la
synthŤse, pour lesquelles la rťaction est la plus lente. Prťciser la
courbe associťe.
Courbe A et synthŤse 1 : proportions stoechiomťtriques, catalyseur et tempťrature de 50įC.
7.
Identifier les conditions expťrimentales, en prťcisant le numťro de la
synthŤse, pour lesquelles le rendement de la rťaction est amťliorť. Prťciser la
courbe associťe.
Courbe C et synthŤse 2 : alcool en excŤs, catalyseur et tempťrature de 50įC. ( il reste peu d'acide carboxylique ŗ l'ťquilibre).
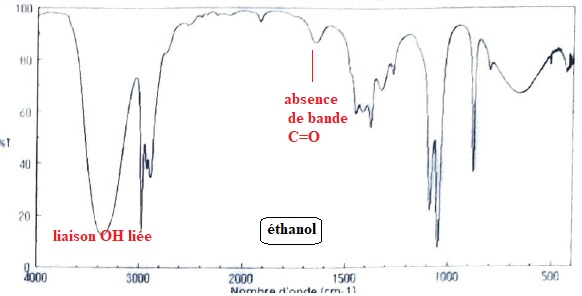
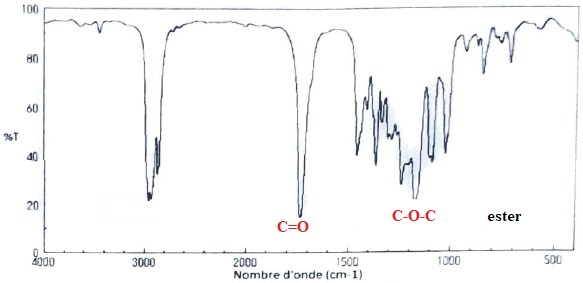
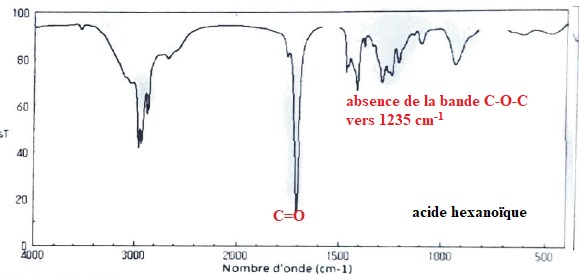
On
donne les spectres infrarouge de chacun des rťactifs avant la synthŤse
et du produit organique isolť et purifiť aprŤs la synthŤse.
8. Identifier celui de l'ester en justifiant.
|
...
|
....
|
Etude de l'eau de brassage d'une biŤre brune.
L'eau utilisťe doit contenir des ions chlorure ŗ une concentration massique comprise entre 100 mg et 200 mg / L.
On souhaite savoir si une eau de source peut convenir au brassage. On
titre les ions chlorure de cette eau par une solution de nitrate
d'argent. Le titrage est suivi par conductimťtrie.
Il faut que la transformation associťe au titrage soit rapide et totale. Pour cela on mťlange dans un tube ŗ essai :
V1 =2,0 mL de solution aquueuse de chlorure de sodium de concentration C1 =0,050 mol/L et V2=2,0 mL de solution aqueuse de nitrate d'argent de concentration C2=0,0425 mol / L.
On observe la formation immťdiate d'un prťcipitť blanc, de chlorure d'argent.
Ag+aq +Cl-aq --> AgCl(s). k = 6,4 109.
9. Montrer qu'ŗ l'ťquilibre, l'avancement xťq peut Ítre dťterminť par la rťsolution de l'ťquation :
K = (V1+V2)2 / ((V1C1-xťq)(V2C2-xťq)).
K = 1 /([Ag+]ťq [Cl-]ťq).
[Ag+]ťq= (V2C2-xťq) / (V1+V2).
[Cl-]ťq= (V1C1-xťq) / (V1+V2).
Les solutions de cette ťquation sont :
x1 = 1 10-4 mol et x2 =8,5 10-5 mol.
Quelle solution doit Ítre retenue ?
V1C1 =2,0 x0,05 10-3 =1 10-4 mol.
V2C2 =2,0 x0,0425 10-3 =8,5 10-5 mol.
xťq < 8,5 10-5 mol. ( on retient x2).
10. Cette transformation est-elle adaptťe au titrage des ions chlorures.
Oui, la trasformation est totale ( tous les ions chlorure ont rťagi ) et de plus rapide.
Dosage par titrage de l'eau de source.
On prťlŤve un volume V1 = 100,0 mL d'eau de source que l'on
introduit dans un grannd becher dans lequel on plonge une cellule
conductimťtrique. A l'aide d'une burette graduťe, on ajoute
progressivement une solution aqueuse de nitrate d'argent de
concentration C3 = 1,00 10-2 mol/ L.
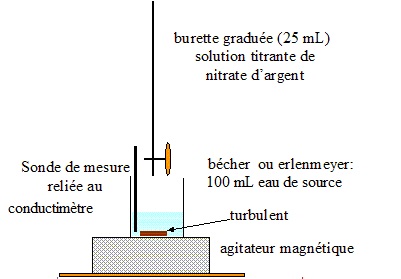
11. Faire un schťma lťgendť du dispositif utilisť lors de ce titrage.
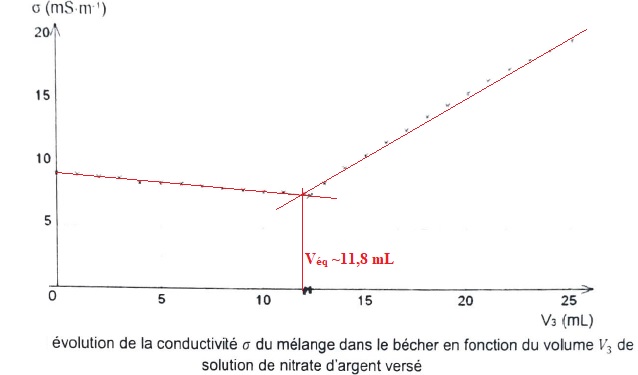
2. Justifier l'allure de la courbe.
L'ion
argent est en dťfaut avant l'ťquivalence ; du point de vue de la
conductivitť, tout revient ŗ remplacer l'ion chlorure par l'ion nitrate
de conductivitť molaire ionique un peu plus faible.
La conductivitť, et en consťquence la conductance de la solution diminue lentement.
- l'augmentation de la conductance G aprŤs l'ťquivalence.
L'ion
argent est en excŤs aprŤs l'ťquivalence. On ajoute des ions argent et
nitrate ŗ la solution. La conductivitť de la solution va croÓtre assez
vite.
13. Indiquer si la teneur en ion chlorure de cette eau peut convenir pour la fabrication de la biŤre.
A l'ťquivalence : [Cl- ] V1 = Vťq C3;
[Cl- ] V1 = Vťq C3 / V1 =11,8 x 1,00 10-2 / 100 =1,18 10-3 mol / L.
Titre massique en ion chlorure : 1,18 10-3 M(Cl) =1,18 10-3 x35,5 = 4,19 10-2 g / l ( ~42 mg / L).
Cette valeur n'ťtant pas comprise entre 100 et 200 mg/L, cette eau de source ne convient pas.
|
|