Principes de la chimie verte.
Polymères de l'acide lactique. Capes 2018.
En
poursuivant votre navigation sur ce site, vous acceptez l’utilisation
de Cookies vous proposant des publicités adaptées à vos centres
d’intérêts.
|
|
......
.....
|
Le poly(acide lactique), PLA présente un double intérêt en chimie verte :
l'acide lactique peut être généré grâce à des ressources renouvelables ;
le PLA est entièrement biodégradable.
Un devoir surveillé est proposé en terminale S.
Q31. Corriger la copie présentée dans le documen réponse.
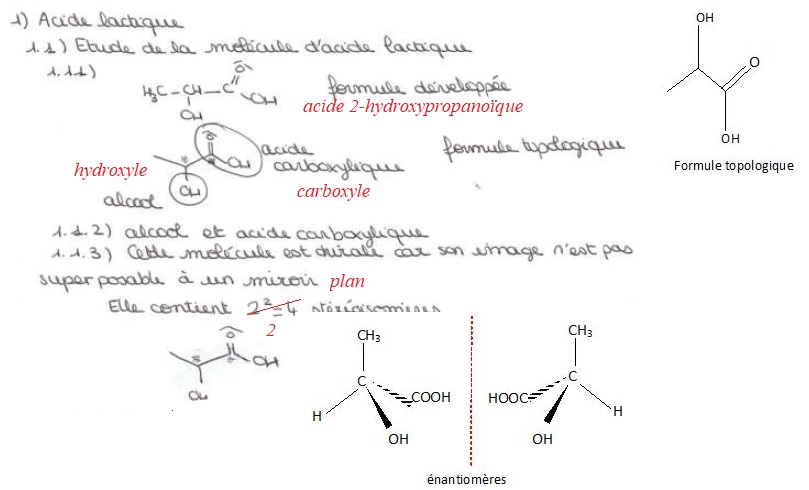
La formule semi-développée de l’acide lactique est la suivante :
1.1. Étude de la molécule d’acide lactique
1.1.1. Donner la formule topologique de cet acide et le nommer.
1.1.2. Entourer sur la représentation précédente les groupes caractéristiques présents dans la molécule et les nommer.
1.1.3. Justifier la chiralité de la molécule d’acide lactique et représenter ses stéréoisomères. Préciser le type de stéréoisomérie.
1.2. Analyse spectroscopique
1.2.1. Parmi les spectres IR proposés dans le document ci-après, choisir en justifiant celui correspondant à l’acide lactique.
1.2.2. Prévoir, en justifiant la réponse, le nombre de signaux présents
dans le spectre RMN de l’acide lactique ainsi que leur multiplicité.

2. Polymérisation de l’acide lactique
Une molécule d’acide lactique peut, dans certaines conditions, réagir avec une autre molécule d’acide
lactique pour former une molécule de chaîne plus longue, à six atomes
de carbone. À son tour cette dernière peut réagir avec une autre
molécule d’acide lactique pour donner une molécule encore plus longue
et ainsi de suite. On obtient ainsi une molécule de polymère constituée
d’un très grand nombre d’atomes de carbone, appelée acide polylactique,
reproduisant régulièrement le même motif d’atomes.
L’acide polylactique est un polymère biodégradable : l’action de l’eau peut le détruire en régénérant l’acide lactique.
2.1. La polymérisation de l’acide lactique est-elle lente ou rapide ? Justifier.
2.2. Citer un paramètre influençant l’évolution temporelle de cette réaction chimique.
2.3. Proposer un protocole permettant de vérifier que l’acide sulfurique est un catalyseur de cette réaction.

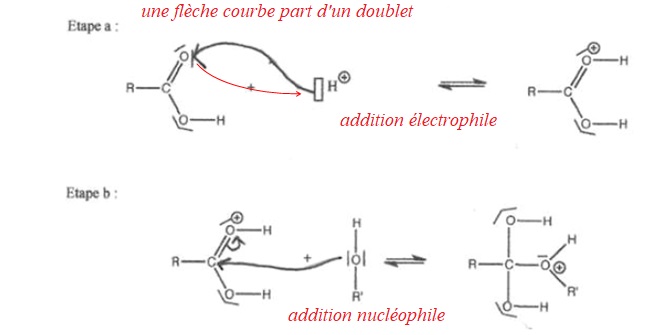
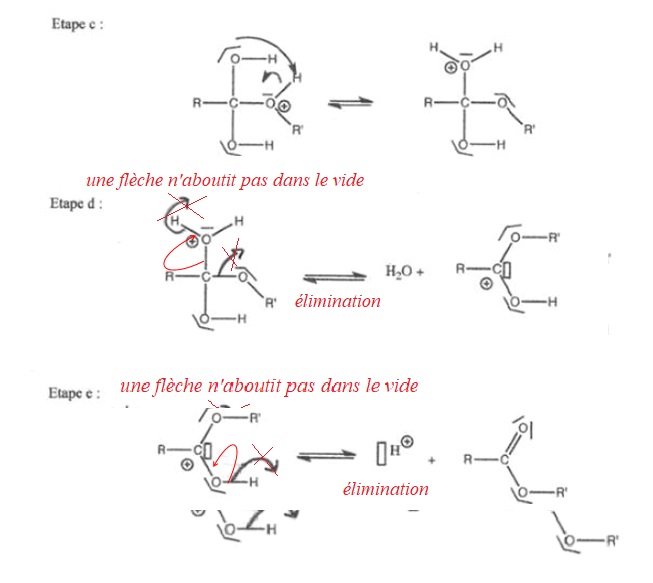
2.4. Le mécanisme simplifié de la réaction de polymérisation est proposé sur l’annexe à rendre avec la copie.
2.4.1. Représenter les flèches courbes rendant compte du mécanisme des étapes a, b, d et e.
2.4.2. Pour chacune des étapes a, b, d et e, indiquer la catégorie de la réaction.
Q32. Préciser les compétences exigibles qui ne sont pas acquises.
Une fonction doit être associée à un groupe caractéristique.
Identifier un atome de carbone asymétrique ; revoir la représentation de Cram.
RMN : la multiplicité d'un signal est lié au nombre de protons des carbones voisins.
Revoir les flèches courbes dans un mécanisme.
Préciser la catégorie d'une réaction.
|
...
|
|
.
|
....
|
La
synthèse du PLA à partir d’acide (DL)-lactique est réalisée en classe
avec les élèves de terminale S suivant l’enseignement de spécialité.
Q34 Donner la signification des notations L et D. Qu’est-ce que l’acide (DL)-lactique ?
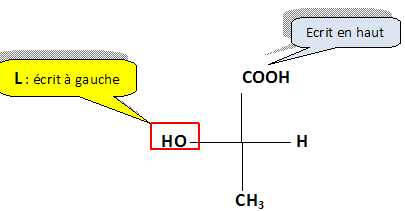
D signifie : le groupe OH est écrit à droite dans cette représentation.
L'acide (DL)-lactique correspond au mélange récémique constitué pour 50 % de chaque énantiomère.
Q35 Lequel des deux acides (acide (L)-lactique ou acide (D)-lactique) est de configuration S ? Justifier la réponse.
Numéroter de façon décroissante
chacun des quatre substituants selon son numéro
atomique.
OH (1) ; COOH (2) ; CH3 (3) ; H (4).
On place alors l'atome (ou le groupement) de
numéro le plus élevé
derrière.
On regarde dans quel sens, sens horaire ou
trigonométrique, on passe du numéro 1, au 2,
au 3.
- Si le sens de rotation est le sens horaire (ou
anti-trigonométrique), le carbone est Rectus (R),
- Si le sens de rotation est le sens
trigonométrique (ou anti-horaire), le carbone est
Sinister (S).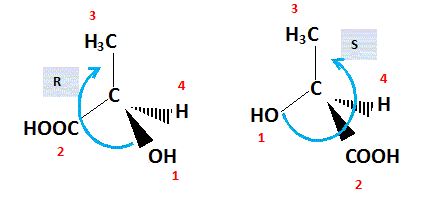
L'acide ( L) lactique est de configuration S.
L’acide lactique de configuration S a un pouvoir rotatoire spécifique de +3,8 °C·dm−1·cm3·g−1 à 25 °C. Un échantillon de concentration c =1500 g·L−1 est analysé dans un polarimètre de Laurent à l’aide d’une cuve de longueur 20 cm : une déviation de +10,5 °est mesurée.
Q36 Quelle est la pureté optique de l’échantillon ? Sachant que l’excès énantiomérique noté « ee » s’exprime selon ee = (xS − xR), en déduire la valeur de la fraction molaire xS de l’acide lactique S dans l’échantillon.
20 cm = 2 dm ; 10,5 = 3,8 x 2,0 xC S ; CS = 10,5 / 7,6 = 1,38 cm-3;
pureté : 1,38 / 1,5 = 0,92 ( 92 %).
xR + xS = 1 et xS-xR = 0,92
xS = (1+0,92) / 2 = 0,96 et xR = 0,04.
Q37 Écrire l’équation de la réaction de polymérisation mettant en jeu n molécules d’acide lactique.
Quelle est la masse molaire d’un motif constitutif du polymère ? À quelle grande famille de polymères le PLA appartient-il ?
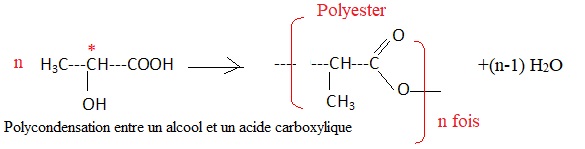
M(motif élémentaire) = 3 x12 + 4 + 2 x16 = 72 g / mol.
|
|







