Principes de la chimie verte.
Pourcentage d'économie d'atomes. Capes 2018.
En
poursuivant votre navigation sur ce site, vous acceptez l’utilisation
de Cookies vous proposant des publicités adaptées à vos centres
d’intérêts.
|
|
......
.....
|
Notion
d'économie d'atomes.
Les alcloïdes et leurs dérivés constituent une classe de molécules
ayant des propriétés pharmacologiques importantes. L'aspidospermine (-)
peut être obtenue à partir du lactame (3) préparé à partir du dérivé
cyclohexènique (4) lui même issu du triène (5) par RCM. La partie qui
suit se limite à l'étuse de l'obtention de (4) à partir de l'alcool
diènylique (6).
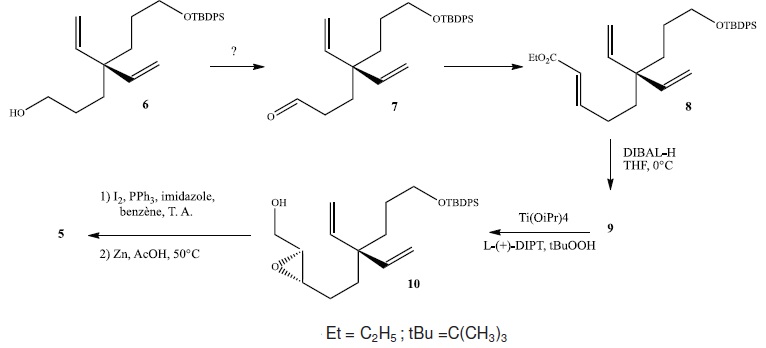
Q19. A quel type de
réaction correspond le passage du composé 6 au composé 7. Porposer un
réactif permattant d'effectuer cette transformation.
L'oxydation ménagée d'un alcool primaire en aldehyde peut être réalisée
à l'aide du permanganate de potassium utilisé en quantité
stoechiométrique ( un excès d'oxydant conduirait à l'acide carboxylique
).
L'aldehyde 7 formé a une masse molaire de 402,1 g / mol et sera noté
RCHO par la suite. La préparation de 8 se fait selon deux étapes.
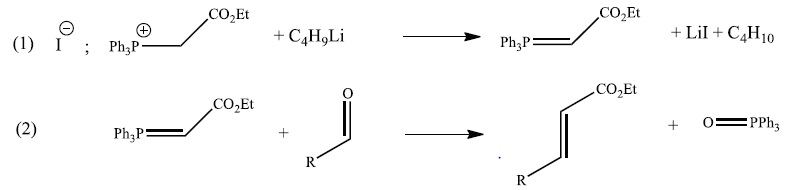
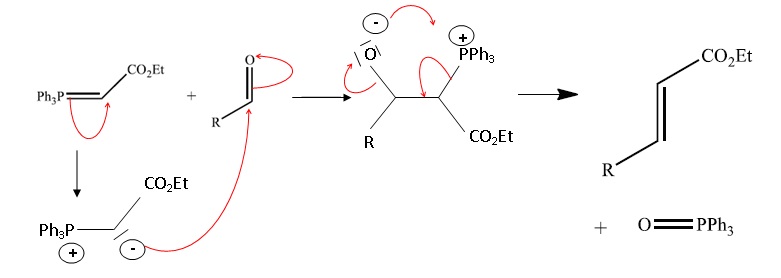
Q20. Donner le
mécanisme de la deuxième étape.( Réaction de Wittig )
Le
pourcentage d'économie d'atomes est calculé en effectuant le rapport de
la masse molaire du produit désiré sur la somme des masses molaires de
tous les réactifs pondérés par leur coefficient stoechiométrique.
Q21. Calculer le pourcentage
d'économie d'atomes de la réaction 7 ---> 8.
Masse
molaire des réactifs : M(7) = 420,1 g / mol ;
M(I- ; +PPh3CH=CHCO2Et)
=127 +31 + 3x(6 x12+5) +12+1+12+1+12+2 x16 +2x12 +5) =488 g/mol.
M( C4H9Li) =4 x12 +9 +6,9 =63,9 g/mol.
M(8) = M(7) - 16+12+1+M(CO2Et) = 490,1 g/mol.
Economie d'atomes = 490,1 / (420,1 +63,9 +488) =50 ( 50 %).
|
...
|
|
Le réactif di-isobutylhydrure
d'aluminium noté DIBAL-H a pour formule :
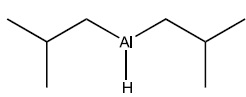
Q22.
Donner la formule topologique du composé 9. ( C29H40O2Si).
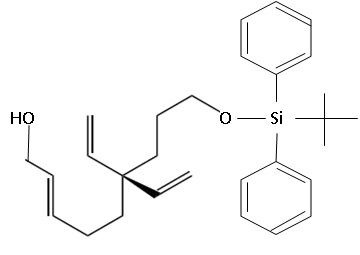
Le
composé 9 subit une époxydation asymétrique de Katsuki- Sharplesse et
forme 10 avec un fort excès énantiomérique ( ee > 99 %). Le
catalyseur est à base d'un complexe de titane Ti (OiPr)4 et
le L-(+)-DIPT est un catalyseur qui se coordine au titane lors de la
réaction..
Q23. Citer un autre
catalyseur permettant d'effectuer l'epoxydation de 9.
Un peracide peut être utilisé.
Q24. Quels sont les
rôles respectifs du peroxyde de tertiobutyle tBuOOH et du L-(+)-DIPT ?
tBuOOH est l'un des réactifs de la réaction catalysée par le L-(+)-DIPT.
Q25. Indiquer
l'intérêt de l'époxydation asymétrique par rapport à une époxydation
classique.
Lors d'une époxydation classique :
Le pont "oxygène se forme soit au
dessus du plan de la double liaison, soit en dessous : en conséquence,
à partir de l'alcène suivant, plusieurs énantiomères sont obtenus.
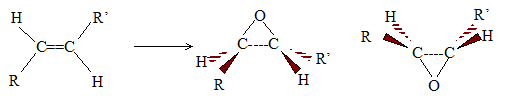
Par contre une époxydation asymétrique est stéréosélective.
Q26. Expliquer, en
une dizaine
de ligne maximum, comment un professeur d'une classe de terminale
STL-SPCL pourrait utiliser cette synthèse pour illustrer la notion de
régiosélectivité.
Le composé 8 compte 3 doubles liaisons C=C susceptibles de subir une
époxydation ( remplacement d'une liaison par un pont oxygène ). Donc
trois produits devraient être obtenus. Or on obtient uniquement le
produit (10). On dit que cette époxydation est régiosélective.
|
....
|
Formation du composé cyclique (4) par RCM.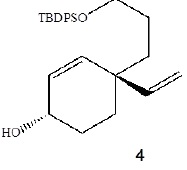
Pour simplifier, le complexe carbène-ruthénium

La fermeture du cycle par métathèse peut se résumer par le schéma
suivant.
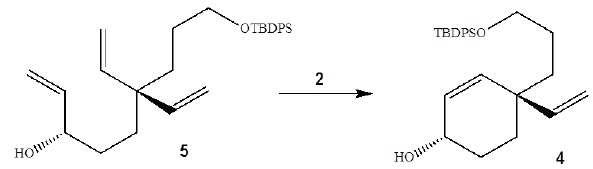 + H2C=CH2. + H2C=CH2.
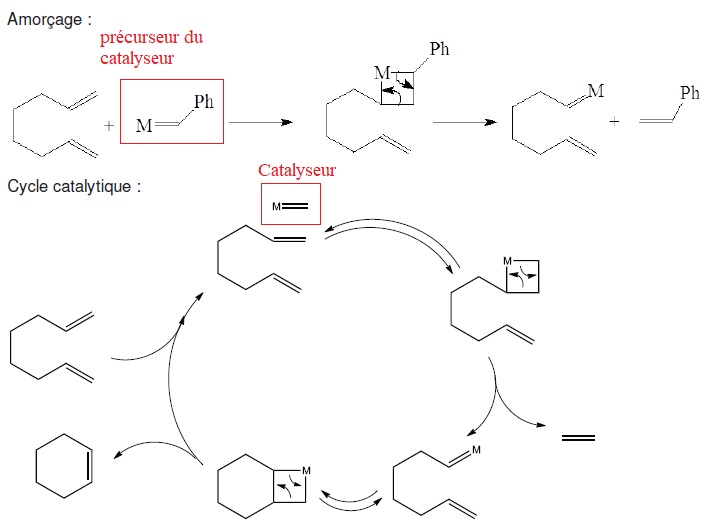
L'un des mécanisme possible pour la RCM est exposé ci-dessous.
Q27. Indiquer le
précurseur de catalyseur et le catalyseur de la réaction.
Q28. Compléter
l'équation de la transformation 5 ---> 4 en ne prenant en compte que
les produits principaux.
Q29. Sachant que la masse molaire de
5 est 448,1 g / mol, calculer le pourcentage d'économie d'atomes de la
métathèse par la fermeture du cycle. Comparer avec la valeur trouvée
pour la transformation 7 ---> 8 et conclure.
M(4) = M(5) - M(CH2=CH2) = 448,1 - 28 = 420,1
g/mol.
Economie d'atomes = M(4) / M(5) = 420,1 / 448,1 ~ 0,94 ( 94 %).
Pour l'ensemble de la synthèse, l'étape 7 --> 8 limite l'économie
d'atomes.
Q30.. Un chimiste français s'est illustré par ces travaux sur la
métathèse en recevant le prix Nobel de chimie en 2005 avec deux
chercheurs américains. Quel est son nom ?.
Yves Chauvin.
|
|









