Le
kétoprofène, bac S Nlle Calédonie 2019.
En
poursuivant votre navigation sur ce site, vous acceptez l’utilisation
de Cookies vous proposant des publicités adaptées à vos centres
d’intérêts.
| .
. |
......
.....
|
Masse molaire du kétoprofène M =254 g / mol.
Le kétoprofène est soluble dans l'éthanol et très peu soluble dans l'eau.
L'eau et l'éthanol sont miscibles.
1. Etude de la structure du kétoprofène.
L'un des énantiomères du kétoprofène est représenté ci-dessous.
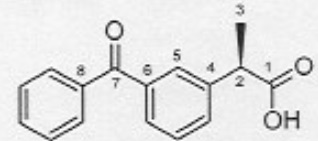
1.1. Justifier que cette molécule est chirale.
Le carbone n°2 est tétraèdrique et lié à 4 goupes d'atomes différents. Il est asymétrique.
Une molécule possèdant un atome de carbone asymétrique est chirale.
1,.2. Représenter l'autre énantiomère du kétoprofène.
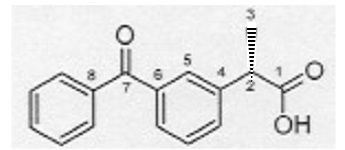
1.3 Entourer les groupes caractéristiques présents et nommer les familles chimiques correspondantes.
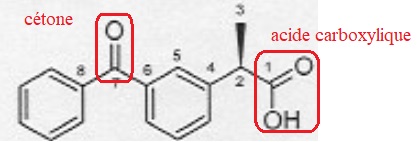
1.4. Dans le
spectre RMN, quelle est la multiplicité attendue pour les groupes de
protons équivalents portés par les atomes de carbone 2 et 3 ?
Le carbone n°3 porte 3 protons. Le signal du proton du carbone n°2 est donc un quadruplet.
Le carbone n°2 porte un proton. Le signal du carbone n°3 est donc un doublet.
1.5. Dans le médicament, les deux énantiomères sont présents dans les mêmes proportions. Comment appelle t-on ce type de mélange ?
Il s'agit d'un mélange racémique.
|
|
.
|
....
|
Analyse d'un comprimé comportant du kétoprofène.
Le kétoprofène est noté R-COOH. On cherche à déterminer la masse mK de kétoprofène contenue dans un comprimé.
Protocole :
Ecraser 5 comprimés dans un mortier.
Ajouter 60 mL d'éthanol. Les excipients ne sont pas solubles dans l'éthanol. Filtrer.
Rincer 3 fois le papier filtre avec 10 mL d'éthanol.
Introduire le filtrat dans une fiole jaugée de 100 mL et compléter avec de l'éthanol ; on obtient la solution S.
Prélever 20,0 mL de cette solution et ajouter quelques gouttes de rouge de crésol.
Titrer par une solution aqueuse d'hydroxyde de sodium de concentration CB = 1,00 10-2 mol / L.
2.1. Expliquer l'intérêt de rincer le papier filtre avec de l'éthanol.
On récupère dans le filtrat tout le kétoprofène. Les excipients ne sont pas solubles dans l'éthanol.
2.2. Faire un schéma légendé du dispositif de titrage.
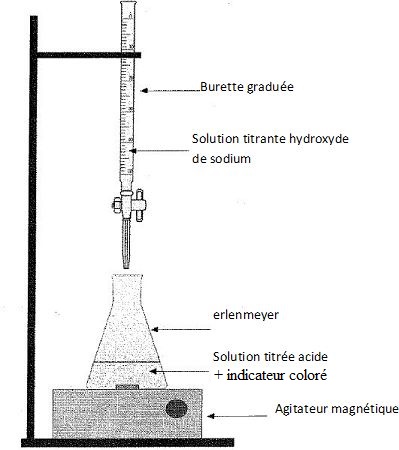
2.3 Ecrire l'équation de la réaction support du titrage.
RCOOH aq + HO-aq ---> RCOO-aq + H2O(l)
2.4 Indiquer à quelle condition un indicateur coloré est adapté au suivi d'un titrage acido-basique.
La zone de virage de l'indicateur coloré doit contenir le pH du point équivalent.
2.5. Une série de titrages permet d'obtenir un volume équivalent VE = 9,8 ±0,1 mL.
La détermination de ce volume est la principale source d'incertitude.
U(mK) / mK = U(VE) / VE.
Déterminer un encadrement de mK et vérifier si les mesures sont compatibles avec les informations de la notice.
(25 mg kétoprofène par comprimé ).
A l'équivalence la quantité de matière de solution titrante est : n = CB VE =1,00 10-2 x 9,8 =9,8 10-2 mmol.
9,8 10-2 mmol de kétoprofène dans 20,0 mL de prise d'essai.
Soit 5 x9,8 10-2 = 0,49 mmol dans 100 mL ou dans 5 comprimé.
Masse correspondante : mK = 0,49 x 254 / 5 = 24,892 mg.
U(mK) / mK = U(VE) / VE = 0,1 / 9,8 ~0,01.
U(mK)=24,892 x0,01 ~0,249 ~0,2 mg.
mK = 24,9 ±0,2 mg, en accord avec la valeur de la notice.
|
|



