Chimie
analytique, Concours interne technicien de la police technique et
scientifique 2018
En
poursuivant votre navigation sur ce site, vous acceptez l’utilisation
de Cookies vous proposant des publicités adaptées à vos centres
d’intérêts.
|
|
|
|
Partie
A.
1. Expliquer comment réaliser le dosage de l'alcool dans le sang.
L’éthanol
contenu dans10 mL de sang est séparé par distillation, en présence
d’acide picrique qui a une action défécatrice et antimousse. Le
distillat est recueilli dans une fiole jaugée de 50 mL contenant de
l’eau distillée et placée dans un bain réfrigérant. La solution aqueuse
d’éthanol est alors mise en présence d’une solution nitrochromique
(mélange d’acide nitrique et de dichromate de potassium) à froid et en
excès. L’excès d’ions dichromate est dosé en retour par iodométrie. Un
essai à blanc est pratiqué en parallèle par remplacement de la solution
aqueuse obtenue à partir du distillat par de l’eau distillée.
2. L'analyse du taux d'alcoolémie a été réalisée trois heures après l'accident, qu'est ce que cette information vous apporte ?
Après 4 verres de vin et un taux maximum estimé à 0,8g/L dans le sang,
il faut en moyenne 2 heures pour revenir sous les 0,5g/L. Au
moment de l'accident le taux d'alcoolémie était bien supérieur à 0,8 g
/ L.
3.
Que signifie la présence uniquement de THC-COOH dans le sang ?
Le test de dépistage sanguin permet de détecter la consommation de
cannabis dans un délai de 2 à 10 heures après la prise. Il permet
d'estimer le temps entre la dernière consommation et la prise de sang.
4. La famille
déclare ne pas savoir que leur fils consommait régulièrement de
l'elcool et des substances illicites. Quels moyen avez-vous de savoir
si c'était un consommateur régulier ou occasionnel ?
Dans les cheveux la consommation de canabis peut se voir plusieurs mois après, les traces de THC ne disparaissent pas.
L'alcool est la cause principale des cirrhoses du foie. Le test
capilliare de l'Etg permet de réaliser un dépistage de la consommation
abusive d'alcool et de connaître le niveau de consommation d'alcool au
cours des trois derniers mois.
.
Partie B.
1. Comment une trace de peinture apparente sur le scooter accidenté est-elle analysée ?
Le spectre infrarouge de chaque couche ( vernis, apprêt, teinte et
couche anticorrosion ) est comparé avec ceux de la base de données
conservant les caractéristiques des peintures de 4000 véhicules. La
probabilité d'idenfier la marque et le type de véhicule est de 70 %.
2.
L'analyse de la trace de peinture apparente sur le scooter révèle
qu'elle est composée d'écailles de peinture à deux couches :
vernis et teinte. La base de données indique une automobile de marque
Citroên modèle C3 de couleur bleu outre-mer. Examinez les spectres de
supeprosition des vernis et des teintes. Que pouvez-vous en déduire ?
Justifier.
On observe une concordance parfaite entre les spectres de la
trace retrouvée sur le scooter et le spectre de teinte de la Citroën C3.
Les pics au nombre d'onde suivants figurent sur les deux spectres :
3375 ; 2963 ; 2935 ; 2874 ; 1728 ; 1609 ; 1547 ; 1508 ; 1473 ; 1420 ; 1374 ; 1333 ; 1286 ; 1240 ; 1166 ; 1093.
Par contre la concordance est faible en comparant le spectre de la
trace retrouvée sur le scooter et le spectre du vernis de la Citroën C3.
Seuls 4 pics concordent ( 1235 ; 1728 ; 1374 ).
Il s'agit donc d'un véhicule de teinte bleu outre-mer, mais pas nécessairement Citroën C3.
3. Quelles sont les
techniques les plus discriminantes qui permettent de différencier un
fragment de verre provenant du phare d'un scooter, d'une vitre de
voiture ( float glass ) ?
Microscope électronique : informations sur la morphologie et la composition.
4. Sous quelle forme se présentent les éléments chimiques constitutifs d'un verre minéral ?
Les verres présentent une structure amorphe, non cristalline.
Un verre est une substance qui s'apparente à un liquide par sa
struicture chimique ; sa viscosité étant très élevée à température
ambiante, il s'apparente à un corps solide.
5. Peut-on retrouver du plomb dans un fragment de verre ? Justifier.
Le plomb est utilisé pour donner un éclat particulier " le
cristal ". Le verre feuilleté des pare-brises ne contient pas de plomb.
|
|
Partie C.
1. Quelle(s) substance(s), parmi la liste suivante, est (sont) classée(s) parmi les stupéfiants ?
Bicarbonate de soude ( non) ; cocaïne ( vrai) ; lactose (non ).
2. A quoi servent ces substances, peut-on diluer l'une avec l'autre ?
On ajoute un produit de moindre valeur à la cocaïne afin de la couper.
Bicarbonate de soude : poudre cristalline à base de craie ; lactose : glucide ; cocaïne : poudre blanche.
Ces trois poudres peuvent parfaitement être mélangées.
3. Expliquer la différence entre la cocaïne base et chlothydrate. Comment passe t-on d'une forme à l'autre ?
Le chlorhydrate de cocaïne se présente sous la forme d'une poudre
blanche. Chaufée en présence d'ammonique ou de bicarbonate de soude, on
obtient la cocaïne base solide cristalisée ( petits cailloux
destinés à être fumés ).
Les effets de la cocaïne base sont plus puissants, leur apparition est
rapide ( 1 à 2 minutes contre 15 à 30 minutes ), mais leur durée est
plus courte ( 10 à 15 min contre une heure ). Les usagers multiplient
les prises.
4. Dans la
fabrication du crack on utilise préférentiellement du bicarbonate de
soude, quelle autre substance chimique peut lui être substituée ?
L'ammoniaque.
5.a. A quelle famille de molécule appartient la cocaïne ? Citez une autre substance de cette famille n'ayant pas les mêmes effets.
La cocaïne est un alcaloïde tropanique ( molécules à base azotée,
majoritairement d'origine végétale ) extrait de la feuille de
coca.
L'atropine, la scopolamine.
5.b. Quels sont les modes de consommation de la cocaïne ? Ont-ils des conséquences sur les effets ?
Ingestion par voie orale ( magée, dissoute dans l'eau, gobée ) : ce mode engendre peu de dépendance.
Respirée, inhalée : la poudre déposée sur une feuille d'aluminium est
chauffée par dessous avec un briquet : montée rapide des effets et
durée d'action brève.
Injection par piqure intraveineuse : action rapide de courte durée provoquant une dépendance.
5.c. On vous demande de comparer trois échantillons de ccaïne afin de savoir si l'origine est commune.
Echantillon A
|
cocaïne 80 %
|
lévamisole 5 %
|
| Echantillon B |
cocaïne 70 % |
lévamisole 6 % |
| Echantillon C |
cocaïne 90 % |
lévamisole traces non dosées
|
Est-ce suffisant pour conclure à une origine de fabrication commune ? Que recherchez-vous et comment ?
Non, ce nest pas
suffisant ; il faut rechercher les différentes espèces chimiques
contenues dans chaque échantillon par chromatographie.
Les échantillons A et B présentent un grand nombre de pics communs (
temps de rétention ( min) :3,663 ;4,888 ;5,779 ; 5,997 ; 6,449 ; 7,225
; 7,530 ; 7,635 ; 8,423 ; 8,593 ; 8,884 ; 10,153 ; 10,250 ; 11,242 ;
13,141 ; 16=3, 932).
A et B ont la même origine.
Par contre le chromatogramme de C et ceux de A ou B présentent très peu de pics communs : C est d'origine différente.
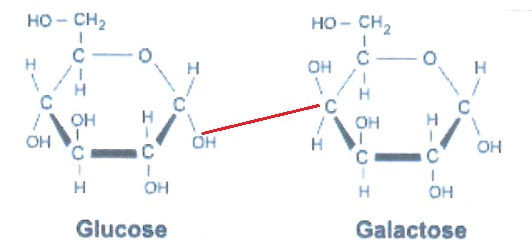
6. La formule brute du lactose est C12H22O11.
C'est un sucre combinant deux sucres simples, le glucose et le
galactose relié par une liaison osidique. Matérialiser la liaison
osidique entre les deux molécules.
Vous ne disposez comme matériel que d'un GCMS, cette technique est-elle
adptée à l'identification des sucres ? Quelle transformation allez-vous
faire subir à l'échantillon ?
Les sucres sont trop peu volatils pour permettre une chromatographie en
pase gazeuse directe. Il faut les rendre plus volatils en formant des
ester acétylés par exemple.
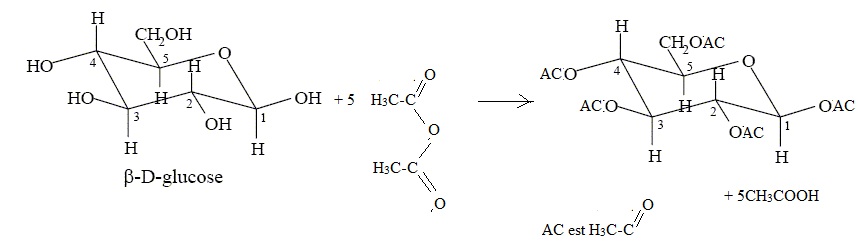
Si vous utiliser l'anhydride acétique, vous allez greffer un groupement
acyle à la molécule. Ecrire la réaction chimique dans le cas du glucose.
La lactase permet de transformer le lactose en glucose et galactose,
comment s'appelle cette réaction. Quelle est la nature du lactase ?
La lactase est une enzyme permettant la dissociation ( hydrolyse ) du
lactose en glucose et galactose. Cette enzyme nous permet de bien
digérer le lactose.
|
|
II. Hygiène et sécurité.
Quelle est la particularité de la cocaïne quand vous la manipulez ? Quelles sont vos protections individuelles lors de cette manipulation ?
La poudre blanche de cocaïne est légèrement volatile. Travail sous hotte aspirante, port de gants et blouse.
Quel est l'autre nom chimique du trichlorométhane ? Donnez la
signification des pictogrammes de ce produit. A quoi correspond la
codification H.?
Qu'appelle-t-on CMR ? Cette substance en fait-elle partie ?

Autre nom : Chloroforme.
Toxique, cancèrogène, tératogène.
Codification H : mentions de dangers.
CMR : certains agents chimiques ont des effets cancèrogène, mutagènes
ou toxiques pour la reproduction. Le trichlorométhane en fait partie.
III. Exercices.
1. Préparation d'une solution tampon.
On met dans un becher 50 mL de NH3 aq 1 mol / L et 50 mL de NH4Cl 1 mol / L ( pKa (NH4+ / NH3) = 9,26 ).
Calculer le pH de cette solution.
[NH3] = [NH4+] ; pH = pKa = 9,26.
On ajoute à cette solution 150 mL de NaOH 0,1 M. Quel est le pH obtenu ?
NH4+aq + HO- aq --> NH3 aq + H2O(l).
Quantité de matière de soude ajoutée : 0,150 x0,1 = 0,015 mol.
0,015 mol d'ion NH4+disparaît ; il en reste 0,050 x1 -0,015 = 0,35 mol.
Il apparaît 0,015 mol NH3 ; il y en a donc 0,050 x1 +0,015 = 0,065 mol.
pH = pKa + log ( [NH3] /[NH4+] ) =9,26 + log( 0,065 / 0,035) = 9,53.
2. Dosage de la nicotine dans le tabac.
Vous avez du tabac déshydraté sous forme de brins.
Vous préparer une solution d'extraction à partir d'une solution de
potasse KOH 0,05 N dans laquelle vous y ajoutez du dipyridyle à la
concentration de 0,25 mg / mL.
Vous préparez une solution de référence 1 : 50 mg de nicotine dans 10
mL de la solution d'extraction. Vous diluez cette solution au dixième.
a. Quelle est la concentration en mg / mL pour la référence 1 ?
50 / 10 = 5 mg / mL ; après dilution 5 / 10 = 0,5 mg / mL.
Vous obtenez le chromatogramme de la solution de référence avec les résultats suivants :
Aire dipyridyle Adipy = 8667 ; aire nicotine Anico = 12084.
Vous préparer 25 mg de tabac que vous mettez dans 1 mL de solution
d'extraction. Vous obtenez un chromatogramme pour le tabac avec les
résultats suivants : Aire dipyridyle A'dipy = 9060 ; aire nicotine A'nico = 23200.
b. Calculer la concentration en nicotine de cette solution.
Anico / Adipy =1,3942 ; A'nico / A'dipy =2,561.
2,561 / 1,3942 x 0,5 = 0,918 mg / mL.
Pour plus de précision vous décjdez de préparer trois autres références à des concentrations différentes.
|
Cnico (mg /mL)
|
Cdipy (mg /mL) |
Cnico / Cdipy |
Anico |
Adipy |
Anico / Adipy |
Réf 1
|
500
|
250
|
2
|
12084
|
8667
|
1,39
|
Réf 2
|
1000
|
250
|
4
|
24002
|
8632
|
2,78
|
Réf 3
|
250
|
250
|
1
|
9619
|
13702
|
0,7
|
Réf 4
|
125
|
250
|
0,5
|
2984
|
8429
|
0,35
|
Tracer la droite du
rapport des aires en fonction du rapport des concentrations. Trouvez
l'équation de la droite de régression, calculer le coefficient de
réponse relatif k. En déduire la concentration de la solution analysée,
comparer avec la valeur précédente et en déduire la teneur en nicotine
du tabac.
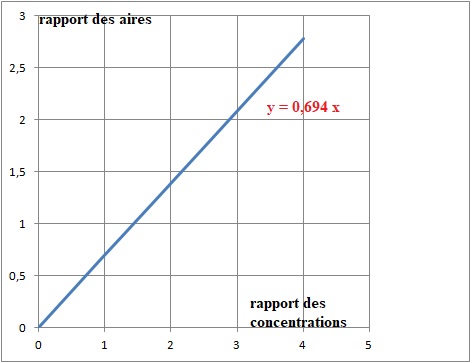
x = 1,3942 / 0,694 =2,001 ; 2,001 x 0,5 ~1,00 mg / mL.
Ecart relatif entre les deux valeurs (1-0,918) / 1 x100 =8,2 %.
Teneur en nicotine du tabac : 1 mg de nicotine dans 25 mg de tabac.
|
|