L'acide
ascorbique, Bac S métropole 2018
En
poursuivant votre navigation sur ce site, vous acceptez l’utilisation
de Cookies vous proposant des publicités adaptées à vos centres
d’intérêts.
|
|
.
.
|
|
1. Synthèse industrielle à partir du D-glucose
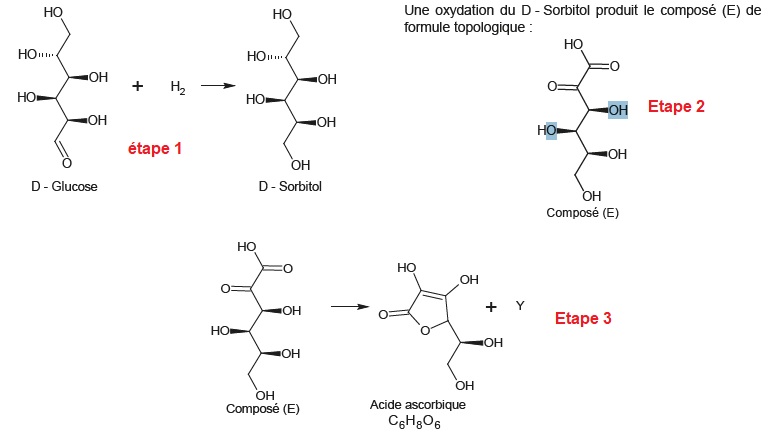
1.1. Etape 1 de la synthèse.
1.1.1. Le passage du D-glucose au D-sorbitol correspond-il à une modification de chaine ou de groupe caractéristique ?
1.1.2. Donner le nom de la catégorie de réaction. Justifier.
La chaine carbonée n'est pas modifiée. La fonction aldehyde du D-glucose est réduite en fonction alcool primaire.
Il y a deux réactifs et un seul produit ; une double liaison disparaît : addition du dihydrogène sur la double liaison C=O.
1.2. Etape 3.
1.2.1 Ecrire la formule brute du composé E.
1.2.2 Identifier Y et le nommer.
C6H10O7.
Y est H2O ( eau).
1.3. Le déroulement
de la synthèse peut être contrôlé par spectroscopie infrarouge.
Attribuer les spectre suivants au D-sorbitol et à l'acide ascorbique.
Justifier.
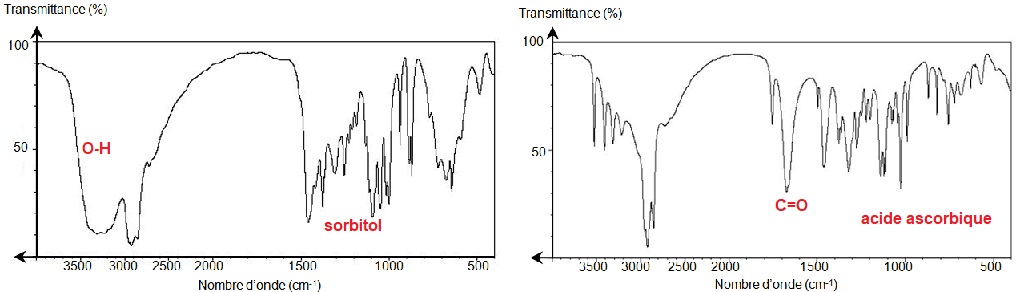
|
|
.
.
|
|
2. Titrage de l'acide ascorbique contenu dans un comprimé de "vitamine C 500".
On
dissout un comprimé de vitamine C dans de l'eau distillée afin
d'obtenir 100,0 mL de solution S. On prélève 10,0 mL de cette solution
que l'on dose par une solution d'hydroxyde de sodium de concentration
2,00 10-2 mol / L. Le titrage est suivi par pH-métrie.
Equation support du titrage : C6H8O6 aq + HO-aq ---> C6H7O6-aq + H2O.
2.1. Réaliser un schéma légendé du dispositif expérimental.
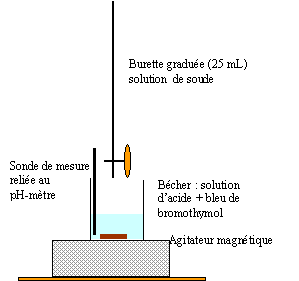
2.2. Justifier que la réaction support du titrage est une réaction acido-basique.
Il y a échange de proton H+ entre l'acide ascorbique et l'ion hydroxyde.
|
|
2.3. Déterminer la concentration molaire de l'acide ascorbique dans la solution S.
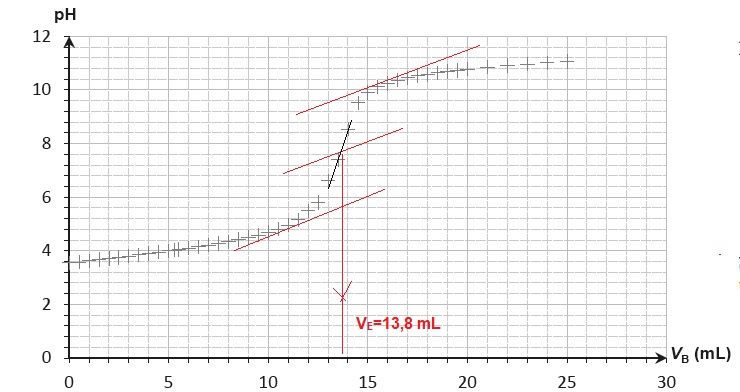
A l'équivalence :
Quantité de matière d'ion hydroxyde = quantité de matière d'acide ascoorbique.
13,8 x 2,00 10-2 = 10,0 C.
C = 2,76 10-2 mol/L.
2.4. Déterminer la
masse m de vitamine C contenue dans le comprimé. Comparer la valeur
obtenue à l'indication donnée par le fabriquant. Proposer deux sources
d'erreurs possibles, liées à la mise en oeuvre du titrage, pouvant
expliquer l'écart observé.
M(acide ascorbique) = 176 g / mol.
Quantité de matière d'acide ascorbique : 2,76 10-3 mol.
m = 2,76 10-3 x 176 = 0,486 g = 486 mg.
Ecart relatif : (500-486) / 500 x100 = 2,8 %.
Sources d'erreur :
Mauvaise lecture des volumes 10,0 mL ( pipette jaugée) et 100,0 mL ( fiole jaugée ).
Soude carbonatée, erreur sur la concentration de la soude.
Dissolution incomplète du comprimé.
|
|