A
l'approche de l'été, la mairie d'une commune fait appel à un technicien
chimiste pour analyser l'eau de sa piscine et établir un rapport.
Votre travail consiste à rédiger ce rapport dans lequel vous
présenterez le bilan des analyses de l'eau effectuées (pH, TAC, TH ) et
le traitement quantitatif à conduire pour rendre l'eau adaptée à la
baignade.
Données :
bassin de 25 m de longueur, de 10 m de largeur et de 2,5 m de
profondeur.
pH
mesuré : 8,0.
TAC = 6,0 °f.
50 mL d'eau de la piscine ont été titrés par la solution d'EDTA de
concentration molaire C
EDTA = 2,0 10
-2 mol/L.
L'équivalence a été obtenue pour un volume d'EDTA versé de 5,0 mL.
Mesure du titre
hydrotimétrique TH.
Ce titre est lié à la concentration totale en ion calcium Ca
2+aq
et magnésium Mg
2+aq.
TH(°f) =10
4([Ca
2+aq]+[Mg
2+aq]) avec
[Ca2+aq] et [Mg2+aq]
exprimées en mol/L.
l'évaluation de la somme des concentrations est effectuée par titrage
des ions Ca2+aq
et Mg2+aq .à l'aide de l'EDTA
Ca2+aq]+Y4-aq
--> (CaY)2-aq et Mg2+aq +Y4-aq
--> (MgY)2-aq.
A l'équivalence : ([Ca2+aq]+[Mg2+aq]) x50 = 2,0 10-2
x5,0 ;
([Ca2+aq]+[Mg2+aq])
= 2,0 10-2 x5,0 / 50 = 2,0 10-3
mol/L.
TF = 104
x 2,0 10-3 = 20°f.
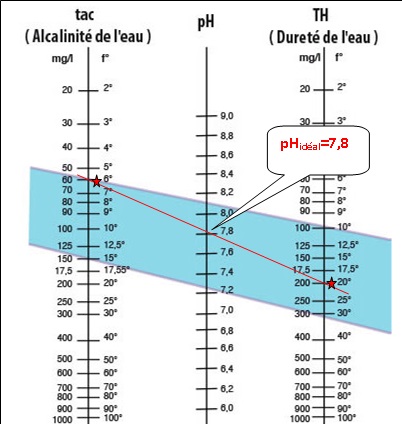
pH idéal de l'eau de la piscine.