Dessalement de
l'eau de mer. Bac S Polynésie 2016.
En poursuivant votre navigation sur ce site, vous acceptez l’utilisation de Cookies vous proposant des publicités adaptées à vos centres d’intérêts.
|
|
|
|
|
|
|
|
En Europe, des usines de dessalement
sont présentes sur les côtes de la mer Méditerranée où l’eau douce est
rare, par exemple à Barcelone en Espagne. On s’intéresse, dans cet
exercice, à l’impact environnemental des saumures rejetées dans la mer
par ces usines.
On appelle saumure la solution concentrée en composés ioniques obtenue
à la fin du processus de dessalement, majoritairement du chlorure de
sodium. Les courants marins de la mer Méditerranée sont en général
faibles et ne permettent pas une dilution immédiate des saumures
rejetées, ce qui peut perturber les écosystèmes marins.
La Posidonie de Méditerranée (Posidonia Oceanica) est une plante
aquatique qui forme de vastes herbiers entre la surface de l’eau et une
profondeur de l’ordre de 40 m. Ces herbiers constituent l'écosystème
majeur de Méditerranée et jouent un rôle important dans la protection
des côtes contre l'érosion. De nombreux organismes, animaux et
végétaux, trouvent protection et alimentation dans ces herbiers.
En Espagne, des études ont montré que la plante à fleurs aquatique
Posidonia Oceanica est très sensible aux variations du taux de salinité
de ses habitats naturels. Des effets notables sur sa vitalité ont été
observés dès que la salinité atteint 37,4 g de sel par kilogramme d’eau
de mer. D’après les sites http://fr.wikipedia.org et
http://www.larecherche.fr
Données :
Masses molaires atomiques : M(Cl) = 35,5 g.mol-1; M(Na) = 23,0 g.mol-1
- Valeur moyenne de la masse volumique de l’eau de la mer Méditerranée : r = 1027 kg.m-3
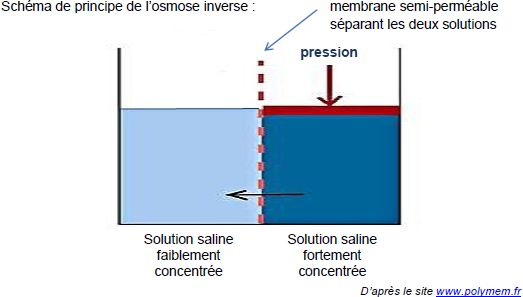
- Osmose inverse : Dans la nature, l’osmose est un phénomène naturel,
essentiel aux équilibres biologiques, qui consiste en la migration de
l’eau vers les solutions les plus concentrées. Cet écoulement s’arrête
naturellement lorsque le système a atteint l’équilibre. L’osmose
inverse est une technologie de séparation utilisée dans le procédé
industriel de dessalement de l’eau de mer. Lorsque l’on applique une
pression suffisante sur la solution la plus concentrée, le flux d’eau
est alors dirigé en sens inverse, c’est à dire de la solution la plus
concentrée vers la solution la moins concentrée.
|
|
|
1. On
appelle salinité la masse totale de sels dissous dans un kilogramme
d’eau de mer. Pour simplifier, on considèrera qu’il s’agit uniquement
de chlorure de sodium.
L’eau de mer de la Méditerranée a une salinité naturelle moyenne de 35,6 g.kg-1.
Déterminer, parmi les valeurs suivantes, celle qui est égale à la
concentration molaire moyenne en ions chlorure dans l’eau de mer.
0,609 mol.L-1 ; 0,687 mol.L-1 ; 0,625 mol.L-1 ; 0,592 mol.L-1.
M(NaCl) = 23+35,5 = 58,5 g/mol.
Masse de chlorure de sodium dans un litre d'eau de mer :
35,6*1,027 =36,56 g /L.
Quantité de matière en chlorure de sodium dans un litre d'eau de mer :
36,56 / 58,5 ~0,625 mol / L.
2. Expliquer en quoi la technique de dessalement de l’eau de mer par osmose inverse est génératrice de saumures.
Le
flux d’eau
est dirigé de la solution la plus
concentrée vers la solution la moins concentrée. On obtient une eau peu
salée ( à gauche de la membrane ) utilisée pour la consommation est une
saumure, solution fortement salée, rejetée en mer.
3.
On envisage de mélanger 1,0 L d’une saumure obtenue en fin de processus
de dessalement avec 200 L d’eau de mer avant de rejeter le mélange
obtenu en Méditerranée. Cette saumure est analysée par conductimétrie,
comme explicité ci-dessous.
Ce rejet présente-t-il un danger pour les écosystèmes marins ?.
|
|
|
|
Dosage des ions chlorure présents dans la saumure en fin du processus de dessalement
Équation de la réaction support du dosage :
Ag+aq +Cl-aq --> AgCl(s).
Protocole opératoire :
Diluer 500 fois la saumure pour obtenir une solution S.
Introduire un volume V1 = 10,00 mL de la solution S dans un bécher.
Mettre en place une sonde de conductimétrie dans le bécher en ajoutant de l’eau distillée de manière à immerger la sonde.
Remplir une burette graduée avec une solution de nitrate d’argent de concentration molaire C2 en ions Ag+ égale à 2,00 × 10-3 mol.L-1.
Verser progressivement la solution de nitrate d’argent dans le bécher
et relever les valeurs de la conductivité du milieu réactionnel après
chaque ajout.
Évolution de la conductivité s du milieu réactionnel en fonction du volume V2 de la solution de nitrate d’argent ajoutée, dans le cas de la saumure obtenue en fin du processus de dessalement :
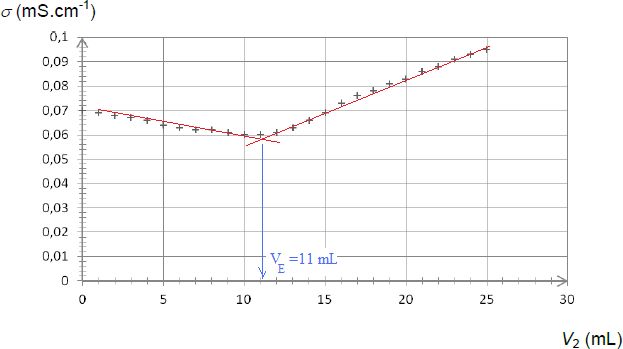
Quantité de matière d'ion chlorure dans la prise : C2VE = 2,00 10-3 *11 =2,2 10-2 mmol dans V1 = 10 mL de solution S.
Concentration en ion chlorure dans la solution S : 2,2 10-2 / 10 =2,2 10-3 mol/L.
Tenir compte de la dilution : [Cl-]saumure = 500 *2,2 10-3 = 1,1 mol/L.
Masse de chlorure de sodium dans un litre de saumure : 1,1 *58,5 = 64,35 g / L.
Masse de chlorure de sodium contenue dans 200 L d'eau de mer : 36,56 *200 = 7,312 103 g.
Masse de chlorure de sodium dans 201 L de rejet : 7,376 103 g.
Concentration en NaCl de cette solution : 7,376 103 / 201 = 36,7 g / L.
ou 36,7 / 1,027 ~35,7 g / kg.
Des effets notables sur sa vitalité ont été
observés dès que la salinité atteint 37,4 g de sel par kilogramme d’eau
de mer.
Ce rejet ne présente pas de danger pour les écosystèmes marins.
|
|