QCM
: acide, alcool, composťs organiques, dissolution, pile.
Concours kinť St Michel 2015
En poursuivant votre navigation sur ce site, vous acceptez l’utilisation de Cookies vous proposant des publicitťs adaptťes ŗ vos centres d’intťrÍts.
|
|
.
|
|
|
|
|
|
|
1. Solutions acides et pH.
( 1 pt).
On considŤre les trois solutions suivantes, de mÍme volume V = 20,0
mL,ŗ 25įC.
La solution 1 est une solution d'acide chlorhydrique de pH1
= 3,0.
La solution 2 est une solution d'acide sulfurique de concentration c2
=0,5 10-2 mol/L.
La solution 3 est une solution d'hydroxyde de sodium de concentration c3
=0,5 10-2 mol/L.
- Pour la solution
2, pH2 = 2,3.
Faux.
L'acide sulfurique est un
diacide fort ; pH2 = -log (2c2)=-log
10-2 = 2.
-
L'ajout de 20 mL d'eau ŗ la solution 1, conduit ŗ une augmentation de
pH de 0,3 unitť. Vrai.
pH'1
= -log (Ĺc1) =log 2 -log c1
=0,3 +pH1.
-
Le pH de la solution 3 est gal ŗ 11,7.
Vrai.
pH3
= 14 + log c3 = 14 + log(0,5 10-2)=11,7.
-
La
solution 3 provient d'une solution obtenue par dissolution d'une mase m
= 1,0 g de soude dans 500 mL d'eau.
Faux.
n = m / M(NaOH) = 1,0 / 40 =
0,025 mol ; c = n /V = 0,025 / 0,50 =0,050 mol / L.
2. Alcools.
(0,5 pt)
On considŤre les molťcules organiques suivantes :
1. 2-mťthylbutan-2-ol ; 2. 2,2-dimťthylpropan-1-ol ; 
- La molťcule 1 est
un alcool secondaire.
Faux.
Alcool
tertiaire.
-
La molťcule 2 est plus soluble dans l'eau que la molťcule 3.
Vrai.
La molťcule
3 possŤde une plus grande chaÓne carbonťe hydrophobe. La solubilitť est d'autant plus grande que la chaÓne carbonťe est plus courte et qu'il y a des ramifications.
-
La cohťsion des alcools ŗ l'ťtat liquide est essentiellement
due ŗ l'existence de liaisons hydrogŤne.
Vrai.
-
Le classement des tempťratures d'ťbullition des alcools ci-dessus est 2
< 1 < 3 < 4.
Faux.
La tempťrature d'ťbullition croÓt avec le nombre de carbone et ŗ nombre de carbone ťgal, diminue si la chaÓne est ramifiťe. 1 < 3 < 2 < 4.
3.
Composťs
organiques. 0,5 pt.
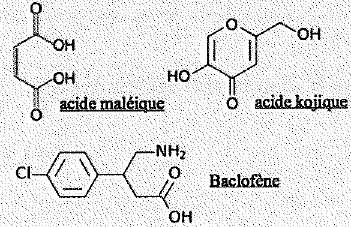
- Ces trois molťcules comportent un groupe carboxyle. Faux.
L'acide
kojique ne comporte pas de groupe -COOH.
- Une seule de ces molťcules est chirale. Vrai. ( le baclofŤne)
- Une de ces molťcule prťsente l'isomťrie Z / E. Vrai. ( l'acide malťÔque )
- La rťaction entre l'acide malťÔque et l'acide kojique peut conduire ŗ
la formation d'un ester.
Vrai.
|
| .
. |
|
|
4.
Nomenclature.
(0,5 pt)
- Le mťthanoate de propyle et le propanoate de mťthyle sont des
isomŤres.
Vrai.
H-COO-CH2-CH2-CH3
et CH3-CH2-COO-CH3.
- L'acide
2-amino-3-hydroxypropanoÔque a pour formule brute C3H7NO3.
Vrai.
HOCH2-CH
NH2-COOH.
- 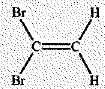 . Cette
molťcule porte le nom de (Z)-1,1-dichloroťthŤne. Faux. . Cette
molťcule porte le nom de (Z)-1,1-dichloroťthŤne. Faux.
1,1-dibromoťthŤne.
- 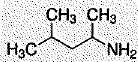 Cette molťcule porte le nom de
1,3-dimťthylbutylamine. Faux. Cette molťcule porte le nom de
1,3-dimťthylbutylamine. Faux.
2-amino-4-mťthylpentane.
|
.
|
|
5. RMN et IR. 0,5 pt
.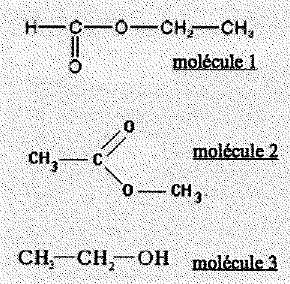
- La spectroscopie IR permet de distinguer les molťcules 1 et 2. Faux.
- La
spectroscopie IR permet de distinguer les molťcules 2 et 3. Vrai.
- Le spectre RMN de la molťcule 2 comprend 2 singulets intťgrant le
mÍme nombre de protons. Vrai.
- Les spectres RMN des molťcules 1 et 3 prťsentent un singulet, un
triplet et un quadruplet et sont donc identiques. Faux.
6. Dissolution (1 pt).
Le sel de Mohr est un solide de formule FeSO4,
(NH4)2SO4,
6H2O. On dissout du sel de Mohr dans 500 mL
d'eau afin d'obtenir une solution dont la concentration en sel de Mohr
est c = 2,0 10-2 mol/L. M( se de Mohr) 391,8
g/mol.
Les ions fer rťagissent avec les ions hydroxyde pour former un
prťcipitť d'hydroxyde de fer.
- Le sel de Mohr
est su solide molťculaire neutre.
Faux.
C'est un
solide ionique.
- Pour prťparer
cette solution, il faut peser une masse m = 3,9 g de sel de
Mohr. Vrai.
n = c V = 0,020 *0,50 =0,010 mol
; m = nM = 0,010 *391,8 = 3,9 g.
- Le prťcipitť d'hydroxyde de fer obtenu par ajout de quelques gouttes
d'hydroxyde de sodium ŗ un prťlevement de la solution a pour formule
Fe(OH)2 (s). Vrai.
- Dans la
solution, la relation entre les concentrations molaires des ions NH4+
et SO42- vťrifient [SO42-]=[NH4+]=Ĺc. Faux.
[SO42-] = 2 c ; [NH4+] = 2c .
7.
Pile.
0,5 pt.
Une pile est formťe ŗ partir des couples Cu2+/Cu
et Al3+/Al. les mťtaux sont en excŤs.les
solutions contenant les ions cuivre (II) et aluminium(III) ont la mÍme
concentration. Le pont salin est constituť d'une solution saturťe de
nitrate de potassium. Le courant circule de l'ťlectrode de cuivre vers
l'aluminium ŗ l'extťrieur du circuit.
- A la borne nťgative : Al(s) ---> Al3+aq
+ 3e-. Vrai.
- Le pont salin
ferme le circuit ťlectrique et assure le passage des ťlectrons. Faux.
Les
ťlectrons se dťplacent dans les mťtaux, pas dans les ťlectrolytes.
- La cathode est constituťe par le cuivre. Vrai.
- L'ťquation de
fonctionnement de la pile est 3Cu(s) + 2Al3+aq
---> 3 Cu2+aq + 2Al(s). Faux.
3
Cu2+aq + 2Al(s)--->3Cu(s) + 2Al3+aq.
|
|
|