QCM Chimie.
Concours kinť Ader.. 2015
En poursuivant votre navigation sur ce site, vous acceptez l’utilisation de Cookies vous proposant des publicitťs adaptťes ŗ vos centres d’intťrÍts.
|
|
.
|
|
|
|
|
|
|
Le sujet
de ce concours n'est pas accessible depuis ce site.
61. Fermentation malolactique du jus de raisin. Rťponses C, D.
Acide malique ---> CO2 + acide lactique.
Concentration molaire initiale en acide malique : m / M(acide malique) =5,2 / 130 ~0,04 mol/L.
Avancement final xf = 5,2 g/L ; avacement au temps de demi-rťaction 5,2 / 2 = 2,6 g/L.
Temps de demi-rťaction : tĹ = 15 jours.
62. Effet batochrome. Rťponses B, E.
La
longueur d'onde du maximum d'absorption est dťplacť vers les grandes
longueurs d'onde lorsque le nombre de liaisons conjuguťes croÔt. La molťcule de couleur jaune possŤde le systŤme conjuguť le plus ťtendu.
63. Acide formique. Rťponses A, D.
HCOOH aq + H2O(l) = HCOO-aq + H3O+aq. Rťaction partielle.
Avancement final =[H3O+aq] V =10-pH V =10-4 *0,05 =5 10-6 mol = 5 10-3 mmol.
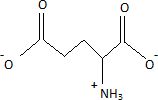
64. Forme prťdominante d'un acide aminť ŗ pH = 7. Rťponse E.
A pH > pKa2, les formes -COO- prťdominent ; ŗ pH <pKa3, la forme NH3+ prťdomine.
65. Dťcomposition d'une eau oxygťnťe. Rťponse C.
H2O2 ---> H2O + ĹO2.
Quantitť de matiŤre initiale d'eau oxygťnťe : n0=C V = 0,10 *20,0 = 2,0 mmol.
Quantitť de matiŤre finale de dioxygŤne : 0,5 n0 = 1,0 mmol.
Volume final de dioxygŤne : 0,5 n0 Vm =1,0 *24 =24 mL.
66. Combustion complŤte du gazole de formule C12H26. Rťponse D.
C12H26 + 18,5 O2 ---> 12 CO2 + 13 H2O.
Quantitť de matiŤre de gazole :V rgazole / M(gazole)=10*0,68 / 0,170 =40 moles.
Quantitť de matiŤre de dioxyde de carbone : 12*40 = 480 moles.
Masse de dioxyde de carbone : 480*44 ~2,1 104 g ~21 kg.
|
|
|
67. SynthŤse du MTBE. Rťponses B, D.
Chlorure de mťthyle + (CH3)3CO- ---> MTBE + Cl-. (Substitution)
Mťthanol + mťthylpropŤne ---> MTBE ( addition).
68. Chiralitť. Rťponse C.
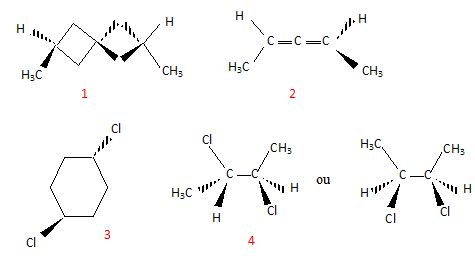
Le spirane (1) et l'allŤne (2) sont chiraux.
(3) ne possŤde pas de carbone asymťtrique : molťcule non chirale.
(4) possŤde 2 carbones asymťtriques identiques ; la molťcule possŤdant un plan de symťtrie n'est pas chirale.
|
.
|
|
69. Titrage conductimťtrique des ions chlorure. Rťponse
D.
Ag+aq +Cl-aq = AgCl(s).
Les quantitťs de matiŤre d'ion argent et d'ion chlorure sont ťgales ŗ l'ťquivalence : n =VE C2 =12*5,0 10-3 =6,0 10-2 mmol.
Concentration des ions chlorure dans la solution mŤre diluťe 5 fois : C1 = n / V1 = 6,0 10-2 / 10,0 =6,0 10-3 mol / L.
Concentration des ions chlorure dans le lait : C = 5 C1 =3,0 10-2 mol / L.
Titre massique en ion chlorure : C M(Cl-) = 3,0 10-2 *35,5 =1,065 ~1,1 g/L.
70. Inertitude d'un titrage. Rťponses C, E.
DV1/V1 =0,1 / 50,0 =2,0 10-3 ; DV2/V2 =0,05 / 25,00 =2,0 10-3 ; DVE/VE =0,08 / 10,00 =8,0 10-3 ; DC/C =0,2 / 50,0 =4,0 10-3 ;
A l'ťquivalence : C VE = 50,0 * 10,0 10-3= 0,50 mmol.
Quantitť de matiŤre d'ibuprofŤne dans un comprimť : 2 * 0,50 = 1,0 mmol.
Masse d'ibuprofŤne dans un comprimť : 1,0 *M(ibuprofŤne) = 1,0 *206 = 206 mg.
m = (206 Ī2) mg alors que la notice annonce 200 mg.
|
|
|