Dosage du glucose
libre dans un jus de fruit :
concours Atpl2 Nice 2014
En poursuivant votre navigation sur ce site, vous acceptez l’utilisation de Cookies vous proposant des publicités adaptées à vos centres d’intérêts.
|
|
.
.
|
|
|
|
|
|
|
Mélange initial.
On prélève 2,0 mL d’une solution de jus de fruit que l’on verse dans
une fiole jaugée de 50 mL. On y
ajoute 20,0 mL d’une solution colorée de diiode, de concentration [I2(aq)]
= 2,0.10–2 mol.L–1. On
complète
au trait de jauge par une solution d’hydroxyde de sodium afin de
maintenir un excès d’ions hydroxyde
dans le milieu réactionnel.
Quelle est la quantité de matière nD de diiode
initialement introduit ? On note nG la quantité
de glucose
initialement présente.
nD = 0,0200*2,0 10-2 = 4,0 10-4 mol.
Réaction
entre le glucose et le diiode.
Le glucose G (que l’on notera RCOH) réagit avec le diiode. Il se forme
des ions iodure I– (aq) et le glucose
se transforme en ion gluconate (qui sera noté RCOO–
(aq)). Dans le mélange étudié, on supposera que
seul le diiode est coloré. Il se produit la réaction totale :
I2 + 3HO- + RCOH = RCOO-
+ 2H2O
+ 2I-.
couple oxydant réducteur : I2 / I-
et RCOO- / RCOH
Au bout d’une demi-heure l’aspect de la solution n’évolue plus,
celle-ci restant partiellement colorée.
Quel est le réactif limitant ?
La solution
restant colorée, elle contient encore du diiode : le réactif limitant
est donc le glucose.
Compléter
le tableau suivant, descriptif de la réaction ; x correspond à
l’avancement de la réaction.
|
avancement (mol)
|
I2
|
+ 3HO-
|
+
RCOH
|
=
RCOO-
|
+ 2H2O
|
+ 2I-.
|
|
initial
|
0
|
nD= 4 10-4
mol
|
excès
|
nG
|
0
|
excès
( solvant)
|
0
|
|
en cours
|
x
|
4 10-4-x
|
nG -x
|
x
|
2x
|
|
fin
|
xmax
|
4 10-4-xmax
|
nG -xmax
=0
|
xmax
|
2xmax
|
En déduire que la quantité de glucose nG
introduite dans la solution peut s’écrire:
nG = nD – nR
où nR représente la quantité de diiode n’ayant
pas réagi.
donc nG = xmax
et nR= 4 10-4-nG
= n0-nG
nG= nD- nR= 4 10-4-nR.
Dosage du diiode en excès.
On souhaite déterminer la quantité de diiode nR
n’ayant pas réagi.
Pour cela on prépare 5 solutions de diiode de concentrations
différentes et on mesure l’absorbance A de chacune à l’aide d’un
spectrophotomètre.
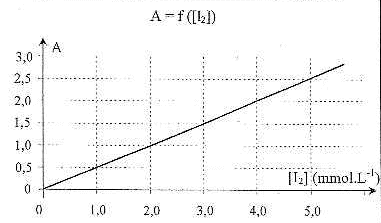
Les valeurs obtenues permettent de tracer la courbe A = f([I2])
proposée ci-dessous .
|
| .
. |
|
|
L’absorbance du
mélange étudié vaut 1,5.
En utilisant la courbe A = f([I2])
, déterminer la valeur de la concentration en diiode restant dans la
solution. En déduire la quantité de matière de diiode restant nR
(on rappelle que cette solution
était préparée dans une fiole jaugée de 50 mL).
La courbe est une droite passant par l'origine :
l'absorbance et la concentration en diiode sont proportionnelles. Le coefficient
directeur de la droite est proche de : 2,5 / 5
10-3 = 500 L/mol.
Concentration
en
diiode restant en solution : 1,5 / 500 = 3 10-3
mol/L.
La
quantité de
matière de diiode restant nR
= volume fiole jaugée (L) *
concentration (mol/L)
nR
=
0,05*3 10-3
= 1,5 10-4 mol.
En utilisant la relation établie ci-dessus en déduire la quantité de
glucose nG introduite initialement ?
nG= nD- nR= 4 10-4-nR = (4-1,5) 10-4 = 2,5 10-4 mol.
Calculer la quantité de glucose n’G et la masse mG
de glucose présentes dans un litre de jus de fruits et
estimer le nombre de morceaux de sucre que cette quantité de glucose
représente.
Donnée : masse molaire moléculaire du glucose : MG = 180 g/mol.
2,5 10-4 mol dans 2 mL de jus soit 2,5 10-4 *500 = 0,125 mol /L.
mG = 0,125*180 =22,5 g soit environ 4 morceaux
de sucre.
|
.
|
|
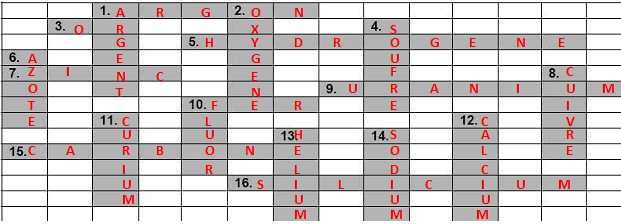
Mots
croisés. Compléter les parties grisées dans la grille
suivante à partir des définitions données ci-dessous :
Horizontal 1 : gaz rare
Vertical 1 : le nitrate de cet élément est 1 produit photosensible très
connu
Vertical 2 : élément dont le rôle fût démontré par Lavoisier
Horizontal 3 : Au
Vertical 4 : élément se dégageant des volcans
Horizontal 5 : un des éléments constitutifs de l’eau
Vertical 6 : élément le plus abondant de l’air
Horizontal 7 : élément à la base de la fabrication des premières piles
électriques
Vertical 8 : élément constitutif du laiton et des petites pièces de
monnaie
Horizontal 9 : dernier élément naturel
Horizontal 10 : Elément 26 dans le tableau périodique
Vertical 10 : élément présent dans les pâtes dentifrices
Vertical 11: Doit son nom à une célèbre scientifique française
Vertical 12: Elément essentiel pour la constitution des os
Vertical 13: On le trouve dans certains ballons
Vertical 14: Elément constitutif essentiel du sel marin
Horizontal 15: L'élément chimique à la base de la vie
Horizontal 16: Elément nécessaire pour la fabrication des panneaux
photovoltaïques.
|
|
|
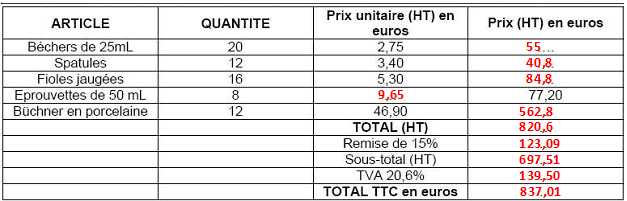
Comptabilité.
Le
laborantin a besoin de faire une commande de petit matériel pour
réapprovisionner ses stocks. Pour cela il a créé un tableau. Compléter
son tableau de commande :
|
|
|