Chimie organique.
Concours Assistant d'ingénieur Maine
Itrf 2014
En poursuivant votre navigation sur ce site, vous acceptez l’utilisation de Cookies vous proposant des publicités adaptées à vos centres d’intérêts.
|
|
.
.
|
|
|
|
|
|
|
Culture générale.
Une molécule de masse molaire 100 est composée de 60% de carbone, 8%
d'hydrogène et 32% d'oxygène. Combien cette molécule comporte-t-elle de
cycles ou d'insaturations, donner une formule développée possible.
CxHyOz avec x, y et z entiers.
12x /60 = M/100 = 1 soit x = 5 ; y/8 = M/100 = 1 soit y = 8 ; 16 z/32 = 1 soit z = 2.
C5H8O2 : nombre d'insaturation½(5*2+2-8) = 2.
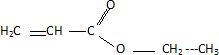
Qu'obtient-on par déshydratation du 2-methylbutan-2-ol en milieu acide ? Ecrire le mécanisme et les formules des produits
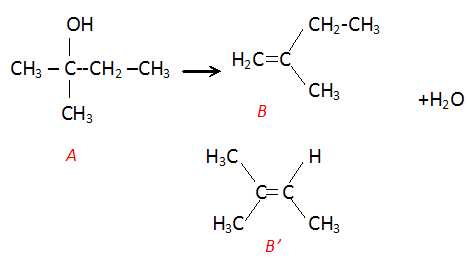
B : 2-méthylbut-1-ène ; B' : 2-méthyl but-2-ène.
Ce sont des isomères qui différent seulement par la position de la double liaison dans la chaine carbonée.
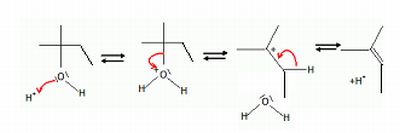
Il y a formation préférentielle de l'alcène le plus substitué ( règle de Zaïtzev).
Que se passe-t-il si l'acide utilisé est trop concentré ?
Le carbocation tertiaire stable peut être attaqué par un nucléophile est conduire à un etheroxyde.
Indiquez deux méthodes de préparation des acides carboxyliques.
Hydrolyse d'un ester; oxydation des alcools primaires, action d'un magnésien sur le dioxyde de carbone.
Ecrire l'équation de la fermentation alcoolique du glucose en milieu anoxique (sans oxygène).
C6H12O6 ---> 2C2H6O + 2CO2(g).
Un vin titre 12 % vol. Quelle est sa concentration en éthanol en mol.L-1 ?
Données : masse volumique de l'éthanol µ= 0,785 g.cm-3,
12 mL d'éthanol soit 12*0,785 =9,42 g dans un litre de vin.
M(éthanol) = 46 g/mol ; C = 9,42 / 46 = 0,205 mol/L.
Quelle masse de glucose doit fermenter pour produire un litre de ce
vin, si on admet que le rendement de la réaction est de 80 % ?
Quantité de matière de glucose : n = 0,205 / 2 = 0,1024 mol
M(glucose) =180 g/mol ; masse de glucose : 180*0,1024 = 18,432 g
Tenir compte du rendement : 18,432 / 0,80 ~23 g.
|
| .
. |
|
|
Le
(3R, 4S)-3-bromo-4-méthylhexane traité par KOH alcoolique concentrée à
chaud conduit à trois composés A, B et C selon un processus élémentaire
B et C sont des isomères de configuration et A est un isomère de
constitution de B et C. Choisissez parmi les propositions suivantes celles qui sont exactes.
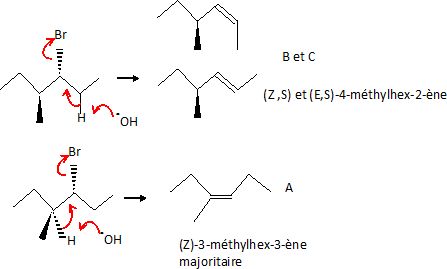
a) A est actif sur la lumière polarisée. Faux
b) le mélange (B + C) est un mélange d’isomères Z et E. Vrai
c) le mélange (B + C) est un mélange d’isomères R et S. Faux.
d) A a une stéréochimie Z. Vrai.
e) A est le produit majoritaire. Vrai.
f) la réaction est une élimination de type E1. Faux.
g) la réaction est une élimination de type E2. Vrai.
h) la réaction est régiosélective. Vrai.
i) le processus qui conduit au produit A est stéréospécifique car le mécanisme réactionnel fait intervenir un carbocation. Faux.
j)
le processus qui conduit au produit A est stéréospécifique car les
atomes d’hydrogène et de brome qui sont éliminés, sont chacun portés
par un carbone asymétrique de configuration absolue fixée. Vrai.
Quelle règle permet de prédire lequel des produits sera majoritaire ?
Il y a formation préférentielle de l'alcène le plus substitué ( règle de Zaïtzev).
|
.
|
|
Etude d'une réaction en pratique.
Ecrire l'équation de la réaction entre l'éthanol et l'acide propanoïque.
C2H5OH + CH3COOH = CH3-COO-C2H5 + H2O.
A quelle classe de composé est associé le produit obtenu. Ester.
Le montage expérimental utilisé pour cette synthèse est schématisé ci-dessous. Nommer les éléments constitutifs du dispositif.
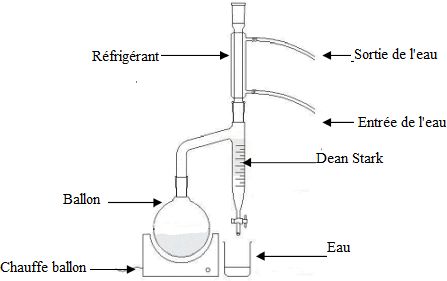
Le cyclohexane est le solvant le plus couramment utilisé dans cette réaction. Quel est le rôle du dispositif ?
Pour augmenter le
rendement de la synthèse, on élimine l'eau en phase vapeur en utilisant
un solvant organique et le montage de Dean-Stark.
Le diagramme binaire simplifié de l'équilibre liquide -vapeur pour le système eau-cyclohexane est donné ci-dessous :
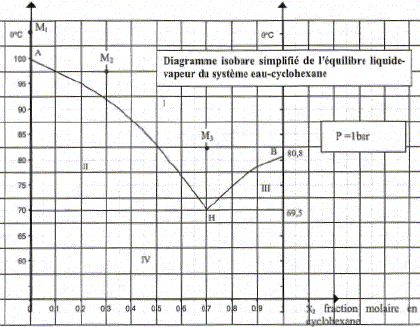
Comment nomme-t-on les branches HA et HB de ce diagramme ? Courbe de rosée.
Comme nomme-t-on le point H ? Hétéroazéotrope.
|
|
Compréhension d’un protocole en anglais
Friedel-Crafts Acylation of Toluen
Objective: The purpose of this experiment is to perform Elecrtophilic
Aromatic Substitution reaction (Friedel-Crafts acylation) of toluene.
Electrophilic aromatic substitution reactions take place between the
nucleophilic of an aromatic ring and an enhanced electrophile. The
intermediate carbocation rapidly goes through elimination of proton to
restore the aromatic system. In the case of Friedel-Crafts acylation,
the electrophile is an acylium ion, formed by the reaction of an acyl
chloride with aluminum chloride.
Chemicals:
toluene, anhydrous aluminum chloride, acetyl chloride, methylene chloride, conc. HCl, 5%, brine anhydrous MgSO4 or Na2SO4
Caution:
Anhydrous aluminum chloride is moisture sensitive and will irritate
your skin producing HCl. Wear gloves and handle this chemical
carefully. Close the bottle as soon as you obtain the amount needed.
Acetyl chloride is an eye and lung irritant: do not remove from the
hood and close tightly after measuring the amount needed.
Wash the glassware after this experiment in the hood with some acetone before moving it to your bench top.
De quel type de réaction s’agit-il ?
Acylation de Friedel et Crafts, substitution électrophile sur le noyau benzénique.
Ecrire le mécanisme réactionnel tel que décrit dans le protocole.
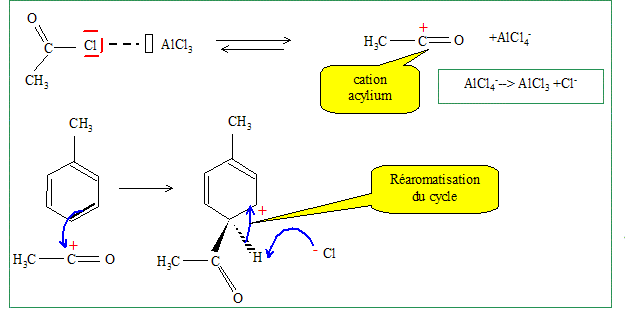
Quelles précautions devrez-vous prendre lors de cette synthèse ?
Le chlorure d'aluminium est sensible à l'humidité et peut irriter la peau. ( Port de gants).
Le chlorure d'acéthyle irrite les yeux et les poumons. Travailler sous hotte.
|
|
|