Composés
ß-dicarbonylés.
Concours agrégation 2004
En poursuivant votre navigation sur ce site, vous acceptez l’utilisation de Cookies vous proposant des publicités adaptées à vos centres d’intérêts.
|
|
.
.
|
|
|
|
|
|
|
Les
composés ayant un groupement CH2 voisin de deux
carbonyles C=O ont un comportement particulier. La forme énol est
présente dans des proportions importantes et l’'acidité de ces composés
est remarquable.
Le spectre RMN de l’acétylacétone H3C-CO-CH2-CO-CH3,
en solution dans CCl4, est donné ci-dessous
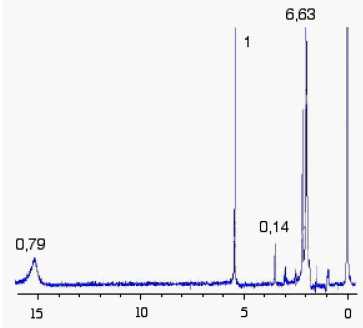
L'’indication
portée à côté de chaque pic représente sa surface, déterminée
expérimentalement par intégration,vle pic à d = 5,5 étant pris
pour référence.
Quel
nom donne-t-on à l’abscisse d du
spectre ? À quoi correspond le pic situé à d = 0 ?
Rappeler la définition de la grandeur d.
L'abscisse d
est le déplacement chimique. d=0
correspond au tétraméthylsilane (TMS), composé choisi comme origine des
déplacements chimiques, compte tenu d'un fort blindage de ces protons. d = (n-nTMS)
/ n0
106.
Quel est
l’intérêt de la mesure de la surface de chacun des pics (ou groupe de
pics) ?
La surface d'un pic
étant proportionnelle au nombre de protons résonnant, elle permet de
connaître le nombre de protons équivalents ayant le même déplacement
chimique.
Ce spectre fait
apparaître la présence des deux formes énol et cétone.
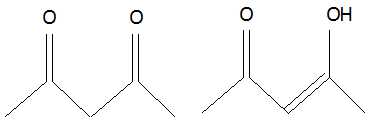
Écrire
la formule semi-développée de la forme énol de l’acétylacétone.
Attribuer les différents pics à chacune des deux formes.
|
| .
. |
|
|
Pic
vers 2 pm : 6 protons équivalents des groupes méthyles de la forme
cétone et 3 protons équivalent CH3 de la forme
énol.
Pic singulet à 3,5 ppm : deux protons équivalents CH2
situé entre les carbonyles de la forme cétone.
Pic singulet à 5,5 ppm : proton porté par le double liaison C=C de la
forme énol.
Pic singulet à 15 ppm : proton énolique.
En
prenant, le cas échéant, une valeur moyenne pour les pics concernant la
même forme, évaluer le pourcentage de chacune des deux formes.
Interpréter la grande stabilité de la forme énol.
Le pic à 15 ppm ainsi que celui à 5,5 ppm correspondent à un proton.
Surface moyenne correspondant à un proton : (0,79 + 1) / 2
=0,895.
Le pic à 3,5 ppm correspond à 2 protons de l'acétylacétone.
On note x la proportion de forme cétone : 0,14 =0,895*2x
; x = 7,8 10-2 ( ~ 8 %) et ~92 % de forme énol.
La forme énol est stabilisée du fait des deux doubles liaisons
conjuguées ainsi que par la formation d'une liaison intramoléculaire. 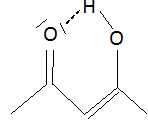
|
.
|
|
Le pKa
attribué à l’acétylacétone est de 9. Interpréter
l’acidité assez forte de ce composé.
La base conjuguée est stabilisée par résonance.
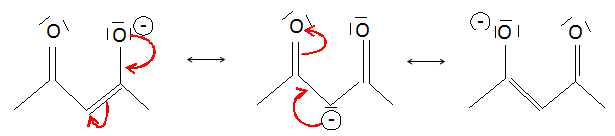
La base conjuguée de l’acétylacétone est un ligand bidentate. Justifier
cette propriété.
Les deux oxygène de la base conjuguée portent tous deux une charge
négative. Ils peuvent donc établir deux liaisons avec un cation
métallique.
|
|
|



