Maison
container : étude acoustique; protection contre la corrosion.
Bts bâtiment 2015.
En poursuivant votre navigation sur ce site, vous acceptez l’utilisation de Cookies vous proposant des publicités adaptées à vos centres d’intérêts.
|
|
.
.
|
|
|
|
|
|
|
|
I.
Isolement brut Db du
local.
On
mesure les niveaux de pression acoustique des bruits extérieurs Lex et
les niveaux de pression acoustique Lin pour différentes bandes
d’octaves. On obtient le tableau suivant :
| Fréquence
médiane (Hz) |
125 |
250 |
500 |
1000 |
2000 |
4000 |
Niveau
d'émission
extérieure Lex (dB) |
75,8 |
73,0 |
77,5 |
74,3 |
70,2 |
68,4 |
Niveau
de réception
intérieur Lin (dB) |
45,6 |
42,3 |
41,3 |
44,2 |
39,8 |
37,1 |
1.
Donner le type d’appareil qui permet de mesurer les niveaux acoustiques.
Le sonomètre.
2.
Montrer que le niveau global de pression Lg peut
se calculer à partir de la relation
Lg = 20∙log (S 10Li/20)
où i = 1,2,3,…,6.
Les pressions acoustiques de chaque bande d'octave s'ajoutent :
Ptotal = S P où i = 1,2,3,…,6.
Ptotal
/ P0 = S P
/ P0 ; P / P0 = 10Li/20.
Ptotal
/ P0 = S 10Li/20.
Ltotal =
20 log( Itotal / I0
)=20
log S 10Li/20.
3. Montrer que le
niveau sonore global des bruits extérieurs vaut Lgex=
89,3 dB.
1075,8 /20 + 1073 /20
+ 1077,5
/20 + 1074,3 /20
+ 1070,2
/20 + 1068,4 /20 =6166 + 4467 +7499 +5188+3236+2630 = 29 176.
Lgex= 20
log 29176 = 89,3 dB.
4. Le niveau sonore
global des bruits à l’intérieur du logement est Lgin
= 57,8 dB.
Déterminer l’isolement brut Db.
89,3-57,8 = 31,5 dB.
II. Temps de réverbération dans
le local.
On donne les coefficients d’absorption ai des différents matériaux à
l’intérieur du local :
| Matériau
i |
Surface
Si (m2) |
Coefficient
ai |
Aire
équivalente Ai (m2) |
Parois
verticales
(liège) et plafond |
100 |
0,42 |
100*0,42=42 |
| Sol(
bois) et portes |
32,8 |
0,12 |
32,8*0,12~3,94 |
| Baie
vitrée et fenètre |
9,2 |
0,18 |
1,7 |
1. Compléter le
tableau.
Surfaces des murs recouverts de liège : 72 m2 ;
surface du plafond : 12,01*2,33 ~28 m2.
Surface recouverte de liège : 72+28 = 100 m2.
2.
Calculer l’aire d’absorption équivalente A du logement.
A = 42 +3,94 +1,7 ~47,6 m2.
3.
Définir la durée de réverbération acoustique dans un local Tr.
La durée de réverbération Tr est le temps mis par un son
pour décroître de 60 dB après la coupure de la source.
4. Montrer que Tr
= 0,28 s.
Tr = 0,16 V / A avec
V volume de la salle.
V = 12,01*2,33*3,0 = 83,9 m3.
Tr = 0,16* 83,9 /
47,6 =0,28 s.
5. Le temps de
réverbération du logement est-il le même pour un logement vide et pour
un logement meublé ? Justifier la réponse.
Le
temps de réverbération diffère si le logement est vide ou meublé. En
présence de meubles en bois, l'aire équivalente va augmenter alors que
le volume de la pièce reste inchangé. Tr diminue.
|
| .
. |
|
|
C.
Oxydoréduction et protection contre la corrosion
Le
container maritime est en acier (alliage de fer et de carbone) qui peut
être corrodé. Pour le protéger on choisit de relier le container à un
métal plus réducteur que lui : le zinc.
On donne les potentiels standards d’oxydoréduction :
E° (Fe2+/ Fe) = - 0,44 V; E° (Zn2+/
Zn) = - 0,76 V ; E° (O2 / H2O)
= + 1,23 V
I.
Problème de corrosion du container
1.
En utilisant les couples relatifs au fer et au dioxygène ci-dessus,
- expliquer pourquoi le fer est corrodé ;
Le
fer est le réducteur le plus fort et le dioxygène est l'oxydant le plus
fort. La réaction entre le fer et le dioxygène est spontanée.
- écrire les demi-réactions électroniques et la réaction globale
correspondant à la corrosion du fer (Fe) par le dioxygène (O2)
en milieu acide.
Fe(s) = Fe2+aq + 2e-.
½O2(g) +2e-+2H+
aq= H2O(l).
Fe(s) +½O2(g) +2H+
aq= Fe2+aq + H2O(l).
2.
Quel nom courant donne-t-on au mélange d’oxydes de fer formé par la
corrosion du fer ?
La rouille.
|
|
|
|
II. Protection du container contre la corrosion
Le container est protégé suivant le montage modélisé ci-dessous.
1.
Écrire la demi-réaction électronique qui se produit sur l’électrode de
zinc et celle qui se produit sur le container. Quel élément du
dispositif est oxydé ? Lequel est réduit ?
Oxydation du zinc, plus réducteur que le fer : Zn(s) = Zn2+aq +2e-.
Réduction des ions Fe2+ : Fe2+ aq + 2e- =Fe(s).
2.
Indiquer sur le schéma : le sens de circulation des électrons (e-), le
sens conventionnel du courant I, les pôles + et -, l’anode et la
cathode.
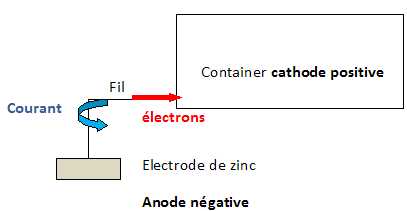
3. Quel nom donne-t-on à ce type de protection ? Pourquoi la qualifie-t-on ainsi ?
Protection par anode sacrificielle : le zinc s'oxyde ( disparaît ) à la place du fer qui est protégé.
4. Citer deux autres modes de protection des métaux contre la corrosion.
Couche de peinture ou de matière plastique ; galvanisation ; électro-zingage.
|
|
|
|