Edulcorant,
vitamine C, plongée sous-marine.
Bac St2s 2015
En poursuivant votre navigation sur ce site, vous acceptez l’utilisation de Cookies vous proposant des publicités adaptées à vos centres d’intérêts.
|
|
|
|
|
|
|
Consommation
d’édulcorants.
Le
néotame. Sur une bouteille de boisson light, on peut lire :
Boisson Light Agrum’ Zéro 33 cL
Eau gazéifiée, extraits naturels d'orange 10 mg, édulcorant : néotame
15 mg, conservateur : sorbate de potassium, amidon modifié, antioxydant
: acide ascorbique 8,1 mg,
arômes naturels d'agrumes (orange, pamplemousse, citron vert et
mandarine) avec autres arômes naturels, stabilisant E445, colorant E142.
Le néotame, de formule brute C20H30N2O5,
est listé comme édulcorant et exhausteur de goût. C’est un dipeptide 40
à 60 fois plus sucré que l’aspartame. Il ne se dégrade pas en
phénylalanine lors de la digestion, ce qui rend son ingestion possible
chez les personnes souffrant de phénylcétonurie (trouble héréditaire du
métabolisme ne permettant pas d’éliminer la phénylalanine dans le sang
dont l’accumulation cause des effets indésirables). On le trouve dans
les boissons non alcoolisées, les desserts, les confiseries, certaines
céréales pour petit déjeuner, …
La DJA du néotame a été fixée, par l’Agence Européenne de sécurité des
aliments, à 2,0 mg par kg de masse corporelle par jour.
Donner la signification des 3 lettres DJA. Donner la définition de la DJA.
La Dose Journalière Admissible
(DJA) est la dose maximale d’une
substance (exprimée en
mg par kg de
masse corporelle et par jour) à laquelle on peut être
exposé de façon répétée sans
risque pour
la santé.
Calculer la masse maximale de néotame qu’un adulte de 55 kg peut
consommer quotidiennement.
55*2,0 = 1,1 102 mg jour-1.
Calculer le nombre de bouteilles entières de boisson Light Agrum’ Zéro
33 cL qu’un adulte peut consommer en une journée, sans risque pour sa
santé.
110 / 15 =
7,3~ 7 bouteilles.
Le texte précise que le néotame est un dipeptide. Donner la définition
d’un dipeptide.
Un dipeptide
résulte de la condensation de deux acides aminés avec élimination d'une
molécule d'eau. Il se forme une liaison peptidique.
L’aspartame.
L’usage de l’aspartame compote quelques effets indésirables.
Lorsqu’une personne ingère de l’aspartame il se produit, dans
l’estomac, la réaction suivante :
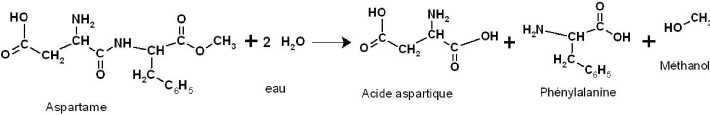
Nommer ce type de réaction. Hydrolyse.
Justifier que la phénylalanine appartient à la famille des acides a-aminés.
La
phénylalanine possède une fonction amine et une fonction acide
carboxylique portées par le même carbone.
Donner la représentation de Fischer de la D-Phénylalanine.
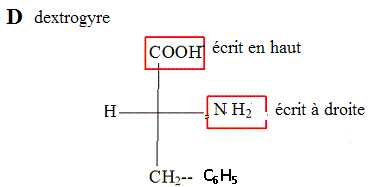
Expliquer pourquoi un individu souffrant de phénylcétonurie ne doit pas
consommer des produits contenant de l’aspartame.
Dans
l'estomac, l'aspartame s'hydrolyse et libère de la phénylalanine.
La
vitamine C contre le diabète de type 2.
Le diabète de type 2 est une maladie caractérisée par une hyperglycémie
qui engendre souvent des problèmes cardiovasculaires. Des études
récentes montrent que des patients diabétiques traités avec un apport
quotidien de vitamine C réduisent de manière significative leur taux de
glucose dans le sang, à jeun comme après les repas.
La vitamine C ou acide ascorbique est une vitamine hydrosoluble. C’est
une substance organique non calorique, essentielle à notre métabolisme
et non produite par notre organisme.
On s’intéresse, dans un premier temps, aux propriétés de l’acide
ascorbique.
Une recherche documentaire permet de trouver la fiche détaillée des
propriétés de cet acide.
Formule : C6H8O6
Etat : solide blanc. Densité
: 0,95 g cm-3 à 20 ° C
Formule de
la base conjuguée : C6H7O6
– (ion ascorbate)
Masse molaire : M = 176 g mol-1 . Solubilité :
333 g L-1 (dans l’eau à 20 °C)
pKa : 4,1 à 25°C. Se dissocie partiellement dans
l’eau.
DJA : 15 mg kg-1 Température de fusion : 191 °C
Utilisation : L’acide ascorbique évite l’oxydation du vin et dans
l'industrie agro-alimentaire empêche
la prolifération des bactéries (conservateur).
|
|
|
Dans cette
fiche on peut lire « évite l’oxydation du vin ». Donner la définition
d’un oxydant.
Un oxydant
est une espèce susceptible de gagner un ou plusieurs électrons.
L’oxydation ménagée de l’acide ascorbique donne de l’acide
déshydrocorbique selon la demi-équation : C6H8O6 = C6H6O6
+ 2 e- + 2 H+.
Indiquer si l’acide ascorbique est un oxydant ou un réducteur.
Justifier la réponse.
L'acide
ascorbique est un réducteur : il libère des électrons en s'oxydant.
Justifier le fait que l’acide ascorbique est un acide faible.
L'acide
ascorbique se dissocie partiellement dans l'eau.
Il est possible de déterminer la quantité d’acide ascorbique contenue
dans la boisson Light Agrum’ Zéro, à l’aide
d’un dosage pH-métrique.
Un étudiant trouve sur Internet un descriptif de cette manipulation qui
lui semble très incomplet. En voici le contenu.
On souhaite doser 50,0 mL de boisson Light. La
solution titrante est une solution d'hydroxyde de sodium (ou soude) de
concentration molaire CB = 1,0 . 10-3
mol.L-1. Verser peu à peu par ajouts successifs
la solution de soude dans la boisson Light et relever pour chaque ajout
la valeur du pH.
Pour réaliser ce dosage, une liste de matériel est proposée.
Burette graduée de 25,0 mL, potence et support de fixation.
Fiole jaugée de 50,0 mL. Pipette pasteur. Béchers de
150 mL. Eprouvette graduée de 50 mL.
Pipette graduée de 10,0 mL. Pipette jaugée de 10,0
mL. Propipette.
pH-mètre étalonné muni d’une sonde de pH. Agitateur magnétique
et barreau aimanté. Chauffe-ballon
Dans la liste proposée, choisir le matériel nécessaire pour réaliser le
prélèvement de la boisson dans laquelle on titre l’acide ascorbique.
Fiole jaugée de 50,0 mL.
Dans la liste
proposée, choisir le matériel nécessaire pour réaliser le dosage.
Burette graduée
de 25,0 mL, potence et support de fixation. Bécher de 150
mL.
pH-mètre
étalonné muni d’une sonde de pH. Agitateur magnétique et
barreau aimanté.
|
.
|
|
On note VB
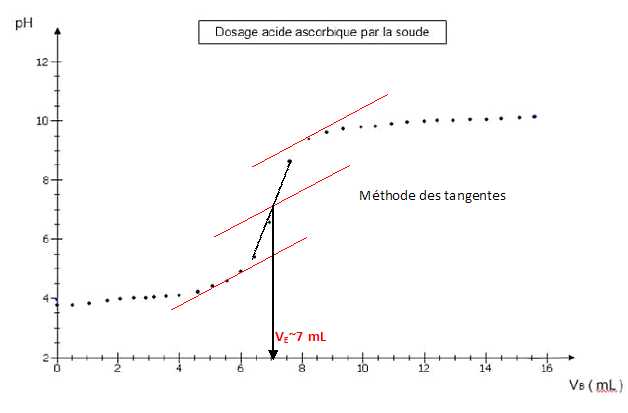
le volume de soude versé. En traçant pH = f (VB
) on obtient la courbe suivante.
Vérifier à l’aide du graphique, que le volume équivalent VE
est proche de 7,0 mL. Faire apparaître les traits de construction.
L’équation de la réaction chimique acido-basique mise en jeu
au cours de ce dosage est :
C6H8O6
+ HO– ---> C6H7O6
– + H2O
En utilisant la valeur du volume équivalent donnée, montrer que la
quantité de matière d’acide ascorbique dosée n est égale à 7,0 x 10-6
mol.
A
l'équivalence, les quantités de matière de soude et d'acide ascorbique
sont égales à : CBVE =1,0 10-3*7,0 10-3 = 7,0 10-6 mol.
En déduire que la bouteille de Light Agrum’ Zéro contient 4,6
x 10-5 mol d’acide ascorbique.
7,0 10-6 mol dans la prise de 50 mL soit
dans 33 cl (
330 mL) : 7,0 10-6 *330 / 50 =4,6 10-5
mol.
Calculer la
masse m d’acide ascorbique dans la bouteille de Light Agrum’ Zéro.
4,6 10-5
*176 =8,1 10-3 g = 8,1 mg, en accord
avec l'indication portée sur l'étiquette.
Plongée
sous-marine.
Les
ondes électromagnétiques en mer.
Le radar est un appareil qui envoie des micro-ondes par l’intermédiaire
d’une antenne. Lorsque ces ondes rencontrent un obstacle (rocher,
iceberg, navire, bouée...), elles "rebondissent" et reviennent vers
l'antenne donnant ainsi la distance entre le bateau et l'obstacle. Les
radars que l’on rencontre le plus souvent sur les bateaux fonctionnent
avec une longueur d'onde de 3,0 cm.
Il y a également les caméras thermiques qui permettent de naviguer la
nuit. Grâce à leur extrême sensibilité aux infrarouges, elles peuvent
distinguer clairement les autres navires.
Citons encore le phare, système de signalisation maritime constitué
d'une puissante lumière visible placée le plus souvent en haut d'une
tour. Il permet aux navires de repérer la position des zones
dangereuses se trouvant près des côtes ainsi que les ports maritimes.
Pour assurer sa sécurité en mer, il est bon de pouvoir communiquer pour
obtenir des informations météo ou demander du secours si besoin. La VHF
Marine permet de passer des communications vocales en utilisant des
ondes radio de hautes fréquences. Un canal, le 16, est réservé aux
appels d’urgence, d’autres canaux permettent de communiquer entre
embarcations ou avec les capitaineries et sémaphores.
Relever les 4 domaines d’ondes électromagnétiques mentionnés ci-dessus.
Micro-ondes,
infrarouges, lumière visible, ondes radio hautes fréquences.
Indiquer les trois domaines précédents qui n’y figurent pas. Repérer
par un astérisque la zone de la longueur d’onde utilisée par le
radar.
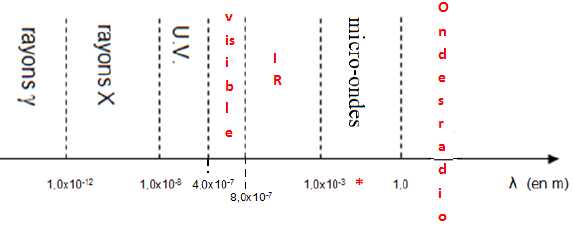
La relation entre la longueur d’onde et la fréquence n d’un
rayonnement s’écrit : l
= c / n.
Célérité de la lumière dans le vide : c = 3,0 108
m.s-1.
Calculer la fréquence de fonctionnement du radar considéré dans le
texte.
n = c / l = 3,0 108 /0,030 = 1,0 1010 Hz.
|
Plongée et pression.
Le responsable du groupe souhaite suivre le parcours ABCD :
Déterminer la pression PB, au point B. En
déduire la pression PC, au point C. Justifier la
réponse.
La pression
est la même en tous points d'un même plan horizontal : PB =PC = 1,5 bar.
La loi fondamentale de la statique des fluides permet d’écrire que la
différence de pression DP
entre les points A et D est telle que :
DP =
PD – PA = r
g h
r :
masse volumique de l’eau de mer
h : différence de profondeur entre les points A et D
g : intensité de pesanteur soit 9,80 N kg-1.
Rappeler la définition de la masse volumique d’un matériau
homogène. Donner
son unité dans le système international (S.I.).
La masse volumique, exprimée en
kg m-3, est la masse de l'unité de volume d'un
matériau homogène.
Montrer que la différence de pression DP =
PD – PA
est proche de 1,50 . 105 Pa.
DP = PD
– PA = 2,5 -1,0 = 1,5 bar =1,5 105 Pa.
Montrer que la valeur de la
masse volumique de l’eau salée est de 1,02 103
S.I.
r =DP /(g h) =1,50 105 /(9,80 *15,0)=1,02 103 kg m-3.
En prenant la masse volumique
de l’eau pure = 1,00 kg L-1, expliquer si le
résultat précédent est vraisemblable.
Le résultat
précédent est vraisemblable, car l'eau de mer contient du sel.
Les plongeurs évoluent à 10,0 m de profondeur où il règne une pression
de 2,00.105 Pa. Leur masque a une surface S =
200 cm2. On rappelle : la relation entre la
force pressante F exercée sur une surface S et une pression P : P =F /
S. On donne la correspondance : 1 cm2 = 10-4
m2.
Calculer la force pressante F, exercée par l’eau sur le masque, à la
profondeur de 10 m.
F = P S = 2,00.105 *200 10-4=4,0 103 N.
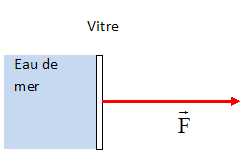
Représenter sur un schéma la
vitre du masque et la force pressante F exercée par l’eau sur cette
vitre. Echelle : 1 cm pour 1000 N.
|
|
|