Chimie et piscine.
Bac S
Antilles 2015
En poursuivant votre navigation sur ce site, vous acceptez l’utilisation de Cookies vous proposant des publicités adaptées à vos centres d’intérêts.
|
|
|
|
|
|
|
Influence du pH de l'eau de piscine
Les quantités de dichlore et des formes acide ou basique de l’acide
hypochloreux, en solution, sont fonction du pH de la solution. Ainsi, à
25°C, les proportions de ces espèces en fonction du pH sont données par
les courbes de la figure 1.
Le pH d’une eau de piscine doit être compris entre 7,2 et 7,6 pour le
confort de la baignade. Pour les deux bornes de cet intervalle de pH,
estimer les proportions de chacune des espèces chimiques. Ces
proportions correspondent-elles à une désinfection optimale ?

Entre pH = 7,2 et pH = 7,6 :
il n'y a pas de dichlore ; la proportion de HClO est comprise entre 72 et 47 % ; la proportion de ClO- est comprise entre 28 et 53 %. La désinfection est optimale.
Dosage des ions chlorure.
Pour que l’électrolyse soit efficace, l’eau de piscine doit contenir
entre 3 et 5 grammes de sel par litre. Pour s’assurer du bon
fonctionnement du système de désinfection de sa piscine, un chimiste
prélève un échantillon d’eau de piscine qu’il va analyser dans son
laboratoire. Il procède à un dosage conductimétrique des ions chlorure
présents dans l’eau de piscine par les ions argent.
L’équation de la réaction support du titrage est la suivante :
Ag+(aq) + Cl– (aq)---> AgCl(s).
Protocole du dosage :
- Remplir la burette graduée avec la solution aqueuse titrante de
nitrate d’argent de concentration en soluté apporté c = 0,050 mol.L-1.
- Dans un bécher de 200 mL, introduire précisément V=10,0 mL d’eau de piscine prélevée et ajouter 90 mL d’eau distillée.
- Placer, dans le bécher, la cellule conductimétrique reliée au conductimètre.
- Verser des volumes successifs de 2,0 mL de solution de nitrate d’argent dans le bécher en
maintenant en permanence une agitation. Relever après chaque addition la conductivité s de la
solution obtenue et rassembler les résultats dans un tableau.
Schématiser et légender le montage expérimental réalisé pour effectuer le dosage conductimétrique.
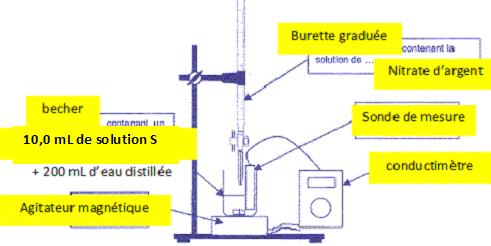 Quelles verreries doit-on utiliser pour introduire dans le bécher les 10,0 mL d’eau de piscine à
Quelles verreries doit-on utiliser pour introduire dans le bécher les 10,0 mL d’eau de piscine à
doser, puis les 90 mL d’eau distillée ? Justifier.
Un volume précis ( 10,0 mL) est mesuré à l'aide d'un pipette jaugée.
Un volume approximatif ( 90 mL) est mesuré à l'aide d'une éprouvette graduée.
|
| .
. |
|
|
Donner l’expression de la conductivité s du mélange avant l'équivalence, puis celle après
l'équivalence.
Avant l'équivalence les ions chlorure sont en excès, les ions argent sont en défaut.
s= lNa+ [Na+aq] + lCl-[Cl-aq] +lNO3-[NO3-aq].
Après l'équivalence les ions chlorure sont en défaut, les ions argent sont en excès.
s= lNa+ [Na+aq] + lAg+[Ag+aq] +lNO3-[NO3-aq].
Interpréter qualitativement les variations de la conductivité avant et après l’équivalence.
- la diminution de la conductivité avant l'équivalence.
L'ion
argent est en défaut avant l'équivalence ; du point de vue de la
conductivité, tout revient à remplacer l'ion chlorure par l'ion nitrate
de conductivité molaire ionique un peu plus faible.
La conductivité, et en conséquence la conductance de la solution diminue lentement.
- l'augmentation de la conductivité après l'équivalence.
L'ion
argent est en excès après l'équivalence. On ajoute des ions argent et
nitrate à la solution. La conductivité de la solution va croître assez
vite.
|
|
|
Donner l’allure de la courbe de titrage s = f(VAg+) représentant la conductivité σ du mélange en fonction du volume de solution de nitrate d’argent versé et justifier la position du point
d’équivalence sur cette courbe.
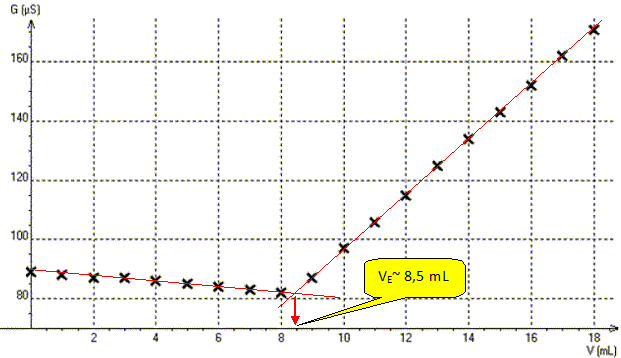
Le volume versé à l’équivalence est VE = 15,0 mL.
En explicitant votre démarche, déterminer la concentration molaire en ions chlorure de l’eau de piscine.
A l'équivalence : n(Cl-) = n(Ag+) ; V[Cl-]= C VE ; [Cl-]= C VE / V = 0,050 *15,0 / 10,0 = 0,075 mol/L.
Est-il nécessaire de rajouter du sel dans la piscine ? Justifier.
M(NaCl) = 58,5 g/mol.
Titre massique en sel : 58,5 *0,075 = 4,4 g/L.
Cette valeur étant comprise entre 3 et 5 g/L, il n'est pas nécessaire d'ajouter du sel dans la piscine.
|
|