Solubilité de
l'acide benzoďque, étude de l'ibuprofčne,
concours kiné Assas 2014
En poursuivant votre navigation sur ce site, vous acceptez l’utilisation de Cookies vous proposant des publicités adaptées ŕ vos centres d’intéręts.
|
.
.
|
|
|
|
|
|
|
|
Solubilité de
l'acide benzoďque.
A 20°C, l'acide benzoďque se présente ŕ l'état pur sous forme de
cristaux blancs, C6H5COOH (s). La dissolution de
ce solide dans l'eau est modélisée par l'équation chimique suivante :
C6H5COOH
(s) = C6H5COOH(aq).
Une solution saturée d'acide benzoďque est obtenue lorsque des cristaux
solides restent présents dans la solution de cet acide. A 20°C, on peut
dissoudre au maximum 2,93 g d'acide benzoďque pur par litre de solution.
l'acide benzoďque appartient au couple acide / base : C6H5COOH(aq)
/ C6H5COO-(aq)
Ecrire l'équation
chimique modélisant la réaction entre l'acide benzoďque et l'eau.
C6H5COOH(aq)
+H2O(l)= C6H5COO-(aq)+H3O+(aq).
Déterminer
la concentration molaire volumique en acide apporté dans un litre de
solution saturée d'acide benzoďque ŕ 20°C. En déduire la solubilité s
de cet acide.
M(acide benzoďque) = 7*12+6+32 =122 g/mol.
n = m / M = 2,93 / 122 =2,4016 10-2 ~2,40 10-2
mol dans un lite ; s = 2,40
10-2 mol/L.
On considčre une solution S d'acide benzoďque de volume V = 20,0 mL
Quelle serait la
valeur de l'avancement maximal de la réaction entre l'acide benzoďque
et l'eau ?
Dans
l'hypothčse oů la réaction entre l'acide benzoďque et l'eau est totale,
l'avancement maximale vaut :
xmax =s V = 2,40 10-2
*0,0200 = 4,80 10-4 mol.
Le pH de la solution est égal ŕ 2,90.
Construire le
tableau d'évolution de la réaction entre l'acide benzoďque et l'eau.
|
Avancement
(mol)
|
C6H5COOH(aq)
|
+H2O(l)
|
= C6H5COO-(aq)
|
+H3O+(aq)
|
initial
|
0
|
sV
|
solvant
|
0
|
0
|
en
cours
|
x
|
sV-x
|
x
|
x
|
ŕ
l'équilibre
|
xéq
= V 10-pH
|
sV-xéq |
xéq
|
xéq
|
Déterminer
l'avancement final puis le taux d'avancement final t de cette réaction.
xéq
=V 10-pH = 0,0200*10-2,90 = 2,52 10-5
mol.
t = xéq
/ xmax =2,52
10-5 /(4,80
10-4)=
5,25 10-2.
La
transformation étudiée est-elle totale ? Justifier.
t <1, la
transformation n'est pas totale.
On titre la solution S par de la soude ŕ 7,50 10-2 mol/L en
soluté apporté.
Calculer
le volume de solution titrante versé pour obtenir l'équivalence.
Véq = V s / Csoude = 20,0 *2,40 10-2 /
(7,50 10-2)=6,40 mL.
Quelle
est l'espčce du couple acide base prédominante dans le milieu
réactionnel, pour les volumes V de solution de soude versés figurants
dans le tableau suivant ?
Volume
de solution titrante versé
|
Espčce
prédominante du couple acide / base
|
V
= 1,5 mL
|
C6H5COOH(aq)
: pH < pKa.
|
V
= 3,2 mL = ˝Véq.
|
[C6H5COOH(aq)]
= [C6H5COO-(aq)] : pH = pKa. |
V
= 6,4 mL
|
C6H5COO-(aq) : pH > pKa. |
|
|
|
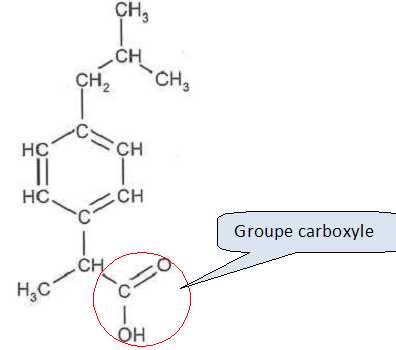
Etude de l'ibuprofčne.
M = 206 g/mol.
Entourer le groupe caractéristique associé ŕ la fonction acide carboxylique. Nommer ce groupe.
Cette molécule est-elle chirale ? Justifier.
Cette
molécule possčde un atome de carbone asymétrique, c'est ŕ dire un atome
de carbone tétragonal lié ŕ 4 atomes ou groupes d'atomes différents.
Une molécule possédant un atome de carbone asymétrique est chirale.
Comment appelle-t-on les configurations suivantes de l'ibuprofčne ? Justifier.
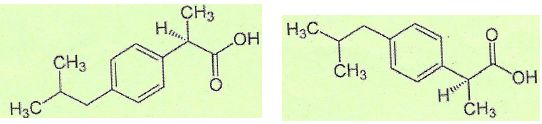
Une
molécule chirale n'est pas superposable ŕ son image dans un miroir. La
molécule et son image dans un miroir constitue un couple d'énantiomčres. Deux énantiomčres sont 2 isomčres de configuration, images l'un de l'autre dans un miroir.
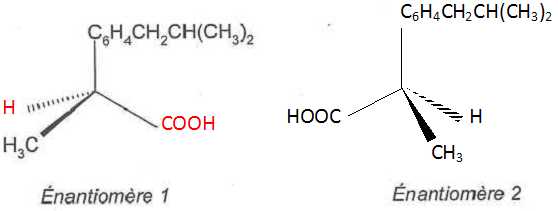
|
.
On
souhaite déterminer la teneur d'un comprimé d'ibuprofčne ( 400 mg
d'aprčs le fabricant ). L'ibuprofčne est trčs peu soluble dans l'eau
mais trčs soluble dans l'éthanol. On dissout un comprimé dans 200 mL
d'une solution hydro-alcoolique dont le comportement est assimilable ŕ
celui d'une solution aqueuse. Aprčs élimination des excipients (
insolubles dans l'eau et l'éthanol ), 50,0 mL de cette solution sont
dosés par une solution d'hydroxyde de sodium de concentration 0,0500
mol/L. Véq = 9,70 mL.
Quelle est la masse d'ibuprofčne dans le comprimé testé ?
Quantité de matičre d'ibuprofčne dans 50 mL : 0,0500*9,70 10-3 = 4,85 10-4 mol ; soit dans 200 ml : 1,94 10-3 mol.
Masse : n M = 1,94 10-3 *206 =0,3996 g ~400 mg.
|
|