L'acide tartrique
: solution aqueuse, stťrťochimie, loi de Biot, bts Qiabi 2013.
En poursuivant votre navigation sur ce site, vous acceptez l’utilisation de Cookies vous proposant des publicitťs adaptťes ŗ vos centres d’intťrÍts.
|
|
.
|
|
|
|
|
L’acide
tartrique est utilisť comme additif alimentaire, il est dťsignť par le
code E334. Il peut jouer le rŰle d’antioxydant, de rťgulateur de pH ou
de sťquestrant. Il est autorisť dans la plupart des produits
alimentaires et on le trouve notamment dans les produits ŗ base de
cacao, dans le chocolat, dans les confitures et gelťes, dans les fruits
et
lťgumes en conserves …
L’acide tartrique est issu des dťchets de l’industrie vinicole : c’est
en effet le principal acide contenu dans le raisin.
Propriťtťs
de l’acide tartrique en solution aqueuse.
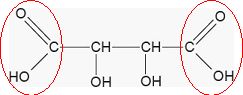
L’acide tartrique est l’acide 2,3-dihydroxybutanedioÔque. C’est un
diacide dont la formule semi-dťveloppťe est reprťsentťe ci-dessous. Entourer les
fonctions acide carboxylique.
L’acide tartrique (notť H2T) se comporte comme un diacide en
solution aqueuse et ses pKa ont pour valeur :
pKa1 = 3,04 ; pKa2 =
4,34 (ŗ 25 į C).
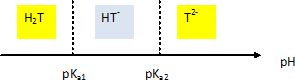
Indiquer,
sur un axe graduť en pH, les zones de prťdominance des espŤces suivantes
: H2T, HT- et T2-.
Ecrire
les ťquilibres acido-basiques successifs de dissociation de l’acide
tartrique dans l’eau et donner l’expression des constantes d’ťquilibre
correspondantes.
H2Taq + H2O(l) = H3O+aq + HT-aq.
Ka1 = [H3O+aq][HT-aq] / [H2Taq].
HT-aq
+ H2O(l)
= H3O+aq + T2-aq. Ka2
= [H3O+aq][ T2-aq] / [ HT-aq].
A partir des valeurs
des pKa, calculer
numťriquement les constantes Ka1 et Ka2.
Ka1 = 10-pKa1 = 10-3,04 =9,12 10-4.
Ka2
= 10-pKa2 = 10-4,34 =4,57 10-5.
Pour extraire l’acide tartrique du moŻt de raisin, on ajoute des ions
calcium Ca2+ : l’acide tartrique rťagit avec les ions
calcium Ca2+ pour former du tartrate de calcium, CaT, qui
est un sel peu soluble. L’ťquation de la rťaction ayant lieu est : Ca2+
(aq) + H2T(aq) + 2 H2O(l) =
CaT(s) + 2 H3O+(aq). (1)
Sa constante d’ťquilibre a pour valeur K = 5,4.10-2 ŗ 25 į C.
Donner
l’expression de K en fonction des concentrations des espŤces ŗ
l’ťquilibre.
K = [H3O+(aq)]2
/ ([H2T(aq)][Ca2+
(aq)]).
Discuter
qualitativement de l’influence d’une augmentation de la concentration
en ions calcium sur le rendement de l’extraction. Justifier.
A pH constant, une augmentation de la concentration en ion calcium,
dťplace l'ťquilibre (1) dans
le sens direct.
La masse de prťcipitť CaT(s) augmente ainsi que le rendement de
l'extraction.
Discuter
qualitativement de l’influence d’une augmentation du pH de la solution
sur le rendement de l’extraction. Justifier.
Une augmentation du pH ( diminuion de la concentration en ion oxonium
), dťplace l'ťquilibre
(1) dans
le sens direct.
La
masse de prťcipitť CaT(s) augmente ainsi que le rendement de
l'extraction.
|
| .
. |
|
|
Stťrťochimie.
On s’intťresse ŗ l’acide (+) tartrique ou (2R,3R) acide
2,3-dihydroxybutanedioÔque. Il comporte plusieurs atomes de carbones
asymťtriques.
Donner
la dťfinition d’un atome de carbone asymťtrique.
Un atome de carbone asymťtrique est tťtragonal et liť ŗ 4 atomes ou
groupe d'atomes diffťrents.
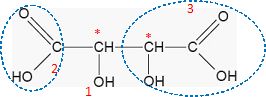
Repťrer
chaque atome de carbone asymťtrique par un astťrisque. Classer les groupes
attachťs ŗ chaque carbone asymťtrique par ordre de prioritť en suivant
les rŤgles de Cahn, Ingold et Prelog.
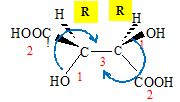
En
dťduire une reprťsentation de Cram du (2R,3R) acide
2,3-dihydroxybutanedioÔque. Justifier.
Le (2R,3R) acide 2,3-dihydroxybutanedioÔque possŤde un ťnantiomŤre.
Rappeler
ce que sont deux ťnantiomŤres.
Deux ťnantiomŤres sont deux molťcules images l'une de l'autre dans un
miroir plan. Ces deux molťcules ne sont pas superposables.
Donner
une reprťsentation de Cram de cet ťnantiomŤre.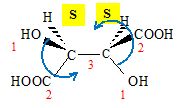
Quelle
propriťtť permet de distinguer deux ťnantiomŤres ?
Deux ťnantiomŤres font tourner la lumiŤre polarisťe de maniŤre opposťe.
Un stťrťoisomŤre de l’acide tartrique, dont une reprťsentation de Cram
figure ci-dessous, ne prťsente pas la propriťtť citťe ci-dessus. 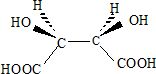
Indiquer
pour quelle raison ce stťrťoisomŤre ne prťsente pas cette propriťtť.
Cette molťcule possŤde un plan de symťtrie.
Activitť
optique.
L’activitť optique fut dťcouverte en 1811 par FranÁois Arago et Jean
Biot.
L’acide (+)-tartrique prťsente une activitť optique.
La loi de Biot permet de mesurer l’activitť optique. Dans le cas
oý une seule substance est active, elle peut s’ťcrire :
a = [a ]20D .L.C
Expliciter
les diffťrents termes intervenant dans cette relation et prťciser leur
unitť.
a (į) angle de rotation du plan de vibration des
ondes lumineuses ; [a
]20D : pouvoir
rotatoire spťcifique ( į m2 kg-1 ); C:
concentration ( kg m-3 ) ; L: longueur (m) de cuve.
Dťfinir les termes
dextrogyre et lťvogyre.
Il existe deux variťtťs de substances optiquement actives : les
substances lťvogyres qui font tourner le plan de polarisation vers la
gauche et les substances dextrogyres qui font tourner ce plan vers la
droite.
L’acide
(+)-tartrique est-il une substance dextrogyre ou lťvogyre ? Justifier.
Par convention, une
molťcule lťvogyre est notťe (-), et une molťcule dextrogyre est notťe
(+). L’acide (+)-tartrique est donc dextrogyre.
Le pouvoir rotatoire spťcifique de
l’acide (+)-tartrique est, ŗ la tempťrature de 20 į C :
[a
]20D =+12,5 į.dm-1.g-1.cm3.
|
.
|
|
La
lettre D indique que le pouvoir rotatoire spťcifique correspond ŗ des
mesures rťalisťes avec la raie D du sodium, onde monochromatique de
longueur d’onde l = 589 nm.
Dťterminer,
en joule puis en ťlectronvolt, l’ťnergie E des photons ayant cette
longueur d’onde.
h = 6,63 10-34 Js ; c = 3,00 108 m/s ; e = 1,60 10-19
C.
E = hc/l =
6,63 10-34 *
3,00 108/
(589 10-9) = 3,38 10-19 J ou 3,38
10-19 /(1,60
10-19)=2,11 eV.
Un
diagramme ťnergťtique simplifiť des niveaux d’ťnergie de l’atome de
sodium est reprťsentť.
Lťgender
ce diagramme en repťrant le niveau fondamental et les niveaux excitťs.

Quelle
ťnergie minimale faut-il fournir ŗ l’atome de sodium dans son ťtat
fondamental pour obtenir l’ion Na+ ? 5,14 eV.
Dťterminer
la transition ŗ laquelle correspond l’ťmission d’un photon de longueur
d’onde l = 589 nm.
5,14 -3,03 = 2,11 eV, transition du niveau n=2 vers le niveau n=1.
Le spectre
visible du sodium comporte deux autres raies ŗ 567 et 615 nm. La
lumiŤre ťmise par une lampe ŗ vapeur de sodium est donc polychromatique.
Indiquer
comment il est possible, ŗ partir d’une lampe ŗ vapeur de sodium,
d’obtenir une lumiŤre monochromatique de longueur d’onde l = 589 nm.
Le faisceau lumineux polychromatique issu de la source traverse une
fente d'entrťe situťe au point focal d'un miroir sphťrique : tous les
rayons rťflťchis par le miroir sont parallŤles.
Le faisceau parallŤle polychromatique est diffractť par un
rťseau,
puis est collectť par un autre miroir qui le focalise sur la fente de
sortie. Les diffťrentes longueurs d'onde sont sťparťes au niveau de la
fente de sortie chacune arrivant ŗ un point diffťrent de la fente.
Un technicien prťpare une solution aqueuse d’acide (+)-tartrique ŗ 1,0
mol.L-1. Il souhaite contrŰler la concentation de la
solution prťparťe, en utilisant la polarimťtrie.
AprŤs avoir traversť 30,0 cm de cette solution d’acide (+)-tartrique,
l’analyseur d’un polarimŤtre doit Ítre tournť de +5,5 degrťs pour
rťtablir l’ťquipťnombre (ŗ 20 į C).
En
utilisant la loi de Biot, dťterminer la concentration massique en acide
(+)-tartrique de la solution.
C
= a
/( [a ]20D
.L) =5,5 /(12,5 *3,0) =0,147 g cm-3.
En
dťduire sa concentration molaire en mol.L-1.
Masse molaire de l'acide tartrique : M =4*12+6+16*6=150 g/mol.
0,147/150 = 9,8 10-4 mol cm-3 = 0,98 mol /L.
La
concentration dťterminťe par la loi de Biot est-elle en accord avec la
concentration attendue ?
A 2 % prŤs les deux valeurs de la concentration sont en accord.
|
RŰle de conservateur.
Un sťquestrant est un additif alimentaire dont le rŰle est d’amťliorer la qualitť et la stabilitť des produits alimentaires.
Les sťquestrants sont, au sens chimique, des ligands qui forment des
complexes chimiques avec des ions mťtalliques tels que le cuivre, le
fer et le nickel, qui sont des catalyseurs de l’oxydation des matiŤres
grasses. Les sťquestrants limitent donc la disponibilitť de ces cations
et agissent ainsi comme des agents conservateurs.
La liqueur de Fehling contient un complexe qui se forme en milieu basique lors de la rťaction entre les ions cuivrique Cu2+ et les ions tartrate T2-. Les ions tartrate permettent la stabilisation des ions cuivrique en milieu basique.
A partir de quel pH les ions tartrate prťdominent-ils devant H2T et HT- ?
A partir de pH = pKa2 +1 = 5,4 les ions tartrate prťdominent devant H2T et HT-.
L’ion complexe prťsent dans la liqueur de Fehling a pour formule [CuT2]2-. Sa structure est plan carrť.
Ecrire l’ťquation de sa rťaction de formation en milieu basique.
Cu2+ aq + 2T2-aq = [CuT2]2-aq.
Le test ŗ la liqueur de Fehling permet de caractťriser les sucres (ou
oses) rťducteurs : en milieu basique, ŗ chaud et en prťsence d’un sucre
rťducteur, les ions cuivrique complexťs rťagissent pour donner un
prťcipitť rouge brique d’oxyde cuivreux Cu2O(s). L’ťquation de cette rťaction est :
2CuT2]2-aq +RCHO + 5HO-aq = Cu2O(s) + RCOO-aq + 4T2-aq + 3 H2O(l).
Rappeler le nom de la fonction prťsente dans les sucres rťducteurs qui rťagit avec les ions cuivrique complexťs.
La fonction aldehyde rťagit avec la liqueur de Fehling.
Ecrire les deux couples mis en jeu dans cette rťaction et identifier l’oxydant et le rťducteur de chaque couple.
Dans chaque couple l'oxydant est ťcrit en premier.
RCOO-aq / RCHO ; Cu2+aq / Cu2O(s).
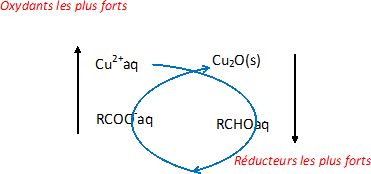
La rťaction observťe lors du test ťtant spontanťe, placer qualitativement ces couples sur l’axe des potentiels standards.
L'oxydant le plus fort rťagit spontanťment avec le rťducteur le plus fort.
|
|