Une
substance organique, le mecoprop ; alimentation triphasée
: Bts Métiers de l'eau 2014
En poursuivant votre navigation sur ce site, vous acceptez l’utilisation de Cookies vous proposant des publicités adaptées à vos centres d’intérêts.
|
|
.
|
|
|
|
|
L’hexachlorobenzène,
le pentachlorobenzène, le mécoprop font partie des substances
détectables par une station prototype installée à Ternay auprès du
Rhône, en aval de l’agglomération lyonnaise et des installations
pétrochimiques. Le mécoprop est un herbicide dont une étude a été menée
par l’INERIS.
Dans le rapport sont notées les indications suivantes concernant le
mecoprop :
Formule brute C10H11ClO3
; masse molaire M = 214,6 g.mol–1 ;
nom : acide 2-(4-chloro-2-methylphenoxy)-propanoïque ;
solubilité dans l’eau : 6,60 g.L–1 à pH = 4 et
250 g.L–1 à pH = 7 ; pKa = 3,11 ;
Formule semi-développée : 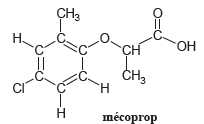
Écrire
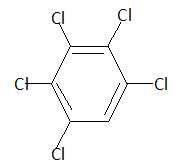
la formule topologique ou semi-développée du pentachlorobenzène.
Le mécoprop présente un caractère acide.
Reproduire
la molécule et entourer précisément la partie justifiant ce caractère
acide. Nommer la fonction organique associée. 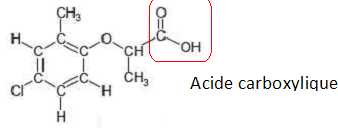
En
utilisant la formule brute, écrire l’équation d’équilibre acido-basique
du mécoprop dans l’eau.
C10H11ClO3
aq + H2O (l) = C10H10ClO3-
aq +H3O+aq.
On note le couple
acide base associé au mécoprop sous la forme HA/A–.
Exprimer
alors la constante d’acidité du couple et donner sa valeur.
AH aq + H2O (l) = A-
aq +H3O+aq.
Ka = [A-
aq][H3O+aq] / [AH aq] = 10-3,11
=7,76 10-4.
Une des étapes de
synthèse du mécoprop pourrait être la chloration du benzène.
Proposer
un catalyseur pour cette réaction. AlCl3.
Écrire
la réaction équilibrée de monochloration du benzène par le dichlore.
Nommer les produits obtenus.
Nommer
ce type de réaction.
C6H6 + Cl2
= C6H5Cl + HCl. Produits
: monochlorobenzène et chlorure d'hydrogène.
Il s'agit d'une substitution électrophile sur le noyaux benzénique.
Une autre étape en fin de synthèse pourrait consister en l’oxydation
d’une fonction alcool primaire du réactif noté R–CH2–OH,
en fonction acide carboxylique du mécoprop, par une solution diluée
d’ions permanganate en milieu acide.
Écrire
la demi-équation rédox associée à l’oxydation du réactif noté R–CH2–OH.
5 fois
{ R-CH2-OH
aq+ H2O(l) = R-COOHaq + 4H+
aq+ 4e-}.
Écrire
la demi-équation rédox associée au couple ion permanganate / ion
manganèse MnO4–(aq)/Mn2+(aq).
4 fois { MnO4–(aq)+
8H+aq + 5e- = Mn2+(aq)+4H2O
}.
Écrire la
réaction d’oxydation du réactif R–CH2–OH par
les ions permanganate en milieu acide.
Multiplier comme indiqué ci-dessus puis ajouter :
5R-CH2-OH
aq+ 5H2O(l) +4MnO4–(aq)+
32H+aq + 20e-=
5R-COOHaq + 20H+ aq+ 20e- +4Mn2+(aq)+16H2O
Simplifier : 5R-CH2-OH
aq +4MnO4–(aq)+
12H+aq =
5R-COOHaq +4Mn2+(aq)+11H2O(l).
|
| .
. |
|
|
Alimentation
triphasée.
La
station de surveillance de Ternay utilise un ensemble de pompes pour
prélever et analyser en continu l’eau du Rhône. La puissance active P
consommée par le groupe de pompage est de 350 kW.
La station est
alimentée par un réseau triphasé (230 / 400 / 50Hz). EDF assure la
gratuité de la puissance réactive Q à concurrence de 0,4 P. Ceci
correspond à : tan φ < 0,4 ; φ est le déphasage entre la tension
V(t) et le courant I(t). Le groupe de pompage est modélisé par le
schéma ci-dessous :
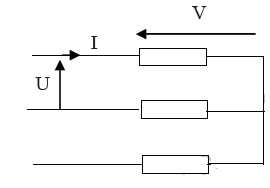
L’annexe
2correspond à un enregistrement du courant en ligne I(t) et de la
tension simple V(t) sur une des trois phases. Le même comportement est
observé sur chacune des phases.
Donner la période T du signal sinusoïdal.
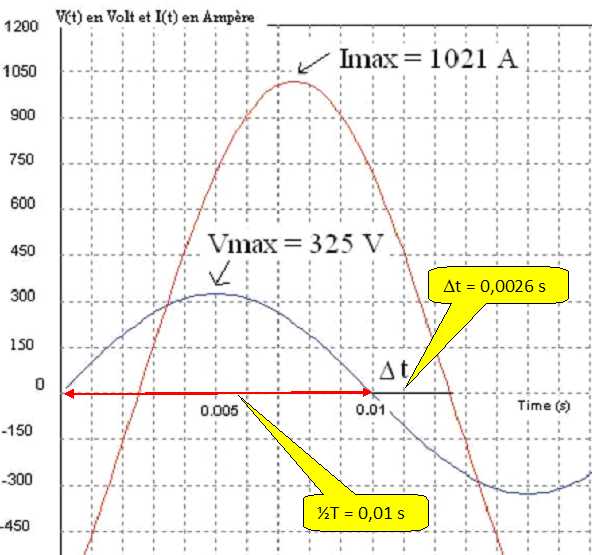
T = 0,01*2 = 0,02 s = 20 ms.
Evaluer le déphasage temporel Dt entre la tension V(t) et le courant I(t).
Montrer que l’angle φ associé au déphasage est proche de 45°.
0,0026 s =2,6 ms ; 2,6 / 20 = 0,13 T ;
une période correspond à 2 p radians ( 360 ° ) ; Dt = 360*0,13 =46,8°~47°.
Calculer le facteur de puissance cosφ.
cosφ = cos 46,8 =0,6845 ~0,68.
|
.
|
|
On compare les puissances active et réactive.
À partir des valeurs précisées en annexe 2, calculer les valeurs efficaces de la tension composée U et du courant en ligne I.
Ieff =Imax / 1,414 = 1021 / 1,414 = 722 A.
Veff = Vmax / 1,414 = 325 /1,414 ~230 V ; Ueff = 1,732 Veff = 1,732*230 =398 V.
Retrouver la valeur de la puissance active consommée par le groupe de pompage.
P = 1,732 Ueff Ieff cosφ= 1,732*398*722*0,68 =3,39 105 W ~340 kW.
Évaluer la puissance réactive Q.
Q = 1,732 Ueff Ieff sin φ= 1,732*398*722*sin 46,8 =3,63 105 W ~360 kW.
Vérifier que tan φ = Q/P.
tan φ =tan 46,8 = 1,06 ; Q/P =360 / 340 =1,06.
Le
groupe de pompage est-il économe ? Sinon quel type de composant permet
d’abaisser la valeur de « tan φ » et de limiter ainsi le coût
d’exploitation ?
tan φ n'est pas inférieur à 0,4 ; le groupe de pompage n'est pas économe.
Pour abaisser la valeur de tan φ il faut augmenter P, ou diminuer Q. On peut utiliser des condensateurs montés en dérivation.
|
|
|