Dosage de
l'insuline
: Bts analyses biologiques médicales 2014
En poursuivant votre navigation sur ce site, vous acceptez l’utilisation de Cookies vous proposant des publicités adaptées à vos centres d’intérêts.
|
|
.
|
|
|
|
|
L’insuline
est un régulateur de la glycémie. Actuellement, l’insuline est dosée
par immunofluorescence, mais avant cette technique le dosage de
l’insuline a bénéficié du développement de la radio-immunologie,
technique de dosage des grosses molécules biologiques mise au point, en
1960, par R. Yalow et S. Berson.
Partie 1 : la
méthode de radio-immunologie.
La méthode consiste à ajouter à la solution d’insuline à doser, de
l’insuline marquée par un atome radioactif, l’iode 125. Ce mélange est
ensuite mis en présence d’un anticorps spécifique. Un complexe
anticorps-insuline se forme alors à partir de l’insuline marquée et de
l’insuline non marquée dans des proportions liées aux concentrations
initiales. Le
complexe est isolé et on mesure son activité. Une courbe d’étalonnage
obtenue à partir de solutions d’insuline de concentrations connues
ayant subi le même traitement que l’échantillon étudié permet de
déterminer la concentration de l’insuline à partir de la valeur de
l’activité mesurée.
Indiquer
la composition du noyau d’iode 125.12553I.
53 protons et 125-53 = 72 neutrons.
L’iode 125 se désintègre par capture électronique interne, c’est à dire
en capturant un électron 0-1e de son cortège
électronique. Écrire
l’équation de la capture électronique de l’iode 125 en explicitant les
lois de
conservation
utilisées.
12553I
+ 0-1e
---> 12552Te.
Un proton se transforme en neutron : 0-1e
+ 10p
--->10n.
Conservation
de la charge : 53-1 = 52 ; conservation du nombre de nucléons.
Pour réaliser le dosage on
a réalisé une gamme de solutions témoins en faisant varier la
concentration d’insuline non marquée, la quantité d’insuline marquée
étant la même pour chaque solution. La mesure de leur activité conduit
aux données suivantes :
Concentration
en insuline non marquée ( µg/mL)
|
0
|
2,5
10-4
|
6,8 10-4 |
1,6 10-3 |
3,2 10-3 |
Activité
( Bq)
|
242
|
193
|
155
|
112
|
85
|
Tracer la courbe
donnant l'activité en Bq en fonction de la concentration en insuline.
La mesure réalisée avec l’échantillon de sérum sanguin donne une
activité de 142 Bq.
En
déduire la valeur de la concentration d’insuline dans le sérum dosé.
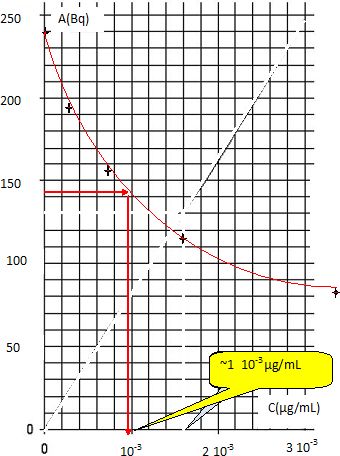
Estimer la valeur de l’activité de
l’échantillon dosé au bout d’un an de stockage.
Constante radioactive de l'iode 125 : l = 1,3 10-7 s-1.
Demi vie ou période
radioactive : T = ln2 / l
=ln2 / (1,3 10-7) =5,3 106 s ~62 jours.
1 an ~ 6 périodes ; l'activité au bout d'un an sear voisine de 142 / 26
~2 Bq.
.
|
| .
. |
|
|
L’insuline est une hormone
peptidique constituée de deux chaînes polypeptidiques comportant
respectivement 21 et 30 acides aminés. Ces deux chaînes sont reliées
entre elles par deux ponts disulfures.
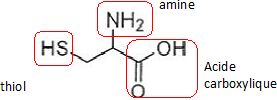
Les ponts disulfures s’observent au niveau des molécules de cystéine
dont la formule est donnée ci-dessous.
Recopier
la formule de la cystéine. Entourer les différents groupes fonctionnels
qu’elle comporte et les nommer.
La formation d’un pont disulfure est modélisée par la demi-équation
suivante :
2 R-SH = R-S-S-R + 2 H+ + 2 e –.
Justifier
que la formation de pont disulfure se fasse en conditions oxydantes.
Deux molécules R-SH s'unissent en libérant deux électrons ; RSH est
donc un réducteur qui s'oxyde.
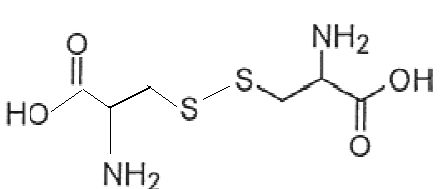
Deux molécules de cystéine s’unissent par un pont disulfure pour former
la cystine.
Écrire
la formule topologique de la molécule de cystine.
|
.
|