|
|
|
|
On donne en MeV/c2 la masse de quelques nuclťides et des nuclťons :
mP = 938,3 ; mN = 939,6.
Nuclťide
|
5626Fe
|
8438Sr |
105B |
3818Ar |
5525Mn |
147N |
84Be |
Masse
|
52 089,8
|
78 145,5
|
9 324,4
|
35 352,9
|
51 161,7
|
13 040,2
|
7 454,9
|
Nombre de proton
|
26
|
38
|
5
|
18
|
25
|
7
|
4
|
Nombre de neutron
|
56-26=30
|
46
|
5
|
20
|
30
|
7
|
4
|
Energie de liaison
par nuclťon ( MeV )
|
8,82
|
8,71
|
6,51
|
8,64
|
8,80
|
7,51
|
7,09
|
Energie de liaison = masse des protons + masse des neutrons - masse du noyau.
Dans le cas du fer : 26*938,3 + 30 * 939,6 -52 089,8 = 494 MeV/c2.
Energie de liaison par nuclťon : 494 / 56 =8,82 MeV.
Pour ces 7 nuclťides calculer en MeV l'ťnergie moyenne de liaison par nuclťon.
Voir tableau.
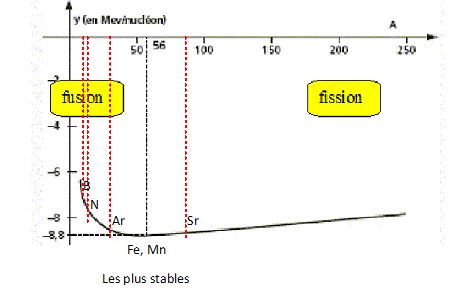
Placer
ces nuclťides sur la courbe d'Aston. Oý sont situťs les ťlťments les
plus stables ? Quels types de transformations nuclťaires sont
susceptible de se produire avec les ťlťments situťs ŗ droite du
graphique et avec ceux situťs ŗ gauche ?
Le noyau de l'ťlťment hydrogŤne possŤde 1 proton et celui de l'hťlium
en possŤde 2. La synthŤse de l'hťlium ŗ partir de l'hydrogŤne se
produit dans les ťtoiles suivant le processus appelť cycle
proton-proton I ( PPI) :
1H + 1H ---> 2H + n + x (i)
2H +1H ---> 3He + g (ii)
3He +3He ---> 4He +21H + g (iii)
Dans la rťaction (i) la particule x a pour masse 0,511 MeV/c2.
Quelle est cette particule ?
Un positon 01e.
Que reprťsentent les symboles n et g ?
Ils reprťsentent respectivement un neutrino et un photon.
Ecrire l'ťquation bilan de ce cycle.
4 1H---> 4He +2 n +2 01e + g.
En dťduire l'ťnergie dťgagťe en MeV par ce cycle. m(4He) = 3727,4 MeV/c2.
m(4He) + 2 m(01e)-4m(1H) =3727,4+2*0,511-4*938,3 = -24,8 MeV.
|
.
|
Le nuclťide 5525Mn peut capter un neutron. Le noyau obtenu peut se transformer spontanťment en 5626Fe en ťmettant une particule.
Ecrire les ťquations de ces deux transformations.
5525Mn + 10n--->5625Mn.
5625Mn ---> 5626Fe + 0-1e.
L'isotope 2H de l'hydrogŤne a pour masse 1875,6 MeV/c2. Il peut rťagir avec l'ťlťment 14N suivant :
14N + 2H ---> AZX +1H.
Identifier AZX.
Conservation de la charge : 7+1 = Z+1 d'oý Z = 7.
Conservation du nombre de nuclťons : 14+2 = A+1 d'oý A = 15.
147N + 21H ---> 157N +11H.
Sa masse est 13 968,9 MeV/c2.
Calculer l'ťnergie dťgagťe par cette rťaction.
m(157N) + m(11H)-m(147N)- m(21H)=13 968,9 +938,3 - 13 040,2-1875,6 = -8,6 MeV.
|
|