|
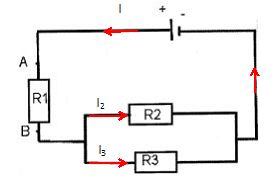
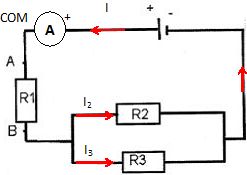
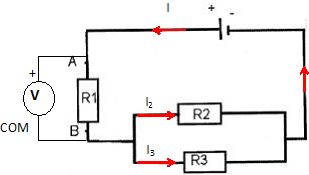
Si UAB = 2 V et R1 = 5 ohms, calculer l'intensité dans le circuit principal.
I = UAB / R1 =2 / 5 = 0,4 A.
Calculer la résistance équivalente au circuit. R2 = 20 ohm et R3 = 12 ohms.
Résistance équivalente à R2 et R3 montées en dérivation : R4 = R2R3 / (R2+R3) =20*12 / 32 =7,5 ohms.
Résistance équivalente à R1 et R4 en série : R = R1+R4 = 5+7,5 = 12,5 ohms.
Calculer la puissance absorbée.
P = RI2 = 12,5 *0,42 =2,0 W.
Le propane a pour formule C3H8. Calculer sa masse molaire M.
M = 12*3 + 8 = 44 g/mol.
Une bouteille contient 13 kg de ce gaz sous pression et liquéfié. Calculer la quantité de matière en moles.
n = m / M = 13 000 / 44 = 295,45 ~295 mol.
En déduire le volume qu'occuperait ce gaz dans les conditions normales de température et de pression Vm = 22,4 L/mol.
V = n Vm = 295,45 *22,4 = 6,6 103 L.
On brûle ce propane dans le dioxygène selon la réaction suivante. Equilibrer cette équation.
C3H8 + 5O2 ---> 3 CO2 + 4H2O.
Calculer le volume de dioxygène nécessaire à la combustion de 13 kg de propane.
n(O2)= 5 n = 5*295,45 = 1477 mol.
Volume de dioxygène : n(O2) Vm = 1477 *22,4 =3,3 104 L.
|