|
|
On souhaite réaliser la synthèse du composé D dont la formule est la suivante : C6H5-CH(NH2)-CH3.
Cette synthèse nécessite trois étapes :
Etape 1 :
On fait réagir du benzène C6H6 avec le monochloroéthane en présence de chlorure d'aluminum AlCl3, catalyseur et acide de Lewis.
Donner le type de cette réaction.
Substitution électrophile sur le noyau benzénique.
Ecrire la formule semi-développée du monochloroéthane
CH3-CH2Cl.
Ecrire l'équation de la réaction sachant qu'il se forme un composé A de formule C6H10.
CH3-CH2Cl +C6H6 ---> C6H5-CH2-CH3 + HCl.
Dans le mécnisme de cette réaction, intervient le composé électrophile E+ : CH3-CH2+. Expliquer sa formation.
E+ s'additionne sur le benzène pour donner un intermédiaire réactionel instable B. Ecrire la formule semi-développée de B.
Expliquer comment B se stabilise pour donner A.
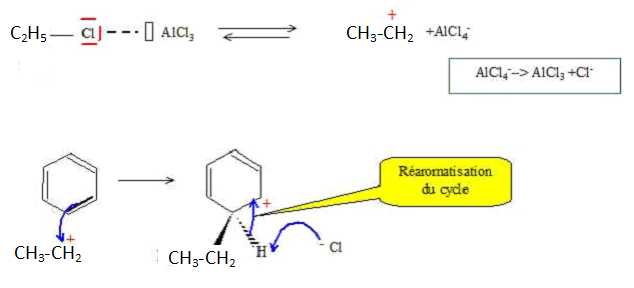
Le composé A réagit avec le dichlore en présence de lumière UV.
On obtient majoritairement C de formule C6H5-CH Cl-CH3.
Ecrire l'équation de cette réaction.
C6H5-CH2-CH3 + Cl2 --->C6H5-CH Cl-CH3 + HCl
Indiquer de quel type de réaction il s'agit.
Substitution radicalaire sur la chaîne latérale.
Donner en justifiant la représentation de Cram de l'isomère R du composé C.
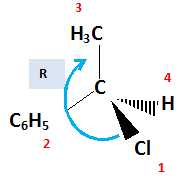
Les deux isomères R et S du composé C forment un couple d'énantiomères. Définir ce terme.
Deux énantiomères ne différent que par leur propriétés optiques ; ils sont
séparables. Ce sont 2 isomères de configuration, images l'un de l'autre dans un
miroir.
Un des isomères de C est dextrogyre. Quelle propriété optique possède cet isomère ?
Une molécule dextrogyre a la propriété de faire dévier le plan de polarisation
de la lumière polarisée vers la droite d'un observateur qui reçoit la
lumière. Une
molécule dextrogyre est notée avec un (+) devant sa nomenclature. Le pouvoir rotatoire,
déterminé expérimentalement, est positif.
Un mélange équimolaire des deux isomères possède-t-il la même propriété ?
Un
tel mélange est optiquement inactif vis à vis de la lumière polarisée,
les pouvoirs rotatoires s'ajoutant et étant opposés.
|
| .
. |
.
.
Etape 3.
Le composé C réagit avec l'ammoniac NH3 pour donner le composé D.
A quelle famille de composé appartient le composé D ? Donner sa classe.
Amine secondaire.
Ecrire l'équation de la réaction conduisant à D.
C6H5-CH Cl-CH3 + 2NH3 ---> C6H5-CH(NH2)-CH3 + NH4+ + Cl-.
Donner le schéma de Lewis dela molécule d'ammoniac. Représenter cette molécule dans l'espace.
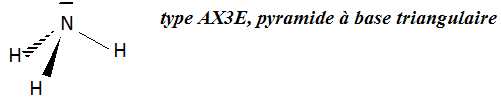
Dans la molécule qu'appelle-t-on site nucléophile ? Le doublet d'électrons libres, non liant.
Pourquoi dit-on que la molécule est nucléophile ?
Nucléophile : ami des noyaux ; une molécule possédant un excès d'électrons est dite nucléophile.
Indiquer sur quel site du composé C aura lieu l'attaque de NH3.
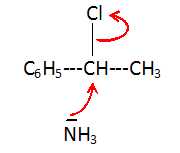
|
.
|