|
|
Le fart est un revêtement spécifique appliqué
sous les skis ou les planches à neige avant usage. Il permet
d’améliorer soit le glissement, soit l'adhérence sur la neige.
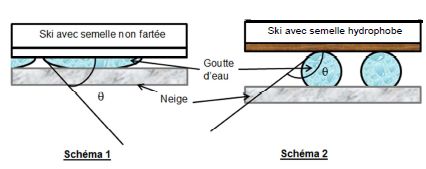
Lors de la glisse, des gouttes d’eau se forment à l’interface
ski-neige. Lorsqu’une goutte s’établit au contact d’un solide, elle
adopte une configuration particulière qui traduit les interactions
entre le solide et le liquide. L’angle q, représenté sur les schémas
cidessous, caractérise ces interactions.
Représenter les
forces extérieures appliquées au centre d’inertie G du système
considéré, en supposant le mouvement rectiligne uniformément accéléré.
On apportera un soin particulier à la longueur relative des vecteurs,
sans toutefois choisir d’échelle particulière. L’action due à l’air ne
sera pas prise en compte.
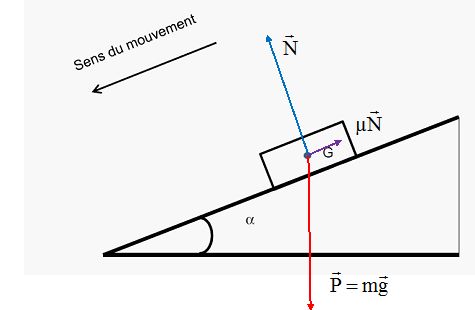
Rédiger
une légende explicative du schéma proposé.
Poids P, vertical, orienté vers le bas, valeur mg.
N : action normale du plan, perpendiculaire au plan, orienté vers le
haut, valeur mc cos a.
µN : force de frottement parallèle au plan, de sens contraire à la
vitesse.
µ : coefficient de frottement, il dépend des matériaux en contact et de
la rugosité.
|
| .
. |
.
|
Décrire en quelques
lignes, les transferts d’énergie mis en jeu dans la situation évoquée.
Au cours de la descente l'énergie potentielle de pesanteur est
convertie en énergie cinétique et en énergie thermique ( force de
frottement )
La chaleur fait fondre la neige, et une pellicule d’eau s’interpose
entre le ski et la neige.
Expliquer
pourquoi les fluorocarbures sont particulièrement intéressants pour le
fartage.
Les fluorocarbures sont hydrophobes. L'eau ne s'étale pas sous le ski (
schéma 1) mais des gouttes d'eau apparaissent entre le ski et la neige
(schéma 2) optimisant la glisse, les frottements étant diminués.
Les
électronégativités des éléments hydrogène, carbone et fluor sont
respectivement 2,1 ; 2,6 et 4,0.
Les hydrocarbures solides à longue chaîne carbonée utilisés pour le
fartage des skis, ont pour formule générale CnH2n+2
(avec n ≥18).
En
quoi ces hydrocarbures sont-ils également intéressants pour le fartage
?
Le carbone et l'hydrogène ont des électronégativités voisines. Les
hydrocarbures sont donc apolaires.
l'eau est une molécule polaire. Les hydrocarbures sont hydrophobes.
De plus ils coûtent moins cher et polluent moins que les fluorocarbures.
Les fluorocarbures sont des polymères de formule semi-développée
suivante.
Mettre
en évidence le caractère polaire d’une liaison C – F.
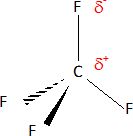
Pourquoi,
selon vous, les molécules de fluorocarbure sont cependant hydrophobes
?
Du fait de la symétrie tétraèdrique le barycentre des charges négatives
est situé sur le carbone.
Le barycentre des charge négative et le barycentre des charges
positives sont confondus. La molécule est donc apolaire.
|
|