On se propose d'ťtudier la vitesse de la rťaction entre les
ions iodure I- et les ions peroxodisulfate S2O82-.
|
|
On prťpare 300 mL d'une solution d'iodure de
potassium dont la concentration en solutť dissous KI est
ťgale ŗ c1 = 2/15 mol/L.
On prťpare 300 mL d'une solution de
peroxodisulfate de potassium dont la concentration en
solutť dissous K2S2O8 est
ťgale ŗ c2 = 1/30 mol/L.
A l'instant t=0 on mťlange les deux solutions, on obtient un mťlange de
volume V = 600 mL.
Mťlange initial
et rťaction ťtudiťe.
La rťaction ťtudiťe a pour ťquation : 2I-aq + S2O82-aq
= I2aq + 2SO42-aq.
Ecrire
les deux couples oxydant / rťducteur mis en jeu.
S2O82-
aq/ SO42- aq et I2 aq/ I-aq.
Dťterminer les quantitťs de matiŤre
initiales des ions iodure, des ions peroxodisulfate et des ions
ptassium dans le mťlange initial.
n(I-aq)0=0,300
*2/15 =4,0 10-2 mol.
n(S2O82-
aq)0=0,300*1/30 = 1,0 10-2 mol.
n(K+ aq)0= 4,0 10-2 + 2,0 10-2 = 6,0
10-2 mol.
Autre mťthode
: la solution reste ťlectriquement
neutre :
n(I-aq)0+
2 n(S2O82-
aq)0=n(K+
aq)0.
On observe le mťlange : il change de teinte, passant de
l'incolore au jaune de plus en plus foncť, puis au marron.
En
quoi cette observation confirme-t-elle que la rťaction est lente
?
L'oeil a le temps de suivre l'ťvolution de la couleur de la solution et
de distinguer les diffťrentes teintes.
On sait que la rťaction est totale.
Construire,
avec les valeurs numťriques, un tableau descriptif d'ťvolution du
systŤme chimique.
|
avancement
(mol)
|
2I-aq |
+ S2O82-aq |
= I2aq |
+ 2SO42-aq. |
initial
|
0
|
0,04
|
0,01
|
0
|
0
|
en
cours
|
x
|
0,04-2x
|
0,01-x
|
x
|
2x
|
fin
|
xmax
|
0,04-2xmax |
0,01-xmax |
xmax |
xmax |
|
| .
. |
Quelle
est la quantitť de diiode formťe quand la rťaction est terminťe ?
Si I-aq est en dťfaut : 0,04-2xmax= 0 ; xmax= = 0,02 mol.
Si S2O82-aq est en dťfaut : 0,01-xmax= 0 ; xmax= = 0,01 mol. On retient la plus petite valeur (S2O82-aq est en dťfaut).
Il se forme donc 0,010 mol = 10 mmol de I2aq.
Etude cinťtique.
On recommence la mÍme expťrience, dans des conditions identiques, mais
cette fois, toutes les cinq minutes, on prťlŤve un volume V0=25,0
mL du mťlange ; on lui ajoute approximativement 100 mL d'eau trŤs
froide et un peu d'empois d'amidon. On dose le diiode en solution avec
une solution de thiosulfate de sodium de concentration c3=
0,010 mol/L. L'ťquation support du titrage est :
I2aq + 2S2O32-aq = 2 I-aq
+ S4O62-aq.
Pourquoi
ajoite-t-on de l'eau froide au prťlevement ?
L'ajout d'eau froide rťalise un
blocage cinťtique de la rťaction.
Quelles
sont les caractťristiques indispensables de la rťaction pour qu'elle
puisse servir de titrage ?
La rťaction doit Ítre rapide et totale.
Dans quoi
place-t-on la solution titrante ? ťprouvette graduťe,
burette graduťe, fiole jaugťe, becher, erlenmeyer.
La solution titrante se trouve dans une burette graduťe.
Quel est
le rŰle de l'empois d'amidon ?
L'empois d'amidon joue le rŰle d'indicateur de fin de rťaction.
Pour chaque titrage, le volume VE de solution titrante pour
obtenir l'ťquivalence est donnťe dans le tableau ci-dessous.
Justifier
la relation x = 0,12 VE qui a ťtť utilisťe
pour complťter la 3Ť ligne du tableau.
A l'ťquivalence les quantitťs de matiŤre des rťactifs sont en
proportions stoechiomťtriques : x = n(I2aq) = Ĺn(S2O32-aq).
x = ĹVE c3 = 0,5 *0,01 VE ; [I2aq]
= 0,005 *0,01 VE mol de diode dans le prťlevement de
25 mL soit 0,005*600 / 25 = 0,12 VE dans le
mťlange total de volume 600 mL.
| t(min)
|
0
|
5
|
10
|
15
|
20
|
25
|
30
|
35
|
40
|
45
|
50
|
55
|
60
|
65
|
70 |
VE(mL)
|
0
|
1,5
|
2,6
|
3,7
|
4,5
|
6,0
|
6,8
|
7,8
|
8,8
|
9,7
|
10,5
|
11,4
|
12,4
|
13,2
|
13,7
|
x
(mmol)
|
0
|
0,18
|
0,31
|
0,44
|
0,54
|
0,72
|
0,82
|
0,94
|
1,06
|
1,16
|
1,26
|
1,37
|
1,49
|
1,58
|
1,64
|
|
A partir du tableau on a
construit la courbe d'ťvolution de l'avancement x (mmol) en fonction du
temps (min).
Rappeler
la dťfinition de la vitesse volumique de rťaction. Peut-on la
dťterminer ŗ t=0 ? Si non indiquer pourquoi et si oui, donner sa valeur.
v = 1/V dx/dt avec V =0,60 L volume de la solution.
dx/dt est le coefficient
directeur de la tangente ŗ la courbe ŗ la date t. On peut donc dťterminer graphiquement [dx/dt]t=0
puis en divisant par V = 0,60 L, calculer la vitesse initiale de la
rťaction.
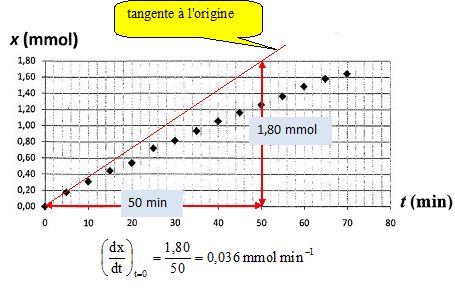
v(t=0) =
0,036 / 0,6 = 0,06 mmol L-1 min-1.
Rappeler la
dťfinition du temps de demi-rťaction. Peut-on le dťterminer ? Si non
indiquer pourquoi et si oui, donner sa valeur.
Le temps de demi-rťaction est la durťe au bout
de laquelle l'avancement est ťgal ŗ la moitiť de l'avancement final. La
rťaction ťtant totale xfin = xmax = 0,010 mol.
xtĹ = Ĺxfin = 0,005 mol = 5,0 mmol. Le graphe ne
permet pas la dťtermination de tĹ.
|
|
