.
|
|
Des
nodules métalliques ont été identifiés au fond des océans. Les bons
nodules contiennent en moyenne 1,25 à 1,5 % de nickel, 1 à 1,4 % de
cuivre ainsi que 27 à 30 % de manganèse, 0,2 à 0,25 % de cobalt.... Les
dépôts de faible profondeur ( <250 m ) sont exploités.
L'acide nitrique concentré attaque le cuivre.
2NO3-aq + 3 Cu(s) + 8 H3O+aq ---> 2 NO(g) + 3Cu2+aq + 12 H2O(l).
On prépare les solutions diluées, notées Sdi, à partir d'une solution mère de sulfate de cuivre (II) de concentration Cm = 0,5 mol/L. On mesure ensuite l'absorbance de ces solutions.
| Solution |
Sm |
Sd1 |
Sd2 |
Sd3 |
Sd4 |
Sd5 |
| [Cu2+] mol/L |
0,500 |
0,250 |
0,200 |
0,100 |
0,050 |
0,010 |
| A |
xxx |
3,0 |
2,4 |
1,2 |
0,60 |
0,12 |
Pour
déterminer le pourcentage massique en cuivre d'un nodule polymétallique
de masse m = 50 g, on verse 50 mL d'acide nitrique concentré sur le
nodule finement broyé. Après réaction et filtrage, le filtrat est versé
dans une fiole jaugée de 1 L que l'on complète avec de l'eau distillée.
On mesure son absorbance à l = 800 nm . A = 0,50.
Quelle est la couleur de la solution obtenue après action de l'acide nitrique concentré sur le nodule ?
La solution contient, entre autres, l'ion cuivre (II) aqueux de couleur bleue.
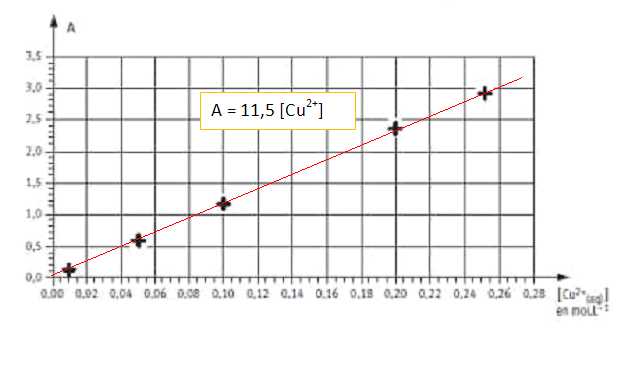
Le graphe suivant illustre la loi de Beer-Lambert ; l'absorbance et la concentration [Cu2+] sont proportionnelles.
Proposer un protocole pour préparer 100 mL de la solution Sd1 à partir de la solution mère Sm.
Facteur de dilution F = 0,500 / 0,250 = 2.
Prélever 100 / F = 100 / 2 = 50,0 mL de solution mère à l'aide d'une pipette jaugée.
Placer dans une fiole jaugée de 100 mL et compléter à l'aide d'eau distillée jusqu'au trait de jauge.
Boucher et agiter pour rendre homogène.
|
.
La valeur de l'absorbance de la solution est connue avec une incertitude expérimentale DA = 5 10-3.
Calculer la masse de cuivre contenue dans la solution analysée.
Concentration de la solution en ion cuivre (II) : C = A / 11,5 = 0,50 /11,5 =4,347 10-2 mol/L.
Masse de cuivre dans 1 L ( ou dans 50 g de nodule ) : C M(Cu) = 4,347 10-2 *63,5 = 2,76 ~2,8 g.
Le nodule polymétallique est-il un bon nodule ?
2,8
g de cuivre dans 50 g de nodule soit 2,8*100/50 = 5,6 %, valeur
supérieure à la moyenne " 1 à 1,4 % de cuivre. Il s'agit donc d'un bon
nodule.
Cette
méthode de détermination de la teneur en cuivre d'u nodule
polymétallique de composition inconnue peut parfois surévaluer la
teneur en cuivre.
Expliquer pourquoi et proposer une amélioration de la méthode.
Le
nodule contient d'autres métaux que le cuivre ; la solution issue de
l'attaque par l'acide nitrique contient d'autre ions que Cu2+aq.
Ces derniers peuvent apporter leur contribution à l'absorbance de la
solution préparée à partir du filtrat. Il faudrait donc soit éliminer
les autres ions métalliques de la solution, soit se placer dans le cadre d’une lixiviation ammoniacale conduisant au complexe [Cu(NH3)4]2+
puis mesurer l'absorbance de la solution à une longueur d'onde où
ce complexe présente un maximum d'absorption. Les autres espèces
colorées présentes en solution doivent, à cette longueur d'onde,
présenter une absorption minimale voir nulle.
|
|
|