|
Concours adjoint technique principal de laboratoire ( interne Lille )2010. |
|||||||
| .
. |
|||||||
|
|||||||
|
Pour réaliser un dosage un professeur vous demande un volume V = 1,00 L d'une solution de permanganate de potassium de concentration c = 0,0250 mol/L. Vous disposez d'une solution mère de concentration c0 = 0,500 mol/L. Vous en prélevez : ( 20 mL ; 5,00 10-2 L ; 50,0 mL ; 25,0 mL ; 5,00 10-3 L ) Facteur de dilution F = c0 / c = 0,500 / 0,0250 =20 ; volume de la pipette jaugée = volume de la fiole jaugée / F = 1,00 / 20 = 5,00 10-2 L = 50,0 mL. Avant de ranger les électrodes combinées de verre( celles-ci étant utilisées couramment ), vous vérifier qu'elles sont : A. immergées dans l'eau distillée. Faux. B. immergées dans une solution saturée de chlorure de potassium . Vrai. Solution de chlorure de potassium à 3 mol/L. C. immergées dans une solution saturée de chlorure de sodium . Faux. D. immergées dans l'eau du robinet. Faux. Un flacon d'acide éthanoïque a été stocké sans indiquer sa concentration. Pour déterminer rapidement celle-ci vous réalisez le dosage de V =10,0 mL avec une solution d'hydroxyde de sodium de concentration c = 0,050 mol/L. Pour déterminer l'équivalence vous utilisez un indicateur coloré. Le volume obtenu à l'équivalence est VE = 12,0 mL. Sachant que la réaction qui a lieu se fait mole à mole, vous en déduisez que la concentration de l'acide est en mol/L : 4,2 10-2 ; 0,060 ; 0,24 ; 0,050 ; 6,0 10-2 ). A l'équivalence les quantités de matière des réactifs sont en proportions stoechiométriques ; c VE = V CA ; CA =c VE / V =0,050 *12/10 = 0,060 mol/L = 6,0 10-2 mol/L.
Nommer les deux montages suivants : 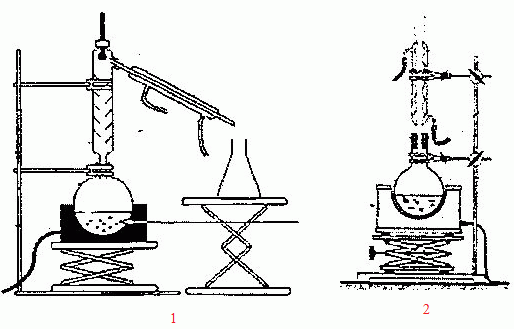 1 : montage de distillation fractionnée ; 2 : chauffage à reflux. -Porter des lunettes ( utilisation d'une solution de soude concentrée ) - dans un ballon introduire 10 mL d'huile ( densité 0,9), 20 mL de solution de soude à 0,75 mol/L et 10 mL d'éthanol - ajouter quelques grains de pierre ponce - chauffer à reflux pendant 30 min - verser le mélange encore chaud dans un becher contenant 100 mL d'eau salée froide de concentration 200 g/L. Cette opération s'appelle le relargage. - écraser les grumeaux et bien agiter - filtrer sous pression réduite à l'aide d'un filtre büchner - rincer avec de l'eau salée froide et mesurer le pH du filtrat - faire secher le savon à l'étuve et le peser. Faire la liste du matériel nécessaire. Chauffage à reflux : élévateur à croisillons, support, ballon de 100 mL, chauffe ballon et réfrigérant droit. Filtration sous vide : filtre Büchner, trompe à eau Lunettes de protection, spatule, huile, soude ( solution hydroalcoolique) , pierre ponce, eau salée, étuve et balance de précision. Un flacon porte l'étiquette suivante : 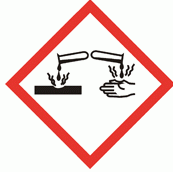 Solurion d'hydroxyde de sodium à 30 %. Provoque de graves brûlures. A l'aide d'une pipette, vous devez prélever 20 mL d'une solution concentrée d'hydroxyde de sodium et les verser dans une fiole jaugée en vue d'une dilution. Pour cela, il faut : A. des lunettes de sécurité. Vrai. B. une hotte aspirante. Faux. C. des chaussures de sécurité. Faux. D. des gants en latex. Vrai. E. des gants souples en PVC. Faux. Un collègue reçoit de l'acide chlorhydrique dans les yeux. Quelles sont les mesures d'urgence à prendre ? A. ne rien faire mais prévenir l'infirmerie. Faux. B. rincer les yeux sous l'eau du robinet pendant 5 min. Faux. C. rincer les yeux avec un rince oeil plusieurs fois. Vrai. D. donner un papier absorbant pour éliminer l'acide. Faux. E. mettre une solution basique dans les yeux pour neutraliser l'acide. Faux.
Vous
devez réaliser V =500,0 mL d'une solution de sulfate de cuivre de
concentration c =0,100 mol/L à partir du solide (M = 229 g/mol). Vous
pesez une masse de solide égale à : Un professeur souhaite projeter des images qu'il a stockées sur clef USB. De quoi à t-il besoin ? ( d'un lecteur DVD ; une télévision ; un vidéoprojecteur relié à un ordinateur ; un rétroprojecteur ; un accès à internet ) Vous
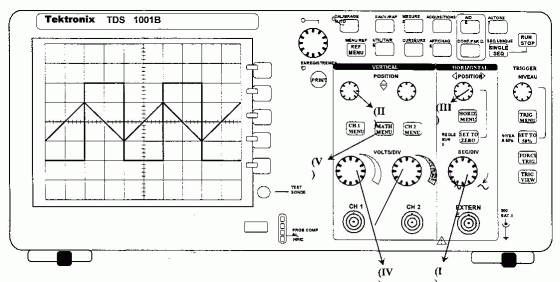
disposez d'un capteur de pression muni d'une sortie analogique
permettant de mesurer la pression du dihydrogène se dégageant par
action de l'acide chlorhydrique sur un morceau de magnésium. L'objectif
est de suivre l'évolution de la pression P au cours du temps et
d'obtenir la courbe P = f(t). Il vous faut au minimum, en plus du
capteur de pression et de l'ordinateur équipé d'un logiciel type
tableur-grapheur :
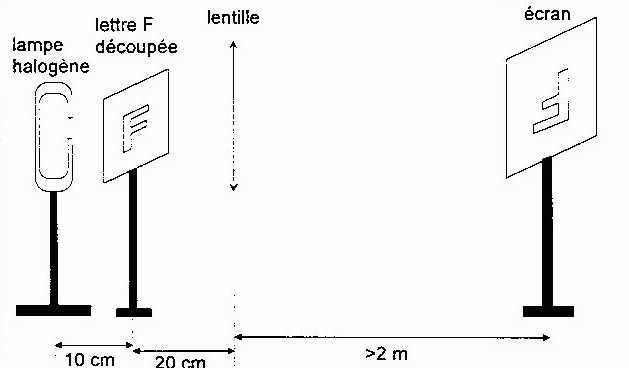
Après la synthèse du benzaldehyde solide, on désire vérifier sa pureté. La lentille est : divergente, convergente, astringente, afocale, auto-focus. Pour
réaliser la synthèse additive de la lumière blanche sur un écran blanc
avec trois projecteurs de diapositives utilisés simultanément, il faut
les filtres suivants :
|
|||||||
| |
|||||||
|
|