|
L'aspirine : synthŤse, dosage bac S Amťrique du Sud 2009. En poursuivant votre navigation sur ce site, vous acceptez l’utilisation de Cookies vous proposant des publicitťs adaptťes ŗ vos centres d’intťrÍts. |
|||||||||||||||||||||||||||||||
|
|||||||||||||||||||||||||||||||
|
Donnťes :
Masses molaires :
-
de l’acide salicylique : Mac = 138 g.mol -1
-
de l’anhydride acťtique (ou ťthanoÔque) : Manh = 102
g.mol
-1
-
de l’aspirine : Masp = 180 g.mol -1 Masse volumique de l’anhydride acťtique (ou ťthanoÔque) : r = 1,08 g.mL -1
Structure et formulation. Donner le nom des
groupes caractťristiques
encadrťs dans les formules topologiques de : la
salicine ; l’acide salicylique ; l’acide
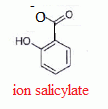
acťtylsalicylique. 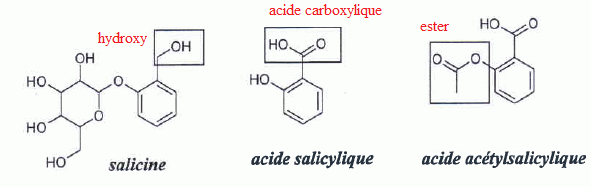 L’acide salicylique
possŤde une base
conjuguťe, l’ion salicylate, mentionnť dans le texte. Donner
sa formule topologique.
De la mÍme maniŤre, l’acide
acťtylsalicylique ou aspirine, possŤde une base conjuguťe,
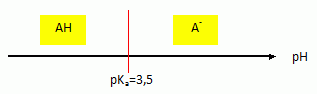
l’ion acťtylsalicylate. Le couple, qu’on notera plus simplement AH/A-
possŤde un pKa de 3,5.
Tracer son diagramme
de prťdominance. Sachant que le pH de
l’estomac est
voisin de 1, citer l’espŤce prťdominante de ce couple. Quand
l’aspirine reste trop longtemps sous cette forme
prťdominante dans l’estomac, elle y provoque des lťsions gastriques.
C’est
pourquoi on trouve dans le commerce des formulations en poudre, moins
agressives, ŗ base d’acťtylsalicylate de sodium, associť ŗ de
l’hydrogťnocarbonate de sodium. La dissolution de la poudre dans un
verre d’eau est
rapide et totale. La solution obtenue contient les ions
acťtylsalicylate A–(aq)
et hydrogťnocarbonate, de formule HCO3–(aq). Donnťes : pKa
du couple (CO2,
H2O)(aq) / HCO3–(aq)
=
6,4
AprŤs
absorption, ces ions pťnŤtrent dans l’estomac oý le
pH est trŤs acide. …crire l’ťquation de la rťaction se produisant entre les ions hydrogťnocarbonate et les ions oxonium prťsents en abondance dans l’estomac. HCO3–(aq) + H3O+aq =
CO2 aq + 2H2O(l). Calculer la constante d’ťquilibre K de cette rťaction. K = [CO2 aq , H2O]
/ ([H3O+aq][HCO3–(aq)])
= 1 / Ka = 1/ 10-6,4 =2,5 106. Au moment
de
l’ingestion du verre d’aspirine, le quotient de rťaction initial est
faible par
rapport ŗ K, en
dťduire l’influence des ions hydrogťnocarbonate sur le pH de
l’estomac.
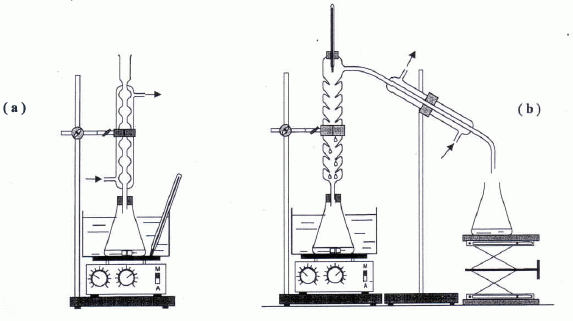
SynthŤse.
Lequel de ces deux montages permet de
rťaliser un chauffage ŗ reflux ?
Justifier.
Donner la formule
semi-dťveloppťe de l’anhydride acťtique (ou ťthanoÔque). Pourquoi utilise-t-on l’anhydride
ťthanoÔque
plutŰt que l’acide acťtique pour cette synthŤse ? …crire l’ťquation de
la synthŤse de
l’aspirine ŗ partir de l’anhydride acťtique et de l’acide salicylique. 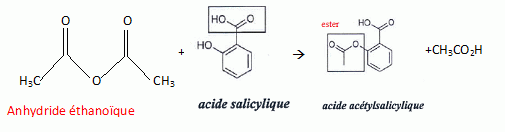 Dans
un erlenmeyer bien sec, on introduit 10,0 g d’acide
salicylique, 12,0 mL d’anhydride acťtique et 0,50 mL
d’acide sulfurique concentrť. ņ quoi sert l’acide
sulfurique ?
Si l'anhydride est en dťfaut : 0,127-xf
=0 ; xf
=0,127 mol
AprŤs 20 minutes de chauffage,
on sort
l’erlenmeyer du bain-marie. On introduit par le haut du
rťfrigťrant 20 mL d’eau distillťe pour dťtruire l’anhydride
acťtique restant. Quand
l’ťbullition a cessť, on ajoute 50 mL Calculer le rendement de cette synthŤse. mexp / mthťo=10,5 / 13,04 =0,805 ~ 80,5 %.
|
|||||||||||||||||||||||||||||||
| |
|||||||||||||||||||||||||||||||
|
|