En poursuivant votre navigation sur ce site, vous acceptez l’utilisation de Cookies vous proposant des publicitťs adaptťes ŗ vos centres d’intťrÍts. |
||||||||||||||||||||||||
|
||||||||||||||||||||||||
|
Texte : on utilise la
spectrophotomťtrique pour doser la cafťine
dans deux solutions de cafť, notťes
S1 et S2, de concentration respective
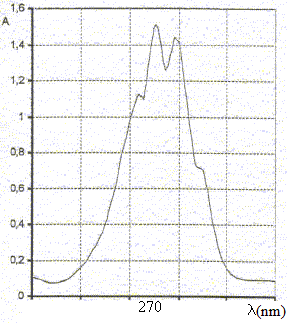
en cafťine c1, c2. On mesure l'absorbance ŗ l = 270 nm des solutions de cafťine et on trouve :
Questions relative aux courbes et au domaine du spectre ťlectromagnťtique.
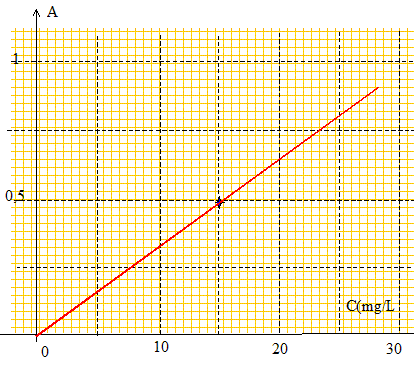
l=270 nm appartient au domaine UV. La valeur de l'absorbance dťpend de la longueur d'onde utilisťe. L'absorbance est une grandeur sans unitť. Les longueurs d'ondes des radiations visibles par l'oeil humain sont comprises entre 400 nm et 800 nm. Questions relatives ŗ l'absorbance et ŗ la concentration. Pour des concentrations assez faibles et pour une longueur d'onde donnťe, l'absorbance A d'une solution colorťe est proportionnelle ŗ sa concentration. La courbe A=f(C) est une droite passant par l'origine et de coefficient directeur : 0,5/15 = 3,33 10-2 L mg-1. A = 3,33 10-2 c ; c1 = A1 / 3,33 10-2 = 0,4*15/0,5 ; c1 =12 mg/L. c2 = A2 / 3,33 10-2 = 0,6*15/0,5 ; c2 =18 mg/L.
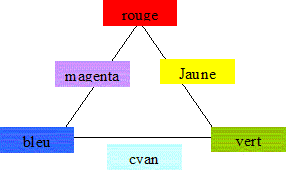
La couleur d'une substance colorťe est
celle de la couleur qu'elle diffuse.
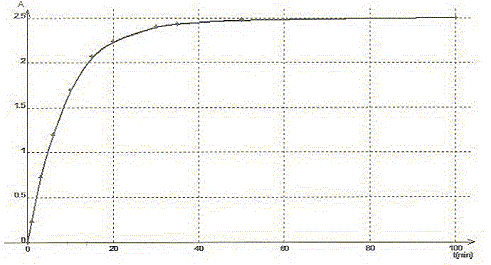
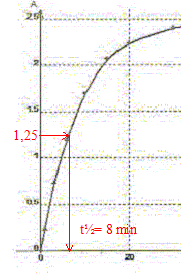
Par spectrophotomťtrie on suit la cinťtique de la rťaction des ions iodures I-(aq) avec les ions peroxodisulfate S2O82-(aq) qui conduit ŗ la formation de diiode ( jaune en solution) et d'ion sulfate. Cette rťaction est lente et totale. La transformation est modťlisťe par l'ťquation chimique : S2O82-(aq) + 2 I-(aq) = I2(aq) + 2SO42- (aq). Les concentrations et volumes des rťactifs introduits sont les suivants : S2O82-(aq) : c1 = 0,50 mol/L ; v1 = 10,0 mL I-(aq) : c2 = 0,020 mol/L ; v2 = 10,0 mL. On a mesurť l'absorbance au cours du temps et obtenu la courbe ci-dessous : On rappelle la loi de Beer aux faibles concentrations : A = k [I2] oý k est un coefficient de proportionalitť.
A. Le temps de demi-rťaction tĹ vaut environ 30 min. Faux.
B. L'ion peroxodisulfate est le rťactif limitant. Faux. Quantitť de matiŤre d'ion S2O82-(aq) : c1v1 = 0,5*10 = 5 mmol Quantitť de matiŤre d'ion I-(aq) : c2v2 = 0,02*10 = 0,2 mmol ŗ partir de 0,2 mmol d'ion I-(aq) il faut, d'aprŤs les coefficients stoechiomťtriques, 0,1 mmol d'ion S2O82-(aq) : or on en a 5 mmol. S2O82-(aq) est en large excŤs. C. La rťaction ťtant totale, la concentration finale doit Ítre [I2]max= 10 mmol/L. Faux. [I2]max=Ĺ[I-(aq)]initial =c2v2 /(v1+v2) =0,1/20= 5 10-3 mol/L = 5 mmol/L D. La valeur de k pour la longueur d'onde choisie est 5,0 102 L mol-1. Amax = k
[I2]max ; k=Amax
/[I2]max=2,5 / 5
10-3 = 500 L mol-1. Vrai.
|
||||||||||||||||||||||||
|
|
||||||||||||||||||||||||
|
|