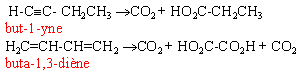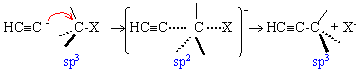. .
voir le match : l'essentiel du cours
les alcènes (quiz et exercices corrigés)
|
|
|
|
|
|
corrigé
Seul le propyne réagit avec le chlorure de cuivre
en donnant ![]()
de masse molaire 102,6 gmol-1. Il s'est formé 0,916 /102,6 = 8,93 10-3 mol
volume de propyne : 22,4*8,93 10-3 =
0,2 L
ou 20%
Le brome (en excès) est
fixé par le propyne et le propène.
C3H4 + 2 Br2 --> C3H4Br4
soit 2*8,93 10-3 *160 = 2,857 g de dibrome
C3H6 + Br2 --> C3H6Br2
soit (4-2,857) /160 = 7,14 10-3 mol de dibrome
7,14 10-3 mol de propène ou 7,14 10-3*22,4= 0,16 L ou 16%
propane: 1-0,2-0,16= 0,64 L ou 64%
|
|
corrigé
Par hydrogénation complète A donne du n-hexane.
A est soit un alcyne soit un composé possédant 2 double liaisons carbone carbone.
A conduit à B par addition d'une molécule d'eau : A est donc un alcyne et B une cétone.
L'oxydation de A donne l'acide propanoique : la triple liaison fait intervenir le 3ème atome de carbone.
A : hex-3-yne
|
|
|
|
|
|
|
|
corrigé
La fonction aldehyde est en bout de chaine : M est l'éthanal.
L est soit le butanal ou le 2-méthylpropanal. Or A conduisant par hydrogénation au n-hexane est linéaire ainsi que les produits qui en dérivent. L est donc le butanal.
G et K sont 2 alcènes isomères (isomèrie Z et E)
les produits de l'ozonolyse indiquent la position de la liaison double C=C; soit entre le 2ème et le 3ème carbone . G et H sont : hex-2-ène (Z et E).
La déshydratation d'un alcool donne un alcène. F est soit l'hexan-2-ol ou l'hexan-3-ol.
La réduction d'une cétone donne un alcool. E est soit l'hexan-2-one ou l'hexa-3-one.
L'addition d'eau à un alcyne donne un alcool. D est un alcyne. D réagit avec le sodium il s'agit d'un alcyne vrai . D est l' hex-1-yne.
E est l' hexan-2-one et F l' hexan-2-ol.
B est le 1,2-dibromohexane.
A est l' hex-1-ène.
réaction de substitution SN2. Elle permet un allongement de la chaîne carbonée.(obtention d'hex-1-yne à partir de l'éthyne)
C est l'hexan-2-one. le groupe carbonyle des aldehyde et cétone donne un précipité jaune avec la DNPH. les aldehydes réduisent la liqueur de Fehling. les cétones ne sont pas des réducteurs. |
A traité par le nitrate d'argent ammoniacal donne un précipité . L'oxydation d'une mole de A donne CO2 et l'acide propanoique.
B traité par le nitrate d'argent ammoniacal ne donne pas de précipité . L'oxydation d'une mole de A donne CO2 et l'acide oxalique.
Identifier A et B
corrigé
A et B sont des hydrocarbures insaturés : addition de Br2 dans CCl4
A est un alcyne vrai : action avec le nitrate d'argent ammoniacal.
B n'est pas un alcyne mais possède 2 doubles liaisons C=C (diène)
formule brute CnH2n-2. ; masse molaire M=14n-2
les réactions d'oxydation donnent les positions des liaisons multiples et le nombre de carbone .