Mathťmatiques,
Physique, chimie,
Concours TSPEI 2015.
|
En
poursuivant votre navigation sur ce site, vous acceptez l’utilisation
de Cookies vous proposant des publicitťs adaptťes ŗ vos centres
d’intťrÍts.
|
|
|
Exercice 1.
On considŤre la fonction dťfinie sur R par : f(x) = 2x 3-3x 2+1.
1. Calculer f(0) et f(1). Dťterminer les rťels a, b, c tels que, pour tout x rťel, on ait :
f(x) = (x-1)(ax 2+bx+c).
f(0) = 1 ; f(1) =0.
(x-1)(ax2+bx+c)=ax3 +bx2+cx-ax2-bx-c.
Par identification a = 2 ; b-2 =-3 soit b = -1 ; c = -1.
f(x) = (x-1)(2x2-x-1).
2. En dťduire l'ensemble des solution de f(x)=0.
x-1=0 soit x=1 ;
2x2-x-1 =0 ; D =(-1)2 -4(-1)x2 = 9
Solutions : x1 = (1+3)/4=1 et x2 = (1-3)/4=-0,5.
3. Calculer la dťrivťe de la fonction f et en dťduire le tableau de variations de f.
f '(x) = 6x2-6x = 6x(x-1).
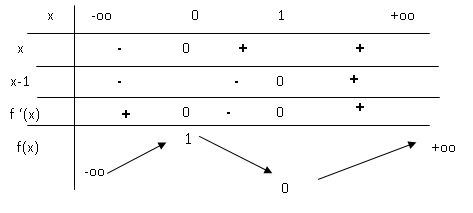
Soit (X) la courbe reprťsentative de f.
4. Dťterminer une ťquation de la tangente (T) ŗ la courne (X) au point d'abscisse x = -0,5.
f '(-0,5) = 4,5.
Equation de (T) : y = 4,5 x +b.
La tangente passe par le point de coordonnťes ( -0,5 ; f(-0,5) = 0 ).
Par suite 0 = 4,5(-0,5) +b ; b = 2,25.
y = 4,5 x +2.25.
5. Construire (X) et (T).
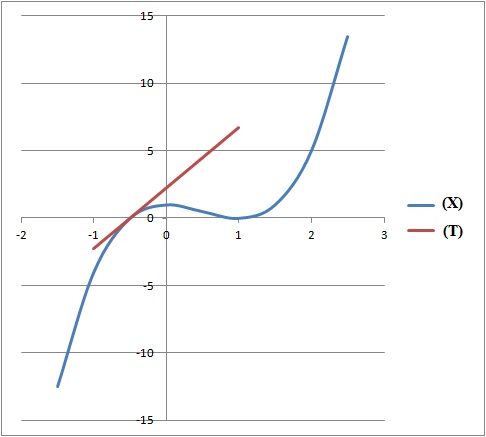
6. On se propose d'installer une rampe d'accŤs en pente douce permettant ŗ des chariots de franchir une marche.
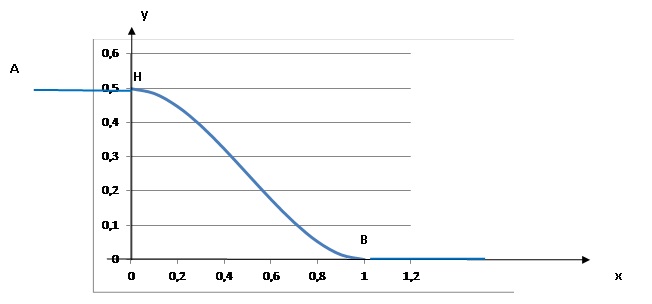
La courbe dťfinie par le profil de la rampe doit Ítre tangente en B ŗ
l'axe (Ox) et en H ŗ la droite (AH). Dťterminer les rťels a, b, c tels
que la courbe dťfinie par le profil ait pour ťquation
y = ax 3 +bx 2+c.
y' = 3ax 2 +2bx.
En H, tangente horizontale d'ťquation y = 0,5.
En B, tangente horizontale d'ťquation y = 0.
Par suite y'(1) = 3a+2b =0. (1).
La courbe passe en H(0 ; 0,5) : 0,5 = c.
La courbe passe en B(1 ; 0) ; 0 = a +b +0,5 soit b = -a-0,5.
Repport dans (1) : 3a-2a-1=0 soit a = 1 et b = -1,5.
y = x3-1,5x2+0,5.
|
| .
. |
....
...
|
Exercice 2.
Un
inspecteur est chargť de contrŰler trois unitťs de production notťes A,
B et C. Chaque mois il effectue un seul contrŰle dans une unitť choisie
au hasard parmi A, B et C. On admet que les choix sont ťquiprobables et
indťpendants. On considŤre une pťriode de 6 mois.
ContrŰles possibles au bout de 1 mois : A ; B ; C.
ContrŰles possibles au bout de 2 mois : AA, AB, AC, BB, BC, CC.
ContrŰles possibles au bout de 3 mois : AAA, AAB, AAC, ABC, BBB, ABB, BBC, CCC, ACC, BCC .
ContrŰles
possibles au bout de 4 mois : AAAA, AAAB, AAAC, AABB, AACC, AABC, ABCC,
ABBB, ABBC, BBBB, BBBC, BBCC, CCCC, ACCC, BCCC.
ContrŰles
possibles au bout de 5 mois : AAAAA, AAAAB, AAAAC, AAABC, AAACC, AAABB,
AABBB, AABBC, AABCC, AACCC, ABBBC, ABBCC, ABCCC, ABBBB, BBBBC, BBBCC,
BBCCC, ACCCC, BCCCC, CCCCC, BBBBB.
ContrŰles
possibles au bout de 6 mois : AAAAAA, AAAAAB, AAAAAC, AAAABB, AAAABC,
AAAACC, AAABBC, AAABCC, AAACCC, AAABBB, AABBBB, AABBBC, AABBCC, ABBBBC,
AABCCC, AACCCC, ACCCCC, ABBBCC, ABBCCC, ABCCCC, ABBBBC, ABBBBB, BBBBBC,
BBBBCC, BBBCCC, BBCCCC, ACCCCC, BCCCCC, CCCCCC, BBBBBB.
1. Quelle est la probabilitť que pendant cette pťriode seule l'unitť A soit contrŰlťe ?
probabilitť que seule A soit contrŰlťe : 1 / 30..
2. Quelle est la probabilitť que pendant cette pťriode une seule unitť soit contrŰlťe ?
3 cas favorables ( AAAAAA, BBBBBB, CCCCCC) sur 30.
Probabilitť qu'une seule unitť soit contrŰlťe : 3 / 30 = 1 / 10.
3. Quelle est la probabilitť que pendant cette pťriode au moins 2 unitťs soient contrŰlťe ?
2 ou trois unitťs doivent Ítre contrŰlťes ; on exclut le cas du contrŰle d'une seule unitť.
Probabilitť de contrŰler au moins deux unitťs :1- 1 / 10 = 9 /10.
4. Quelle est la probabilitť que pendant cette pťriode les 3 unitťs soient contrŰlťe ?
10 cas favorables sur 30 ; probabilitť que les 3 unitťs soient contrŰlťes : 1 /3.
On note XA la variable alťatoire ťgale au nombre de contrŰle ťffectuťs au sein de l'unitť A pendant la pťriode considťrťe.
5. Quelle est la loi de XA ? Donner son espťrance. Interprťter le rťssultat obtenu.
6 contrŰles
|
5 contrŰles
|
4 contrŰles
|
3 contrŰles
|
2 contrŰles
|
1 contrŰle
|
0 contrŰle
|
1
|
2
|
3
|
4
|
6
|
8
|
6
|
Moyenne : (6+10+12+12+12+8+0)/30 = 2.
L'unitť A est contrŰlťe en moyenne 2 fois tous les six mois
6. Quelle est la probabilitť que 2 contrŰles soient effectuťs au sein de A pendant la pťriode considťrťe ?
6 / 30= 1 /5.
|
|
|
Stockage de l'ťnergie .
Un
circuit ťlectrique comprend, en sťrie, un gťnťrateur idťal de tension
de fem E = 12,0 V, un conducteur ohmique de rťsistance R, un
condensateur de capacitť C = 120 ĶF et un interrupteur.
Le condensateur est initialement dťchargť et ŗ la date t=0, on ferme
l'interrupteur. On note q la charge de l'armature du condensateur qui
se charge positivement.
1. Reprťsenter par des flŤches les tension uc aux bornes du condensateur et uR aux bornes du conducteur ohmique.

2. Donner l'expression de uR en fonction de i.
uR = Ri..
3. Donner l'expression de i en fonction de la charge q.
i = dq/dt.
4. Donner la relation liant q et uc
q = CuC.
5. En dťduire l'expression de i en fonction de C et uC.
i = CduC /dt.
6. En appliquant l'additivitť des tensions, ťtablir une relation entre E, uR et uC.
E = uR + uC.
7. Etablir l'ťquation diffťrentielle ŗ laquelle obeit uC.
E =RC duC/dt + uC.
8. Rťsoudre cette ťquation.
Solution gťnťrale de l'ťquation sans second membre : uC =A exp(-t / (RC)), avec A une constante.
Solution particuliŤre de cette ťquation ( condensateur chargť) : uC=E
Solution gťnťrale : uC = E + A exp(-t/(RC)).
A t=0, uC = 0 , d'oý A = -E.
uC = E(1-exp(-t/(RC)).
9a. Vťrifier que t = RC est homogŤne ŗ un temps.
R rťsistance soit tension / intensitť ; C capacitť soit charge / tension d'oý on dťduit : RC charge / intensitť.
or une charge est une intensitť fois un temps ; par suite RC a la dimension d'un temps
9b. Dťterminer graphiquement t. En dťduire la valeur de R.
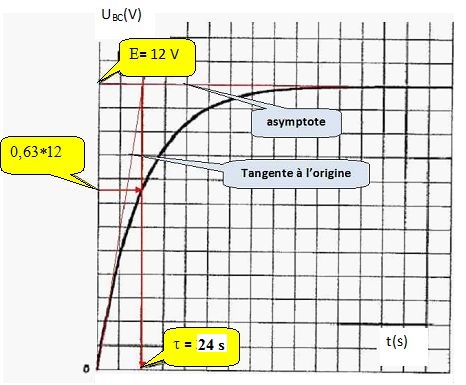
24 =120 10-6 R ; R =24 / (120 10-6) =2,00 105 ohms.
|
|
|
|
Satellites.
1. Rappeler la loi de gravitation universelle.
Deux corps A et B de masses respectives mA et mB sťparťs
d'une distance d exercent l'un sur l'autre des forces opposťes
attractives, importantes dans l'infiniment grand, nťgligeables dans
l'infiniment petit. Ces forces sont proportionnelles aux masses et
inversement proportionnelles au carrť de la distance d.
Satellite en orbite circulaire.
Un satellite de la terre ( masse M et rayon R), de masse m est en
orbite circulaire ŗ l'altitude h = 300 km au-dessus de la terre.
2. Applique la seconde loi de Newton au satellite et montrer qie son mouvement est uniforme.
Le satellite est soumis
ŗ la seule force de gravitation centripŤte
exercťe par la planŤte
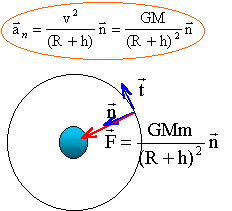
M : masse (kg) de la planŤte ; m : masse du
satellite (kg) ; R (m) rayon planŤte ; h (m) altitude
depuis le sol.
La force de gravitation est toujours perpendiculaire
ŗ la vitesse ; cette force ne travaillant pas, elle
ne modifie pas la valeur de la vitesse : le mouvement est
donc uniforme.
3. Dťterminer l'expression de la vitesse en fonction de r = R+h, G et M.
Suivant l'axe n la
seconde loi de Newton s'ťcrit : GMm /(R+h)2 = m
aN= mv2/ (R+h)
d'oý la valeur de la vitesse (m/s):
v2 =GM /
(R+h)
=GM / r.
indťpendante de la masse du satellite
4. Les
satellitse de type SPOT ťvoluent sur des orbites circulaires d'altitude
830 km environ. Leur vitesse est-elle plus grande, plus petite ou ťgale
ŗ celle du satellite prťcťdent ? Justifier
La vitesse diminue quand r= R+h augmente. SPOT a une vitesse infťrieure ŗ celle du satellite ťtudiť ici
5. Exprimer la pťriode du satellite en fonction de G, R, h et M.
Le satellite dťcrit la circonfťrence 2p(R+h) ŗ la vitesse v en T seconde.
2p(R+h) = vT ;
ťlever au carrť : 4p2(R+h)2 = v2 T2 =GM /(R+h) T2.
T =2p/ (GM)Ĺ (R+h)1,5.
6. Montrer que la troisiŤme loi de Kepler est vťrifiťe.
T2= 4p2(R+h)3 / (GM).
Le carrť de la pťriode est proportionnel au cube du rayon de l'orbite.
7. Prťciser ce qu'est un satellite gťostationnaire. Le satellite ťtudiť est-il gťostationnaire ?
Un satellite gťostationnaire tourne dans le plan ťquatorial, dans le
mÍme sens que la terre, avec la mÍme vitesse angulaire que la terre.
Son altitude est proche de 36000 km.
Le satellite ťtudiť n'est pas gťostationnaire.
|
Fission nuclťaire.
1. Donner la dťfinition de la fission nuclťaire.
Fission nuclťaire spontanťe : le noyau se dťsintŤgre en plusieurs fragments sans absorption prťalable d'un corpuscule ( neutron par exemple).
Fission nuclťaire induite : un noyau lourd capture un neutron puis se dťsintŤgre en plusieurs fragments.
2. Des rťactions de fission sont induites par la capture d'un neutron et s'ťcrivent : 23592U + 10n ---> 94ZSr + A54Xe + x 10n
Quel phťnomŤne se produit si x >2 ?
La rťaction produit plus de neutrons qu'elle n'en consomme. Un rťaction en chaine se produit
3. Pour x = 3, dťterminer A et Z.
Conservation du nombre de nuclťons :235+1=94+A+3 ; A =139.
Conservation de la charge : 92 = 54 +Z ; Z =38.
4a. Enoncer la relation d'ťquivalence masse - ťnergie.
Einstein postule que la masse est une des formes que peut prendre
l'ťnergie. Un systŤme de masse m possŤde lorsqu'il est au repos, une
ťnergie: E = m.c2
E: ťnergie du systŤme en joules (J) ; m: masse du systŤme en kilogrammes (kg) ; c: vitesse de la lumiŤre dans le vide (c=3,0.108m.s-1.
4 b.Exprimer
en fonction des masses des particules et des noyaux intervenant dans
l'ťquation prťcťdente, la variation d'ťnergie de masse DE au cours de cette rťaction nuclťaire.
Variation de masse Dm =2 m(10n) + m(113954Xe) + m( 9438Sr) - m(23592U).
Dm = 2*1,0087 +138,888 2 +93,894 6-235,013 4= -0,2132 u.
-0,2132*1,660 10-27 = -3,539 12 10-28 kg.
Cette diminution de masse s'acompagne de la libťration d'ťnergie dans le milieu extťrieur ( ce que traduit le signe nťgatif) :
Dm c2 = -3,539 12 10-28 *(2,998 108)2 = -3,18096 10-11 J ~ -3,181,0 10-11 J.
-3,1810 10-11 / 1,602 10-13 = 1,985 6 102 MeV
Prťparation industrielle du zinc.
Dans
la nature, le zinc (Zn) se rencontre dans la blende, minerai constituť
essentiellement de sulfure de zinc solide ZnS(s). Pour rťcupťrer le
mťtal zinc, dont la principale application est l'ťlaboration de l'acier
zinguť, la blende subit des transformations physico-chimiques.
La
blende est transformťe en calcine ( constituťe principalement de ZnO)
au moyen d'une opťration appelť grillage. La calcine est alors traitťe
par hydromťtallurgie pour obtenir le mťtal zinc quasiment pur.
Le grillage est effectuť en chauffant fortement le sulfure de zinc en
prťsence du dioxygŤne de l'air. L'ťquation de la rťaction associťe ŗ la
transformation est :
.... ZnS(s) + ....O2(g) =....ZnO (s) +.... SO2(g).
1.a Ajuster les nombres stoechiomťtriques.
2 ZnS(s) + 3O2(g) = 2ZnO (s) +2 SO2(g).
1.b. On grille une masse m = 1,00 t de sulfure de zinc. Dťterminer la masse m2 d'oxyde de zinc obtenue et le volume V de dioxygŤne nťcessaire.
M(Zn) = 65,4 g /mol ; M(O = 16 g/mol ; M(S) = 32,1 g /mol. Vm = 25,0 L /mol.
Quantitť de matiŤre de sulfure de zinc : n = 1,00 106 /(65,4 +32,1) =1,02564 104 mol.
Quantitť de matiŤre d'oxyde de zinc :1,02564 104 mol.
m2 = 1,02564 104. x(65,4 +16) =8,35 105 g = 0,835 t.
Quantitť de matiŤre de dioxygŤne :1,5x1,02564 104 = 1,5385 104 mol.
V = 1,5385 104 x25,0 =3,85 105 L.
2. a. Ecrire l'ťquation de rťduction de l'oxyde de zinc par le carbone. On obtient du monoxyde de carbone et du zinc.
ZnO(s) + C(s) ---> Zn(s) + CO(g).
2.b. Dťterminer la masse m3 de zinc obtenue.
Quantitť de matiŤre de ZnO = quantitť de matiŤre de zinc = 1,02564 104 mol.
m3 = 65,4 x1,02564 104 ~6,71 105 g.
3. . En rťalitť, le rendement de chaque opťration successive ne dťpasse jamais 80 %.
Quelle masse m4 de zinc fabrique t-on par tonne de minerai ?
m4 = 0,80 x0,80 m3 = 0,80 x0,80 x6,71 105 =4,30 105 g = 0,430 kg.
4. Quelle masse m5 de carbone est nťcessaire ŗ la prťparation du zinc ?
Quantitť de matiŤre de carbone = quantitť de matiŤre de ZnO =1,02564 104 mol.
Tenir compte du rendement de la premiŤre rťaction : 1,02564 104 x0,80 =8,205 103 mol.
Masse de carbone : 12 x8,205 103 ~9,85 104 g.
Dosage des ions nitrate par spectrophotomťtrie.
La teneur en ion nitrate dans les eaux potables doit Ítre infťrieur ŗ 50 mg / L.
Les ions nitrate sont rťduits en ion nitrite puis traitťs par un
rťactif de diazotation pour obtenir un composť diazoÔque de couleur
rose dont on peut mesurer l'absorbance.
Une solution ťtalon d'ion nitrate de concentration massique Cm
= 20,00 mg /L et de volume V = 200 mL subit le traitement ci-dessus et
permet de prťparer une sťrie de fioles jaugťes de 100,0 mL notťes 0, 1,
2, 3, 4 selon les mťlanges indiquťs dans le tableau ci-dessous.
Fiole
|
0
|
1
|
2
|
3
|
4
|
X
|
Volume de solution rťduite (mL)
|
0,00
|
2,00
|
4,00
|
6,00
|
8,00
|
5,00
|
Rťactif de diazotation (mL)
|
1 |
Concentration massique ( mg/L)
|
0,00
|
2,00 /100 x20,00 =0,400
|
0,800
|
1,20
|
1,6
|
xxxxxx
|
Absorbance
|
0,00
|
0,251
|
0,524
|
0,782
|
1,031
|
0,657
|
On
complŤte chacune des fioles jaugťes ŗ 100,0 mL avec de l'eau distillťe.
AprŤs 15 minutes d'attente, une partie de la solution est transfťrťe
dans une cuve de longueur L=1,00 cm qui est placťe dans le
spectrophotomŤtre. Longueur d'onde de travail l = 540 nm.
1. Comment la longueur d'onde doit-elle est choisie pour cette mesure ?
Pour une meilleure prťcision, la longueur d'onde de travail doit correspondre au maximum d'absorption de la solution.
2. La solution ťtalon a ťtť prťparťe ŗ partir de nitrate de potassium KNO3.
2.a. Dťterminer la masse m de nitrate de potassium nťcessaire pour prťparer la solution ťtalon.
M(KNO3) = 39,1 +14 +3x16 = 101,1 g/mol. M(NO3-) = 14+3x16=62 g/mol.
Quantitť de matiŤre d'ion nitrate : 20,00 / 62 mmol.
Quantitť de matire de nitrate de potassium : 20,00 / 62 mmol.
Masse de nitrate de potassium = 20,00 / 62 x101,1 = 32,61 mg.
2.b. Proposer un mode opťratoire pour cette prťparation.
Peser ŗ la balance de prťcision 32,61 mg de nitrate de potassium.
Dissoudre dans 100 mL d'eau distillťe et verser dans une fiole jaugťe de 1,00 L.
Complťter avec de l'eau distillťe jusqu'au trait de jauge. Boucher et agiter pour rendre homogŤne.
3. Complťter l'avant derniŤre ligne du tableau.
4.a Rappeler la loi de Beer-Lambert.
La relation fondamentale utilisťe en spectrophotomťtrie est prťsentťe sous la forme :
A= log (I0/I) = elc ( A est l'absorbance ou densitť optique)
e est une caractťristique de la molťcule. Plus e sera grand, plus la solution absorbe.
Absorbance et concentration ťtant proportionnelles, cette relation peut
Ítre utilisťe pour rťaliser des dosages ou des suivis cinťtiques.
4.b.Tracer le graphe A = f(C). La loi de beer est-elle vťrifiťe ?
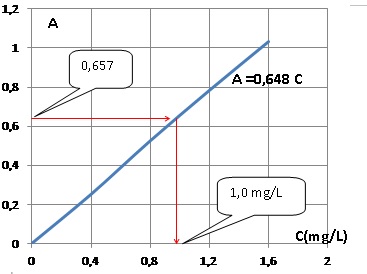
La courbe est une droite passant par l'origine : la loi de Beer est vťrifiťe.
5. Un ťchantillon d'eau de ville est traitť de la mÍme maniŤre que la solution ťtalon. Dťterminer la concentration massique Cx en ion nitrate dans l'eau de ville. Cette eau est-elle potable pour les ions nitrate ?
Le graphe indique 1,0 mg/L ; tenir compte de la dilution 100 / 5 = 20 ; Cx = 20 mg/L, valeur infťrieure ŗ 50. L'eau est potable pour les ions nitrate.
Les alcools.
La molťcule A a pour formule semi-dťveloppťe : CH3-CH(OH) CH2-CH3.
1. a. Citer le nom du groupe caractťristique prťsent. Groupe hydroxyle OH.
1.b. Nommer A. Butan-2-ol.
1.c Donner les reprťsentation spatiales des deux isomŤres du composť A. Quel nom donne-t-on ŗ cette relation d'isomťrie ?
Donner la configuration absolue de l'atome de carbone asymťtrique.
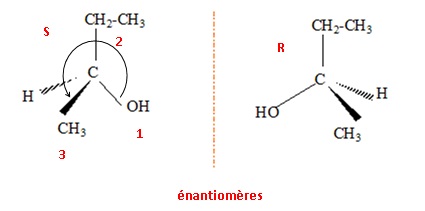
numťroter de faÁon dťcroissante
chacun des quatre substituants selon son numťro
atomique.
OH (1) ; CH2CH3 (2) ; CH3 (3) ; H
(4).
On place alors l'atome (ou le groupement) de
numťro le plus ťlevť
derriŤre.
On regarde dans quel sens, sens horaire ou
trigonomťtrique, on passe du numťro 1, au 2,
au 3.
- Si le sens de rotation est le sens horaire (ou
anti-trigonomťtrique), le carbone est Rectus (R),
- Si le sens de rotation est le sens
trigonomťtrique (ou anti-horaire), le carbone est
Sinister (S).
2. On envisage la rťaction d'oxydo-rťduction suivante :
A --> C4H8O, ( notť B, cťtone ) en prťsence de KMnO4 acidifiť (1).
2.a. Nommer B et donner sa formule semi-dťveloppťe.
Butan-2-one. CH3-C=O CH2-CH3.
2.b. Ecrire les demi-ťquations ťlectroniques mises en jeu et en dťduire l'ťquation de la rťaction.
2 fois { MnO4- + 8H++5 e- = Mn2+ + 4H2O } rťduction
5 fois { CH3-CH2-CH(OH)-CH3 = CH3-CH2-CO-CH3 + 2H+ + 2 e- } oxydation.
2MnO4- + 5CH3-CH2-CH(OH)-CH3 + 6H+ =5 CH3-CH2-CO-CH3 +2 Mn2+ +8H2O
3. On chauffe A en milieu acide et on obtient C ( C4H8).
A ---> C +H2O (2)
3.a Cette rťaction est-elle une addition, une substitution ou une ťlimination ? Justifier.
Elimination d'une molťcule d'eau ŗ partir d'un alcool. Une liaison double C= C est formťe.
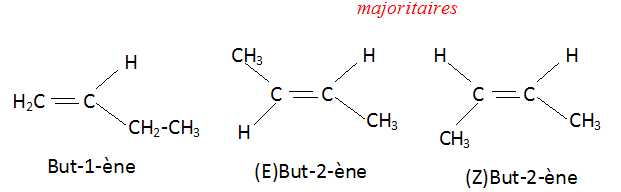
3.b. Donner les formules semi-dťveloppťes des deux isomŤres de position C1 et C2 de C. Quel est celui qui est majoritaire ?
L'alcŤne le plus substituť se forme majoritairement.
|
|