|
chimie
organique
le craquage ; test à
l'eau de brome ; solvants
chlorés ; C3H6O
; stéarine ;
glucose ; urée
; alcane; oxydation ménagée des
alcools ; isomères
En poursuivant votre navigation sur ce site, vous acceptez l’utilisation de Cookies vous proposant des publicités adaptées à vos centres d’intérêts.
|
|
|
|
A)
Un alcène a une masse
molaire de 56 g/mol.
1) Donner sa formule chimique brute.
Formule générale d'un alcène CnH2n.
Masse molaire M = 12 n +2 n = 14 n ; par suite n = 56 /14 = 4.
C4H8.
2) Est-ce que c’est un hydrocarbure saturé ?
Un hydrocarbure saturé ne possède que des liaisons simples entre deux atomes de carbone.
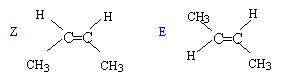
3) Donner ses formules développées ainsi que leurs noms.
CH2=CH-CH2-CH3
but-1-ène ; CH3CH=CH-CH3 deux isomères Z et E du
but-2-ène
(CH3)2C=CH2
; 2-méthylpropène
B)
On brule cet
alcène avec l’oxygène dans une combustion complète.
1) Ecrire la réaction chimique qui se déroule.
2) équilibrer la réaction.
C 4H 8(g) + 6O 2(g) --> 4CO 2(g) +4H 2O(g).
3) si on brule 11,2 g
de cet alcène :
- déterminer la quantité de l'alcène brulé.
n = m / M = 11,2 / 56 = 0,2 mol.
- déterminer la masse de H 2O formée.
n(eau) = 4 x0,2 = 0,8 mol ; M(eau) = 18 g / mol ; 18 x0,8 =14,4 g.
- déterminer le volume de CO 2 formé.
n(CO 2) = 4 x0,2 = 0,8 mol ; volume molaire 24 L / mol ; 24 x0,8 = 19,2 L.
C)
On hydrate cet
alcène en rajoutant de l’eau en présence d’un catalyseur.
1) Ecrire la réaction chimique qui se déroule.
C4H8 + H2O --> C4H10O.
2) Quel est le type de réaction qui se déroule (substitution
ou addition) ? Expliquer.
Addition d'une molécule d'eau sur la liaison double C=C.
3) A quelle famille chimique, appartient le composé formé ?
Alcool.
4) si on fait réagir
11,2 g de cet alcène :
- déterminer la quantité de l'alcène mise en jeu.
n = m / M = 11,2 / 56 =0,2 mol.
- déterminer la masse de H2O nécessaire.
n(eau = 0,2 mol ; M(eau) = 18 g / mol ; m(eau) = 0,2 x18 =3,6 g.
- déterminer la masse du composé organique formé.
M(alcool) = 56+18=74 g / mol.
n(alcool) = 0,2 mol ; masse : 0,2 x74 =14,8 g.
|
|
|
Le craquage :
Par craquage du cyclooctane C8H16,
on obtient uniquement un composé non cyclique de formule C4H8.
- Ecrire l'équation chimique du
craquage réalisé.
- Donner tous les isomères de
constitution du produit de craquage.
- Parmi ces isomères, quels sont ceux
qui présentent une isomérie Z/E ? Les dessiner en faisant apparaître
cette isomérie.
corrigé
|
|
C8H16
--> 2 C4H8.
CH2=CH-CH2-CH3
but-1-ène ; CH3CH=CH-CH3 deux isomères Z et E du
but-2-ène
(CH3)2C=CH2
; 2-méthylpropène

|
|
Test à l'eau de brome :
Afin de déterminer la formule brute d'un alcène X, on mesure
la quantité de dibrome consommée par réaction d'addition. On observe
que 2,1 g d'alcène décolorent complètement une solution contenant 8,0 g
de dibrome.
- Donner la formule générale d'un alcène.
- Ecrire l'équation associée à la réaction d'addition.
- La transformation a lieu dans des proportions
stoechiométriques. En déduire la quantité de matière d'alcène
introduit, puis sa masse molaire.
- Donner la formule brute de X.
Données : M(Br2)= 160.0 g.mol-1; M(C) =
12.0 g.mol-1; M(H)= 1.0 g.mol-1.
corrigé
CnH2n.
CnH2n + Br2 --> CnH2nBr2
( dibromoalcane)
Qté matière Br2 : 8/ 160 = 0,05 mol
donc 0,05 mol alcène de masse molaire 12 n + 2n = 14 n
Qté de matière (mol) = masse (g) / masse molaire (g/mol)
0,05 = 2,1 / (14n) soit n = 3
C3H6 soit CH3-CH=CH2.(propène).
|
|
Solvants chlorés :
Le tableau ci dessous rassemble des
données concernant quelques solvants chlorés.
|
Solvant
|
Formule
|
Température d'ébullition
sous 1 bar (°C)
|
Production européenne en
1991 (t)
|
|
Chlorométhane
|
CH3Cl
|
- 24
|
220 000
|
|
dichlorométhane
|
CH2Cl2
|
40,1
|
234 000
|
|
trichlorométhane
|
CHCl3
|
61
|
220 000
|
|
tétrachlorométhane
|
CCl4
|
76
|
250 000
|
|
1,1,2-trichloroéthylène
|
Cl2C=CHCl
|
86,7
|
125 000
|
|
1,1,2,2-tétrachloroéthylène
|
Cl2C=CCl2
|
121,2
|
210 000
|
|
1,1,1-trichloroéthane
|
H3C - CCl3
|
73,8
|
198 000
|
- Donner l'état physique des solvants
du tableau à 25°C et sous 1 bar.
- Le 1,1,2,2-tétrachloroéthylène peu
être fabriqué par craquage d'un mélange de 1,1,2,2-tétrachloroéthane Cl2HC
- CHCl2 et de 1,1,1,2,2-pentachloroéthane Cl3C -
CHCl2. Compléter les équations suivantes :
Cl2HC - CHCl2 --> Cl2C = CCl2
……
Cl3C - CHCl2 --> Cl2C = CCl2
…….
- Le chlorométhane CH3Cl
gazeux est synthétisé à 150 °C par action du chlorure d'hydrogène
gazeux sur le méthanol CH3OH gazeux, en présence d'alumine, qui sert de
catalyseur. L'excès de chlorure d'hydrogène est éliminé par passage
dans une solution aqueuse d'hydroxyde de sodium. Le chlorométhane est
ensuite séché avec de l'acide sulfurique H2SO4,
puis comprimé et liquéfié.
- Ecrire l'équation chimique de la transformation du méthanol en
chlorométhane.
- Par quel type de réaction de chlorure d'hydrogène en excès est-il
éliminé ? Ecrire l'équation chimique de cette transformation.
- Calculer la quantité de matière de méthanol nécessaire à la
production européenne de chlorométhane.
- Calculer en m3, le volume occupé par le chlorométhane
formé s'il est stocké à 25°C, sous 1 bar.
Données : M (CH3OH) = 32,0
g.mol-1.M (CH3Cl) = 50,5 g.mol-1.Volume
molaire à 25°C sous 1 bar : Vm = 24,0 L.mol-1.
corrigé
Gaz pour le chlorométhane ; liquide pour
les autres à 25 °C sous 1 bar.
Cl2HC - CHCl2
--> Cl2C = CCl2 + H2.
Cl3C - CHCl2
--> Cl2C = CCl2+ HCl
CH3OH + HCl --> CH3Cl +
H2O
Réaction acide base H3O+
+ HO- --> 2H2O
220 000 t = 2,2 1011 grammes
Qté de matière (mol) = masse (g) / masse
molaire (g/mol)
2,2 1011 / 35,5+12+3) = 4,36
109 mol
masse de méthanol (g) = masse molaire
(g/mol) * Qté de matière (mol)
(12+4+16)* 4,36 109 =1,39 1011
g = 139 000 t.
volume chlorométhane (L) = Qté matière
(mol) fois volume molaire (L/mol)
4,36 109 *24 = 1,05 1011
L = 1,05 108 m3.
|
|
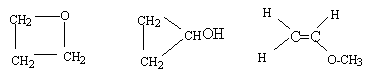
- A partir de la formule brute C3H6O,
combien peut-on construire de molécules ? On utilisera les règles de
l'octet et du duet pour déterminer les formules semi développées.
- Donner la géométrie autour de chaque atome de carbone.
corrigé
CH3-CH2-CHO propanal ( aldehyde)
CH3-CO-CH3 acétone ou propanone (
cétone)
CH2=CH-CH2OH ;
CHOH=CH-CH3 ( instable) ; CH2=C(OH)-CH3
(instable)
d'autres molécules :
carbone tétragonal ( lié à 4 groupes d'atomes) :
le carbone est au centre d'un tétraèdre et les quatre liaisons
sont dirigées vers les sommets du tétraèdre
carbone trigonal ( lié à 3 groupes d'atomes) : structure
triangle plan ( angles proches de 120°)
|
|
La stéarine, constituant de base des bougies, est une espèce
chimique organique de formule brute C57 H 110 O6
.
- Déterminer la masse molaire de la stéarine.
- Déterminer les pourcentages en masse de chaque élément dans
ce composé.
masse atomique molaire C=12 ; O=16 ; H=1 g/mol
corrigé
masse molaire de la stéarine : 57*12 + 110 + 6*16 = 890 g/mol
57*12*100 / 890 = 76,85 % de carbone
110 *100 / 890= 12,36% d'hydrogène
et 16*6 *100 /890 = 10,78 % d'oxygène.
|
|
- Le glucose est
un sucre contenant l'élément carbone, l'élément hydrogène et l'élément
oxygène. Une analyse centésimale conduit aux pourcentages en masse
suivants : %C : 40,0 ; %H : 6,7 ; %O : 53,3.Sachant que la masse
molaire du glucose est de 180 g/mol, déterminer la formule brute du
glucose.
- La
photosynthèse est à la base de la fabrication naturelle de composés
organiques appelés glucides. La transformation peut-être modélisée
ainsi : le dioxyde de carbone réagit avec l'eau pour donner un glucide
et du dioxygène. Le glucose, est un exemple de glucide. En écrivant la
formule du glucose sous une autre forme, justifier l'ancienne
dénomination des glucides : " hydrates de carbone ".
- Que signifie
le terme photosynthèse ?
- Ecrire l'équation chimique de la réaction de photosynthèse.
- Quelle quantité de matière de dioxyde de carbone est nécessaire pour
synthétiser 0,30 mg de glucose ?
corrigé
glucose CxHyOz
masse molaire : 12 x+ y +16 z = 180
12 x /180 = 0,4 --> x = 6
y/180 = 0,067 --> y = 12
16 z / 180 = 0,533 --> z = 6
(C H2O) 6
synthèse utilisant l'énergie solaire: la lumière apporte
l'énergie nécessaire à la synthèse.
6 CO2 + 6H2O --> C6 H12
O6 + 6 O2.
3 10-4 / 180 = 1,66 10-6 mol glucose
soit 6*1,66 10-6 = 10-5 mol CO2.
multiplier par la masse molaire CO2 : 44 10-5
= 0,44 mg.
|
|
L'urée fut la
première molécule organique synthétisée. Sa masse molaire est de 60
g/mol. Une analyse centésimale permet de déterminer les pourcentages en
masse des éléments constitutifs : %C : 20, 0 ; %O : 26,7 ; %H : 6,7 ;
%N : 46,6.
- Déterminer la
formule brute de l'urée.
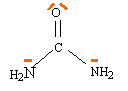
- Donner sa
formule de Lewis, sachant que le carbone présente une double liaison
avec l'atome d'oxygène, que les deux atomes d'azote ne sont pas liés
entre eux et qu'ils ne sont pas engagés dans une double liaison.
corrigé
urée CxHyOzN t
masse molaire : 12 x+ y +16 z+ 14 t = 60
12 x /60= 0,2--> x = 1
y/60 = 0,067 --> y = 4
16 z / 60 = 0,267--> z = 1
14t / 60 = 0,464 --> t = 2
H2N- CO-NH2
|
|
L'analyse
élémentaire d'une espèce chimique organique s'effectue par la
combustion dans le dioxygène. Le carbone et l'hydrogène qu'elle
contient se combinent avec l'oxygène pour former du dioxyde de carbone
et de l'eau. La mesure des quantités de CO2 et de H2O
formées permet de déterminer la formule brute de l'espèce.
Une espèce
chimique organique gazeuse a pour formule brute CuHv
. On réalise la combustion de 10 mL de cette espèce dans une quantité
suffisante de dioxygène. On obtient 30 mL de dioxyde de carbone et 40
mL d'eau (gaz) dans les mêmes conditions de température et de pression.
- Sachant que le
volume molaire est de 25 L/mol dans les conditions de l'expérience,
déterminer la quantité de matière de chacun des produits formés.
- Ecrire
l'équation de la réaction.
- Quel est
l'avancement maximal ?
- Déterminer u,
v et en déduire la formule brute de l'espèce chimique étudiée.
corrigé
CuHv
+ (u +0,25 v)O2 --> u CO2 + ½ v H2O
Qté de matière des gaz ( mol) = volume du gaz (L) / volume
molaire (L/mol)
0,01 / 25 = 0,4 mmol CuHv.
0,03 /25 = 1,2 mmol CO2 donc u = 3
eau gaz : 0,04/ 25 = 1,6 mmol donc v = 8
C3H8 : propane
CH3-CH2-CH3.
avancement maxi : 0,4 mmol (ni excès , ni défaut de réactifs
d'après le texte)
|
|
Choisir la ou les bonnes réponses
:
- L'oxydation du propan-1-ol par des ions permanganate en
milieu acide peut conduire à : la propanone ; l'acide propanoïque ; le
propanal ; le propène
- Écrire la (les) équation(s) chimique(s) correspondante(s).
- Comment peut-on le vérifier expérimentalement ?
- L'oxydation du propan-2-ol par des ions permanganate en
milieu acide peut conduire à : la propanone ; l'acide popanoïque ; le
propanal ; le propène
- Écrire la (les) équation(s) chimique(s) correspondante(s).Comment
peut-on le vérifier expérimentalement ?
- La déshydratation du butan-1-ol conduit au : butanal ;
but-1-ène ; but-2-ène ; 2-méthylprop-1-ène
- Justifier en écrivant l'équation chimique faisant apparaître les
formules semi-développées des réactifs et produits.
- On verse à température modérée quelques gouttes de solution
de permanganate de potassium acidifié dans un bécher contenant 20 mL de
composé A. La solution reste rose violacé. Parmi les composés suivants,
lesquels pourraient être A ? Justifier. méthanal ; pentan-3-one ;
2-méthyl propan-2-ol ; butan-2-ol
corrigé
Un alcool primaire, le propan-1-ol, conduit par
oxydation ménagée à un aldehyde, le propanal, puis à un acide
carboxylique, l'acide propanoïque : on observe alors la décoloration de
la solution de permanganate ( passage du violet à l'incolore)
MnO4-
+ 8H+ + 5e- = Mn2+ + 4H2O (1) réduction
C3H8O
= C3H6O + 2H+ + 2e- (2) oxydation de l'alcool en
aldehyde
faire l'addition
2 fois (1) + 5 fois (2)
2MnO4-
+ 6H+ + 5C3H8O = 5C3H6O
+ 2Mn2+ + 8H2O oxydo-réduction
C3H8O
+H2O= C3H6O + 4H+ + 4e-
(3) oxydation de l'alcool en
acide carboxylique
faire l'addition
4 fois (1) + 5 fois (2)
4MnO4-
+ 12H+ + 5C3H8O = 5C3H6O
+ 4Mn2+ + 11H2O oxydo-réduction
Un alcool secondaire, le propan-2-ol, conduit
par oxydation ménagée à une cétone, la propanone : on observe alors la
décoloration de la solution de permanganate ( passage du violet à
l'incolore)
MnO4-
+ 8H+ + 5e- = Mn2+ + 4H2O (1) réduction
C3H8O
= C3H6O + 2H+ + 2e- (2) oxydation de l'alcool en
cétone CH3-CO-CH3.
faire l'addition
2 fois (1) + 5 fois (2)
2MnO4-
+ 6H+ + 5C3H8O = 5C3H6O
+ 2Mn2+ + 8H2O oxydo-réduction
déshydratation du
butan-1-ol conduit à un alcène : le
but-1ène
CH3-CH2-CH2-CH2OH
--> CH3-CH2-CH=CH2 + H2O
On verse à température modérée quelques gouttes de solution de
permanganate de potassium acidifié dans un bécher contenant 20 mL de
composé A. La solution reste rose violacé: il n'y a pas de réaction
d'oxydo-réduction ( le permanganate est en défaut)
le méthanal serait oxydé en acide méthanoïque
la pentan-3-one, une cétone ne
subit pas d'oxydation ménagée
2-méthyl propan-2-ol : alcool
tertiaire ; il ne subit pas d'oxydation ménagée.
butan-2-ol, alcool secondaire serait oxydé en cétone.
|
|
alcool, aldehyde, cétone, acide
carboxylique :
- Quelle est la formule brute des alcools dont la chaîne
carbonée saturée comporte quatre atomes de carbone ?
- Donner la formule semi-développée, le nom et la classe des
quatre isomères possibles.
- Trois flacons A, B et C ne comportant pas d'étiquette,
contiennent respectivement trois de ces alcools. Dans trois tubes à
essai contenant respectivement 2 mL de solution A, B et C, on verse
quelques gouttes d'une solution de permanganate de potassium acidifiée.
- On observe une décoloration dans les tubes A et C. Que peut-on en
conclure ?
- Les composés A' et C' formés précédemment sont testés avec la liqueur
de Fehling. Décrire ce test (mode opératoire, observations).
- Ce test est négatif avec A', mais positif avec C'. Que peut-on en
déduire ?
- C' est un composé linéaire. Qui est C ? Associer à A et B la formule
d'un isomère en accord avec les observations expérimentales. Justifier
les choix.
corrigé
formule brute des
alcools dont la chaîne carbonée saturée comporte quatre atomes de
carbone : C4H10O
CH3-CH2-CH2-CH2OH
: butan-1-ol, alcool primaire
CH3-CH2-CHOH-CH3 :
butan-2-ol, alcool secondaire
CH3-CH(CH3)-CH2OH :
2-méthylpropan-1-ol, alcool primaire
CH3-COH(CH3)-CH3 :
2-méthylpropan-2-ol, alcool tertiaire
A et C : alcool primaire ou secondaire. B alcool tertiaire :
2-méthylpropan-2-ol
test à la liqueur de Fehling : en présence d'un
aldehyde réducteur, à chaud, on observe un précipité rouge brique
d'oxyde de cuivre (I) Cu2O.
test négatif avec A' : A' est une cétone CH3-CH2-CO-CH3
et A est : CH3-CH2-CHOH-CH3
test positif avec C' : C' est un aldehyde à chaîne linéaie CH3-CH2-CH2-CHO
donc C est : CH3-CH2-CH2-CH2OH
|
|
L
La molécule ci-contre est la phéromone d'alarme des fourmis du
Texas.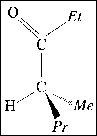
Les symboles Me, Et et Pr désignent respectivement les groupes
méthyl -CH3, éthyl -C2H5 et propyl -C3H7.
- Écrire la formule semi-développée et déterminer la formule
brute de cette molécule.
- A quelle famille appartient-elle ? Comment nomme-t-on le
groupe fonctionnel présent ?
- Parmi les isomères de constitution d'une molécule, on
distingue :
- Les isomères de chaîne ne différant que par l'enchaînement des atomes
de carbone.
- Les isomères de position ne différant que par la place de
l'implantation d'un même groupe fonctionnel.
- Les isomères de fonction différant par la nature du groupe
fonctionnel présent dans leur molécule.
Proposer pour cette molécule, la formule semi-développée d'un isomère
a) de chaîne ; b) de position ; c) de fonction.
Sachant que les préfixes caractérisant les chaînes carbonées à 6, 7, 8
et 9 atomes de carbone sont respectivement hex-, hept-, oct- et non- ,
nommer chaque isomère proposé.
corrigé
CH3-CH2-CH2-CH(CH3)-CO-CH2-CH3
: 4-méthylheptan-3-one C8 H16O.
Il s'agit d'une cétone: le groupe carbonyle >C=O ne se
trouve pas en bout de chaîne.
un isomère de chaîne : CH3-CH2-CH2-CH2-CH2-CO-CH2-CH3
:octan-3-one
un isomère de position :CH3-CH2-CH2-CH(CH3)-CH2-CO-CH3
: 4-méthylheptan-2-one
un isomère de fonction : CH3-CH2-CH2-CH(CH3)-CH(OH)-CH=CH2
: 4-méthylhept-1-ène-3-ol
|
|
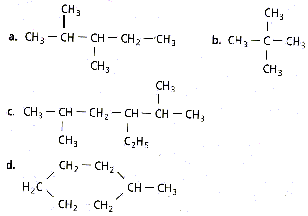
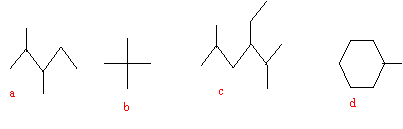
- Nommer les composés ci-dessus et donner l'écriture
topologique de ces quatre hydrocarbures.
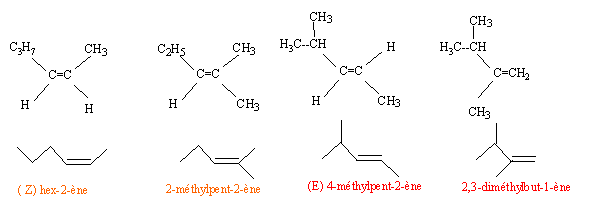
- Donner la formule semi-développée et l'écriture topologique
des alcènes suivants : ( Z) hex-2-ène ; 2-méthylpent-2-ène (E)
4-méthylpent-2-ène ; 2,3-diméthylbut-1-ène.
corrigé
a :
2,3-diméthylpentane ; b: 2,2-diméthylpropane ; c :
3-éthyl-2,5-diméhtylhexane; d : méthylcyclohexane
|
|
On considère un composé organique de formule CxHyO ; la
composition centésimale massique de ce composé est : c : 64,9 % et O :
21,6 %.
- Déterminer la formule brute du composé étudié.
- Donner les différents isomères en précisant la nature des
isomères.
- On réalise la combustion de V= 250 mL de CyHyO dans un
excès de dioxygène ; le sproduits obtenus sont l'eau et le dioxyde de
carbone.
- Ecrire l'équation bilan de la réaction.
- Dresser le tableau d'avancement.
- Déterminer le volume de CO2 obtenu et la masse d'eau
formée.
Masse volumique du composé : r=
0,785 g/mL ; Vm = 25,0 L/mol.
corrigé
On note M la masse
molaire : M= 12 x + y + 16 g/mol
12 x / %C = y / %H = 16 / %O= M/100
%H = 100 - %C - %O= 100-64,9-21,6 =13,5 %
12 x / 64,9 = y/ 13,5 = 16 / 21,6 = M/100
d'où M= 16/0,216 = 74 g/mol ; y= 16*13,5/21,6 = 10 ; x=
16*64,9/(12*21,6)= 4
C4H10O.
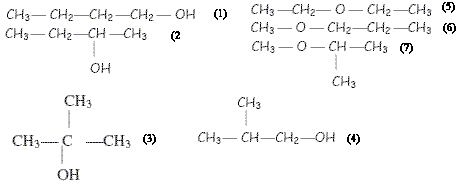
alcools : (1) butan-1-ol ; (2) butan-2-ol ; (4) 2-méthylpropan-1-ol
; (3) 2-méthylpropan-2-ol ; (5, 6, 7) éther
(1) et (2) ; (3) et (4) ; (5) et (6) : isomères de position de la fonction
(1) et (4) ; (7) et (6) : isomères de constitution ou de chaîne
(1) et (5) ; (7) et (3) : isomères de fonction
C4H10O + 6O2 --> 4 CO2
+ 5 H2O
Qté de matière initiale de C4H10O :
masse (g) = volume (mL) * masse volumique (g/mL) = 250*0,785 = 196,25g
puis masse (g) / masse molaire (g/mol) = 196,25 / 74 = 2,65
mol.
|
C4H10O
|
+ 6O2
|
--> 4 CO2
|
+ 5 H2O
|
|
initial
|
2,65 mol
|
excès
|
0
|
0
|
|
en cours
|
2,65-x
|
4x
|
5x
|
|
fin
|
2,65-xmax =0
xmax = 2,65 mol
|
4xmax= 10,6 mol
|
5xmax= 13,2 mol
|
volume CO2 : Qté matière (mol) * volume molaire (L/mol) =
10,6*25 = 265 L
masse d'eau : Qté de matière (mol)* mase molaire (g/mol) =
13,2 * 18 = 238 g soit 238 mL.
|
|
|