La combustion du carbone nécessite du
dioxygčne et produit du dioxyde de carbone.
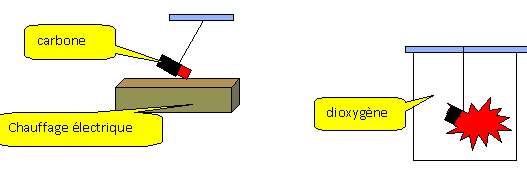
On place un morceau de carbone rougi dans du
dioxygčne : le carbone disparaît ; il brule
avec éclat dans le dioxygčne.
Le gaz formé est aspiré ŕ l'aide
d'une seringue et placer dans un tube ŕ essai
contenant de l'eau de chaux.
L'eau de chaux se trouble
Test du dioxyde de carbone : en présence de
dioxyde de carbone, l'eau de chaux donne un
précipité blanc.
|
Etat initial ( réactifs)
|
état final ( produit)
|
|
carbone ( le combustible)
|
dioxyde de carbone
|
|
dioxygčne ( le comburant)
|
Les espčces initiales sont différentes des
espčces finales : une transformation chimique a eu
lieu.
Elle porte le nom de
combustion.
Cette transformation chimique peut ętre traduite
ŕ l'aide d'une équation :
Carbone + dioxygčne -->
dioxyde de carbone.
|
Une combustion nécessite la
présence de réactifs (combustible et
comburant) qui sont consommés au cours de la
combustion ; un (ou des) nouveau(x) produit(s) se
forme(nt).
|
La combustion du butane et/ou du
méthane, d'une bougie, dans l'air nécessite du
dioxygčne et produit du dioxyde de carbone et de
l'eau.
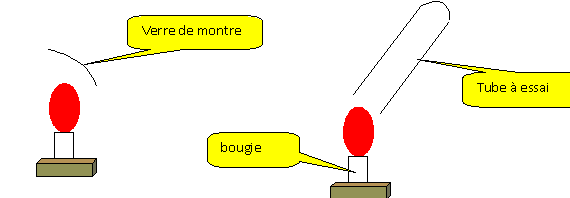
La partie froide du verre de montre
se couvre de buée : la combustion de la bougie
produit de l'eau.
Recueillir les gaz issus de la
combustion de la bougie dans un tube ŕ essais.
Ajouter dans ce tube 2 mL d'eau de chaux. Boucher et
agiter.
L'eau de chaux se trouble : la
combustion de la bougie produit du dioxyde de
carbone.
|
Etat initial ( réactifs)
|
état final ( produit)
|
|
bougie ( le combustible)
|
dioxyde de carbone
|
|
dioxygčne ( le comburant)
|
eau
|
Les espčces initiales sont différentes des
espčces finales : une transformation chimique a eu
lieu.
Cette transformation chimique peut ętre traduite
ŕ l'aide d'une équation :
bougie + dioxygčne -->
dioxyde de carbone + eau.
La combustion du fer dans le
dioxygčne.
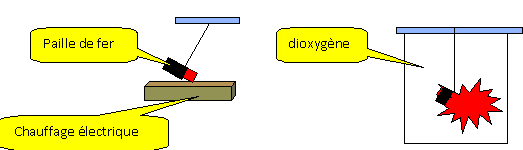
On place un morceau de paille rougi dans du
dioxygčne : le fer disparaît ; il brule avec
éclat et étincelle dans le
dioxygčne.
- On obtient un solide gris aprčs combustion.
- Le gaz formé est aspiré ŕ l'aide
d'une seringue et placer dans un tube ŕ essai
contenant de l'eau de chaux.
L'eau de chaux ne se trouble pas : la combustion ne
produit pas de dioxyde de carbone.
- Tester la présence de dioxygčne dans le
récipient aprčs combustion ŕ l'aide
d'une allumette rougie : l'allumette ne se rallume pas :
absence dedioxygčne.
|
Etat initial ( réactifs)
|
état final ( produit)
|
|
fer ( le combustible)
|
oxyde de fer
|
|
dioxygčne ( le comburant)
|
|
Les espčces initiales sont différentes des
espčces finales : une transformation chimique a eu
lieu.
Cette transformation chimique peut ętre traduite
ŕ l'aide d'une équation :
fer + dioxygčne --> oxyde de
fer.
|
Compléter
les phrases suivantes :
La ……… du carbone dans le
dioxygčne est vive. Dans cette
réaction ………, le carbone est
le ………Les deux
…………disparaissent ; il y a
formation d'un …………
nommé ……………
. L'air est composé essentiellement de
……… et en quantité moindre de
…………Le .....joue le rôle
de comburant.
La
combustion du
carbone dans le dioxygčne est vive. Dans
cette réaction
chimique, le
carbone est le
combustible.
Les deux
réactifs
disparaissent ; il y a formation d'un
produit
nommé dioxyde de
carbone.
L'air est composé essentiellement de
diazote et en
quantité moindre de
dioxygčne
; le dioxygčne
joue le rôle de comburant.
La combustion complčte de 9 g de carbone il
faut 24 g de dioxygčne ( ou bien 18 litres
de dioxygčne mesurés dans les
conditions normales de température et
pression).
Quelle masse de
dioxygčne faut-il pour brűler
complčtement 15 g de carbone
?
Masse de dioxygčne nécessaire
ŕ la combustion complčte de 1 g de
carbone :
24/9 = 2,67 g.
Masse de dioxygčne nécessaire
ŕ la combustion complčte de 15 g de
carbone :
2,67 *15 =
40
g.
Quel volume de
dioxygčne faut-il alors utiliser
?
Volume de dioxygčne nécessaire
ŕ la combustion complčte de 1 g de
carbone :
18/9 = 2 L.
Volume de dioxygčne nécessaire
ŕ la combustion complčte de 15 g de
carbone :
2 *15 = 30
L.
Quelle masse de carbone
peut-on faire brűler complčtement dans
96 g de dioxygčne ?
96 / 24 = 4 puis 9*4 =
36 g de
carbone.
Quel est le volume de
dioxygčne nécessaire ?
18*4 = 72
L.
Quel volume d'air est
alors nécessaire ?
L'air contient en volume 20 % de
dioxygčne.
72 / 0,2 =
360 L
d'air.
|


