|
ťlectrodťposition et prťcipitation bac S Antilles 09/07 En
poursuivant votre navigation sur ce site, vous acceptez l’utilisation
de Cookies vous proposant des publicitťs adaptťes ŗ vos centres
d’intťrÍts. |
||||||||||||||||||||||||||||||||||||||
| .
. |
||||||||||||||||||||||||||||||||||||||
|
||||||||||||||||||||||||||||||||||||||
|
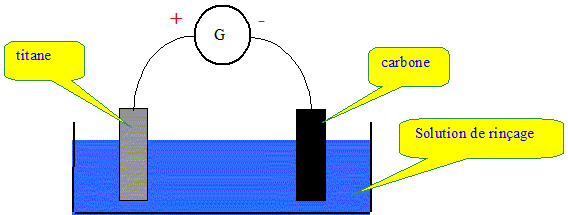
On s'intťresse ici ŗ une technique ťlectrochimique qui vise ŗ respecter la teneur officielle en cuivre dissous dans les effluents qui rťsultent d'opťrations de rinÁage. Le second rinÁage s'effectue en circuit fermť. Les eaux de rinÁage sont envoyťes sur des cellules d'ťlectrodťposition fonctionnant en continu, qui permettent la rťutilisation de ces eaux ultťrieures. La cuve ŗ ťlectrodťposition contient une ťlectrode en titane et une ťlectrode en carbone. Ces deux ťlectrodes sont immergťes dans la solution de rinÁage et sont alimentťes par un gťnťrateur de courant continu comme le montre le schťma suivant :
Principe. L'ťlectrodťposition du cuivre est un exemple d'ťlectrolyse. Est-ce une transformation spontanťe ? L'ťlectrolyse n'est pas une transformation spontanťe. C'est une transformation forcťe qui nťcessite un apport d'ťnergie sous forme ťlectrique. Sur quelle ťlectrode s'effectue le dťpŰt de cuivre mtallique ? Les ions cuivre prťsents en solution subissent une rťduction ŗ la cathode nťgative, le carbone dans ce cas. Ecrire la demi-ťquation ťlectronique correspondante. Cu2+(aq) + 2e- = Cu(s). L'autre ťlectrode est ťgalement le siŤge d'une transformation chimique. Est-ce une oxydation ou une rťduction ? L'anode positive est le siŤge d'une oxydation.
L'ťquation d'oxydorťduction
globale qui se dťroule dans la cellule
d'ťlectrodťposition est la suivante
: 2Cu2+(aq) + 2H2O(l) =
O2(g) + 4H+(aq) +
2Cu(s). Ecrire la demi-ťquation ťlectronique qui se dťroule ŗ l'anode de la cellule et identifier le couple oxydant / rťducteur. 2H2O(l) = O2(g) + 4H+(aq) + 4e-. couple oxydant / rťducteur :
O2(g) /
H2O(l)
La cellule est capable de ramener la teneur initiale en ion Cu2+ cm0=900,0 mg/L ŗ une teneur rťsiduelle cmf = 30,0 mg/L pour une durťe de fonctionnement ťgale ŗ 6 heures, dťlai nťcesaire entre deux rinÁages successifs. Le volume de solution traitťe pendant ce dťlai est V0=300 L.
Calculer la masse initiale m0 d'ions mťtalliques prťsents dans la solution au dťbut du rinÁage. m0 = Cm0 * V0 m0 = 900,0 * 300 =2,70 105 mg =270 g.
Calculer la masse finale mf d'ions mťtalliques prťsents dans la solution en fin de rinÁage. mf = Cmf * V0 mf = 30,0 * 300 =9,00 103 mg =9,00 g. En dťduire la masse mCu de cuivre dťposťe ŗ la cathode. mCu = m0 -mf =270-9,00 = 261 g. Calculer les quantitťs de matiŤre de cuivre prťsent sous ses deux formes nCu2+ et nCu en fin de rinÁage. M(Cu) = 63,5 gmol Quantitť de matiŤre (mol) = masse (g) / masse molaire (g/mol) nCu2+ = mf /M(Cu) nCu2+ = 9,00/63,5 = 0,142 mol. nCu = mCu /M(Cu) nCu = 261/63,5 = 4,11 mol.
Complťter le tableau d'ťvolution ci-dessous avec les quantitťs de matiŤre des espŤces chimiques mises en jeu. Cu2+(aq) + 2e- = Cu(s) La quantitť de matiŤred'ťlectrons est ťgale ŗ deux fois la qauntitť de matiŤre de cuivre
4,25-2xf =0,142 xf = 2,05 mol. ( 2,054)
Exprimer la qauntitť d'ťlectricitť Q utilisťe dans la cellule durant toute l'opťration. 1F= 9,65 104 C Q = 9,65 104 n(e-). avec n(e-) = 4 xf = 4*2,054 = 8,216 mol. Q= 9,65 104*8,216 = 7,93 105 C. Exprimer puis calculer l'intensitť I du courant, supposťe constante. I = Q/Dt avec D t = 6*3600 = 2,16 104 s. I = 7,93 105 / 2,16 104 =36,7 A.
Dans l'installation industrielle, deux appareils montťs en parallŤle sur le circuit des eaux de rinÁage assurent cette fonction d'ťlimination des ions Cu2+. Cela permet, par un dispositif annexe contenant un jeu d'ťlectrodes supplťmentaires, de rťcupťrer le dťpŰt solide de cuivre tout en permettant ŗ l'unitť de traitement de fonctionner sans interruption. Une mťthode plus classique consiste ŗ prťcipiter les ions Cu2+(aq) prťsents dans les eaux de rinÁage sous forme d'hydroxyde de cuivre (II), par ajout d'une solution d'hydroxyde de sodium (Na+(aq) + HO-(aq). La rťaction est alors : Cu2+(aq) +2HO-(aq) = Cu(OH)2 (s). Calculer la masse de prťcipitť d'hydroxyde de cuivre Cu(OH)2 produite lors de la prťcipitation de 4,11 mol d'ion Cu2+. Quantitť de matiŤre d'hydroxyde de cuivre = quantitť de matiŤre d'ion cuivre (II) = 4,11 mol Masse molaire de l'hydroxyde de cuivre (II) : 63,5+2*(16,0+1,0) = 97,5 g/mol. masse (g) = masse molaire (g/mol) * quantitť de matiŤre (mol) m = 97,5*4,11 = 401 g. Comparer cette masse avec la masse de cuivre obtenue. masse de cuivre obtenue : 261 g masse d'hydroxyde de cuivre (II) obtenue : 401 g soit environ 1,5 fois la masse de cuivre.
Ce rťsultat nous permet d'ťtablir une comparaison des deux procťdťs ( ťlectrodťposition et prťcipitation) sur la base des produits otenus dans chaque cas. Quel est le produit obtenu qu'il faudra extraire des eaux de rinÁage, puis traiter chimiquement pour le recycler. hydroxyde de cuivre (II). Lequel des deux procťdťs donne un produit directement utilisale ? L'ťlectrodťposition donne du cuivre pur, directement utilisable. |
||||||||||||||||||||||||||||||||||||||
|
|
||||||||||||||||||||||||||||||||||||||
|
|
||||||||||||||||||||||||||||||||||||||