|
Produit de solubilitť du chlorure d'argent : pile ; ťnergie rťticulaire concours Mines 2009.
En poursuivant votre navigation sur ce site, vous acceptez l’utilisation de Cookies vous proposant des publicitťs adaptťes ŗ vos centres d’intťrÍts. |
||||||||
| .
. |
||||||||
|
||||||||
|
Dans un bťcher nį1, on verse environ 40 mL d’une solution de chlorure de potassium ( K+ ; Cl-) de concentration CA = 1,00.10-2 mol.L-1 ; aprŤs addition d’une goutte de nitrate d’argent (Ag+ + NO3-) de concentration CB = 1,00.10-2 mol.L-1 , on observe la formation d’un prťcipitť de chlorure d’argent AgCl(s). Dans un bťcher nį2, on verse environ 50 mL de nitrate d’argent de concentration CB = 1,00.10-2 mol.L-1 . On plonge une lame d’argent dans chacun des bťchers que l’on relie par un pont salin au nitrate d’ammonium (NH4++ NO3-). On mesure alors ŗ 27įC la force ťlectromotrice de la pile ainsi constituťe : E =E2-E1 = 0,36 V oý E1 et E2 reprťsentent les potentiels des lames d’argent plongeant respectivement dans les bťchers 1 et 2. On posera cį = 1,00 mol/L et eį=RT/F ln10. Donnťes ŗ 27įC : eį = 0,060 V ; Eį1= 0,80 V ; Ks(AgBr)= 7,7.10-13. Rťaliser un schťma lťgendť de la pile, en spťcifiant les branchements du voltmŤtre (bornes COM et mV). 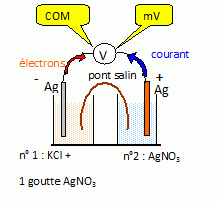 E2 ťtant supťrieure ŗ E1, l'ťlectrode du bťcher nį2 constitue la borne positive de la pile. Prťciser le rŰle du pont salin ; expliquer pourquoi on ne peut pas utiliser un pont au bromure de potassium (K+ + Br-). Le pont salin permet la continuitť ťlectrique et assure l'ťlectroneutralitť des solutions lors du fonctionnement de la pile. Les ions Br- donnant un prťcipitť de bromure d'argent ( Ks (AgBr) ťtant infťrieur ŗ Ks(AgCl), le solide AgBr apparaÓt avant AgCl ), en prťsence d'ion argent, on ne peut pas utiliser du bromure de potassium.
E1 = Eį1 +0,06 log [Ag+]1 avec Ks =[Ag+]1 [Cl-]1 = [Ag+]1 CA. Exprimer puis calculer le potentiel standard Eį2 du couple AgCl/Ag. Expliquer qualitativement pourquoi sa valeur est infťrieure ŗ celle du couple Ag+ /Ag.
Energie rťticulaire du chlorure d'argent. L’ťnergie rťticulaire d’un cristal ionique est l’ťnergie interne standard de rťaction ŗ 0 K, DrUį associťe ŗ la dissociation du cristal en ses ions constitutifs, isolťs et ŗ l’ťtat gazeux. On la confondra ici avec l’enthalpie standard DrHį associťe ŗ cette mÍme rťaction ŗ 298 K. Ecrire, en prťcisant l’ťtat physique de chaque constituant, les ťquations de rťaction permettant de dťfinir : • l’enthalpie standard de formation du chlorure d’argent solide ŗ 298 K : Ag(s) + ĹCl2(g) = AgCl(s), DHf = -127 kJ/mol • l’ťnergie d’ionisation de l’argent : l'argent mťtallique solide est transformť en argent gazeux, l'ťnergie nťcessaire pour cette transformation correspond ŗ l'ťnergie de sublimation DHsubl =285 kJ/mol. L'argent gazeux atomique est ionisť en ion Ag+(g) , l'ťnergie nťcessaire est l'ťnergie d'ionisation DEI = 727 kJ/mol. Ag (g) = Ag+(g) + e-. • l’ťnergie d’attachement ťlectronique du chlore. Le dichlore gazeux est dissociť en deux atomes de chlore gazeux, l'ťnergie nťcessaire est l'ťnergie de dissociation DHD = 242 kJ/mol. Le chlore gazeux atomique reÁoit 1 ťlectron et devient Cl-(g) , l'ťnergie nťcessaire est l'ťnergie d'attachement ťlectronique DAE = -350 kJ/mol. Cl(g) + e- = Cl-(g). On rappelle que le dichlore est ŗ l’ťtat gazeux dans son ťtat standard de rťfťrence ŗ 298 K. Dťterminer l’ťnergie rťticulaire Eret du chlorure d’argent. On pourra s’aider d’un cycle thermodynamique et on nťgligera l’influence de la tempťrature. 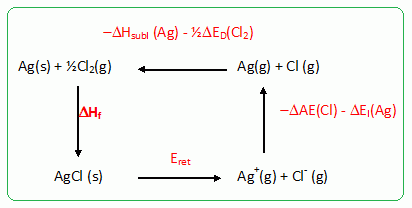 Eret = DHf - DHsubl -ĹDHD -DAE-DEI ; Eret = -127 -285 -0,5*242 -(-350) -727 = -910 kJ mol-1.
|
||||||||
| |
||||||||
|
|