|
Chimie : chlore, dichlore, chlorure, prťcipitation, conductimťtrie concours Mines 2009.
En poursuivant votre navigation sur ce site, vous acceptez l’utilisation de Cookies vous proposant des publicitťs adaptťes ŗ vos centres d’intťrÍts. |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| .
. |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
Le chlore a pour numťro atomique Z = 17. Masse atomique molaire de H : 1 g.mol-1 Masse atomique molaire de Cl : 35,5 g.mol-1 (g), (l), (s), (aq) aprŤs la formule d’une espŤce chimique signifient respectivement gazeux, liquide, solide et aqueux. Gťnťralitťs. Que reprťsente le numťro atomique d’un ťlťment chimique ? Le numťro atomique reprťsente le nombre de protons du noyau de l'atome, le nombre d'ťlectron de l'atome. C'est encore le nombre de charges. Quelle est la configuration ťlectronique du chlore dans son ťtat fondamental ? 1s2 2s2 2p6 3s2 3p5. Dans quelle colonne de la classification pťriodique se situe le chlore ? Comment se nomment les ťlťments de cette colonne ? Le chlore appartient ŗ la famille des halogŤnes, colonne 17 ( VII A) Faire les schťmas des structures de Lewis les plus probables des molťcules de dichlore et de chlorure d’hydrogŤne (HCl). Donner dans les deux cas les nombres d’oxydation du chlore.  Dans HCl, le nombre d'oxydation du chlore vaut -1 et dans Cl2, le nombre d'oxydation du chlore est nul. Qu’est ce qu’un nuclťon ? Un nuclťon est un constituant du noyau de l'atome, c'est ŗ dire un proton ou un neutron. Rappeler la dťfinition de deux isotopes d’un mÍme ťlťment. Deux isotopes possŤdent le mÍme nombre de protons ( mÍme numťro atomique) mais des nombres de neutrons diffťrents. Le chlore a une masse atomique molaire moyenne d’environ 35,5 g.mol-1. Il est essentiellement composť des isotopes 35 et 37. La masse molaire d’un nuclťon est prise ŗ 1 g.mol-1.
Sous la pression P0 = 1 bar maintenue constante, ŗ la tempťrature T, ŗ partir d’un mťlange de HCl(g) et de O2(g), il se forme Cl2(g) et H2O(g). Ecrire l’ťquation bilan de la rťaction avec 1 pour coefficient (nombre) stoechiomťtrique de O2. 4HCl(g) +O2(g) = 2Cl2(g) +2H2O(g). Les rťactifs sont pris en quantitťs stoechiomťtriques (1 mole de O2). Quel est l’avancement maximum xmax de cette rťaction ? Dans le cas d'une rťaction totale, les deux rťactifs disparaissent en fin de rťaction : xmax = 1 mol. A l’ťquilibre, 75% de HCl a disparu. Dťterminer l’avancement xe de la rťaction ŗ l’ťquilibre.
Par suite : 4-4xe =1 soit xe =0,75 mol. Les gaz ťtant supposťs parfaits, dťterminer les pressions partielles de chacun des constituants ŗ l’ťquilibre. Nombre total de moles ŗ l'ťquilibre : N = 4,25 moles. Fractions molaires : XHCl =1/4,25 =0,235 ; XO2 =0,25/4,25 =0,059 ; XCl2 =XH2O =1,5/4,25 =0,353. Pressions partielles : PHCl =XHCl P0 =0,235 bar ; PO2 =XO2 P0 = 0,059 bar ; PCl2 =PH2O =XCl2 P0=0,353 bar. Exprimer la constante de cet ťquilibre K0P ŗ la tempťrature T en fonction des pressions partielles et la calculer. K0P=P2Cl2 .P2H2O / ( PO2.P4HCl) = 0,3534 / (0,059 *0,2354) =86,3 ~ 86.
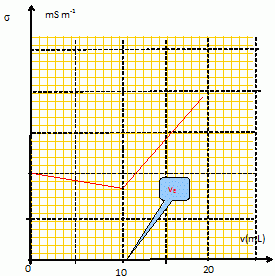
Dosage des ions chlorure Cl-(aq) par prťcipitation. Dans cet exercice, tous les ions sont sous forme aqueuse. Pour s’assurer que le dosage des ions Cl-(aq) par les ions Ag+(aq) est possible, on rťalise au prťalable la manipulation suivante. On effectue le dosage de V1 = 100 mL d’une solution S1 placťe dans le bťcher, de chlorure de sodium (Na+, Cl-) de concentration C1 = 10-2 mol.L-1 par une solution S2 de nitrate d’argent (Ag+, NO3-) placťe dans la burette, de concentration C2 = 8.10-2 mol.L-1. Le produit de solubilitť du chlorure d’argent AgCl(s) est : K0S1 =10-10. Ecrire la rťaction de dosage. Ag+(aq) + Cl-(aq) = AgCl(s). Exprimer la constante d’ťquilibre K en fonction des concentrations. K = 1/ ([Ag+(aq)][Cl-(aq)]) =1/ K0S1 = 1010. La prťcipitation dťbute-t-elle dŤs la premiŤre goutte ? (une goutte = 0.05 mL). La prťcipitation dťbute dŤs que le produit de solubilitť est atteint : [Cl-(aq)]i =C1 = 10-2 mol.L-1. Juste aprŤs l'ajout de la premiŤre goutte : [Ag+(aq)]i = (8 10-2 *0,05 / 100) = 4 10-5 mol/L. [Cl-(aq)]i [Ag+(aq)]i = 4 10-7 , valeur supťrieure au produit de solubilitť : la prťcipitation a dťbutť. Calculer le volume V2e de la solution de nitrate d’argent versť ŗ l’ťquivalence. C2V2e =V1 C1 ; V2e =V1 C1/C2 =100*10-2 /8.10-2= 12,5 mL ~ 13 mL. On a ajoutť dans le bťcher, en guise d’indicateur colorť, V3 = 2 mL d’une solution de chromate de potassium K2CrO4, (2 K+, CrO42-) de concentration C3 = 1 mol.L-1, susceptible de donner le prťcipitť Ag2CrO4(s), de couleur rouge, dont le produit de solubilitť est K0S2 =10-11,8. Ecrire la rťaction de prťcipitation de Ag2CrO4(s). Ag2CrO4(s) = 2Ag+ aq+ Cr042- aq ; Exprimer la constante d’ťquilibre K0S2 en fonction des concentrations. K0S2 = [ Ag+ aq]2[ Cr042- aq] Montrer que AgCl(s) prťcipite avant Ag2CrO4(s). AgCl(s) = Ag+ aq+ Cl- aq; K0s1 = [ Ag+ aq][ Cl- aq] avec [ Cl- aq]initial = 10-2 mol/L. AgCl commence ŗ prťcipiter dŤs que [ Ag+ aq] = K0s1 / [ Cl- aq]initial = 10-10 / 10-2 = 10-8 mol/L Ag2CrO4(s) = 2Ag+ aq+ Cr042- aq ; K0S2 = [ Ag+ aq]2[ Cr042- aq] avec [ Cr042- aq]initial =C3V3/ (V3+V1)=2/102= 1,96 10-2 mol/L Ag2CrO4 commence ŗ prťcipiter dŤs que [ Ag+ aq] =[ K0S2 / [ Cr042- ]initial ]Ĺ=[ 10-11,8 / 1,96 10-2 ]Ĺ = 9 10-6 mol/L AgCl prťcipite donc en
premier. [ Cr042- aq]ťq =C3V3/ (V3+V1+V2e)=2/114,5= 1,74 10-2 mol/L. Ag2CrO4 commence ŗ prťcipiter dŤs que [ Ag+ aq] =[ K0S2 / [ Cr042- ]initial ]Ĺ=[ 10-11,8 / 1,74 10-2 ]Ĺ = 9,5 10-6 mol/L. [ Cl- aq] =K0s1 / [ Ag+ aq] = 10-10 / 9,5 10-6 =1,0 10-5 mol/L.
Cinťtique. La
cinťtique de cette rťaction ťtant d’ordre 1 par rapport ŗ RCl, exprimer
la loi de vitesse, en dťduire une ťquation diffťrentielle en x,
l’intťgrer et exprimer la concentration x en fonction de a, de t et de
la constante de vitesse k.
[ROH]= x = i n/ V0 ; [RCl]= (aV0 - i n)/ V0 =a-x
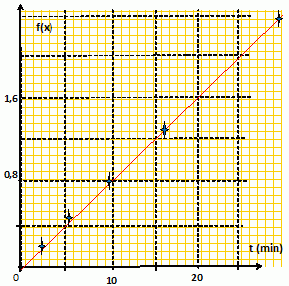
v =k[RCl] = -d[RCl]/dt avec [RCl] = a-x et [ROH]=x ; -d[RCl]/dt = dx/dt Quelle fonction f(x) doit-on tracer pour diffťrentes valeurs de t si l’on veut obtenir une droite de pente +k ? Le tableau ci-dessous donne les diffťrentes valeurs des ti. Reproduire et complťter ce tableau.
Placer les couples de points (f(xi), ti
) sur un graphe (tracť sur la feuille). Leur alignement est-il
satisfaisant ? Dťduire la valeur de la constante de vitesse k en
prťcisant bien son unitť. |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
|