|
Distillation,
diagramme binaire eau ťthanol
concours chimie Capes
2007.
En poursuivant votre navigation sur ce site, vous acceptez l’utilisation de Cookies vous proposant des publicitťs adaptťes ŗ vos centres d’intťrÍts. |
||||||||||||||||||||
| .
. |
||||||||||||||||||||
|
||||||||||||||||||||
|
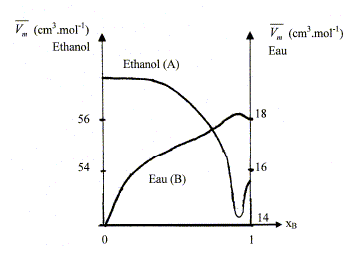
mťlange idťal : microscopiquement la solution se comporte comme un liquide pur : les interactions entre molťcules diffťrentes et molťcules identiques sont ťgales. Il faut pour cela que les molťcules soient assez semblables ( exemple O2 et N2). L'eau et l'ťthanol ne constituent pas un mťlange idťal. Le volume total d’une solution binaire idťale vaut : V = n1Vm,1 + n2Vm,2. Vm i : volume molaire d'un constituant pur ; ni : quantitť de matiŤre (mol) Ou en divisant par n1+n2 : Vm = x1Vm,1 + x2Vm,2= Vm,1 +x2(Vm,1 -Vm,2) (1) Vm : volume molaire de la solution ; xi : fraction molaire x1+x2 = 1. Les forces intermolťculaires entre les diffťrentes espŤces conduisent ŗ des volumes rťels infťrieurs ou supťrieurs ŗ celui prťvu. Les volumes molaires partiels des espŤces sont diffťrents des volumes molaires de ces mÍmes espŤces ŗ l'ťtat pur. (1) s'ťcrit : Vm =V1 +x2(V1 -V2) (2) V i : volume molaire partiel d'un constituant.
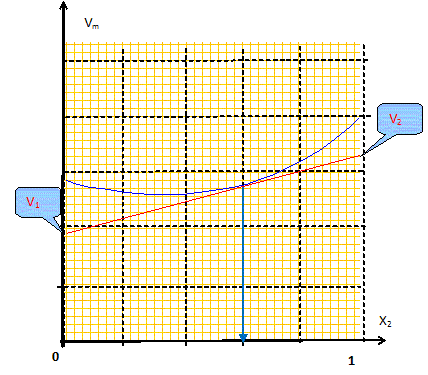
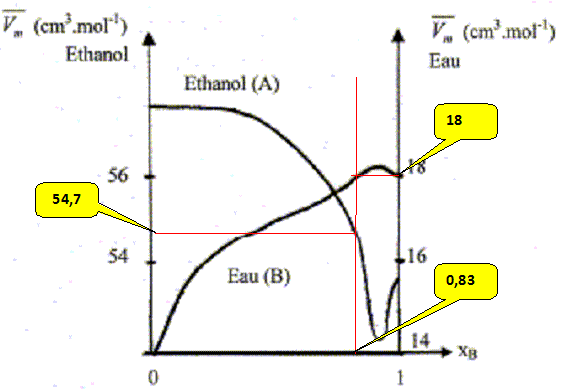
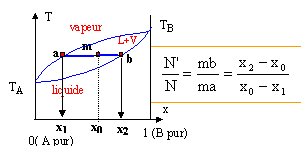
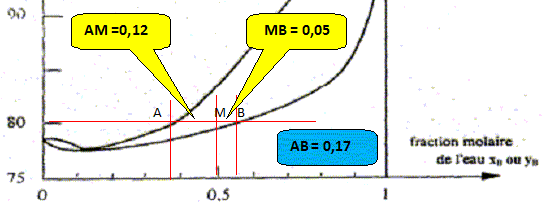
Les volumes molaires partiels ŗ pour une composition donnťe sont obtenus par les interceptions de la tangente ŗ la courbe Vm = f(x2) avec les axes verticaux x2 = 0 et x2 = 1. masse volumique de l'ťthanol A
: rA = 785 km
m-3 = 0,785 g/mL masse volumique de l'eau B :
rB = 1000 km m-3 =
1,00 g/mL Masses molaire ( g/mol) : eau : 18 ;
ťthanol : 46. Calcul du volume du
mťlange obtenu :
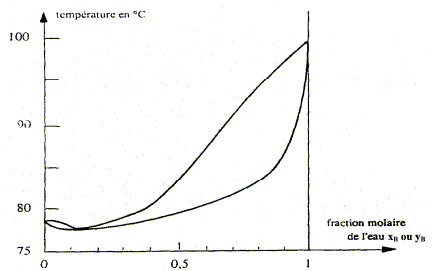
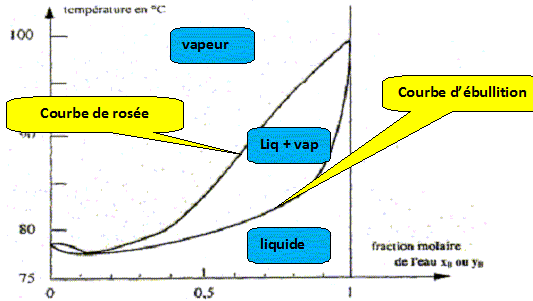
Nom du point de coordonnťes xB=0,11 et T= 78,3į. azťotrope. courbe de rosťe, ensemble des points oý apparaÓt la premiŤre goutte de liquide lorsqu'on refroidit de la vapeur. courbe de d'ťbullition, ensemble des points oý apparaÓt la premiŤre goutte de vapeur lorsqu'on chauffe le liquide.
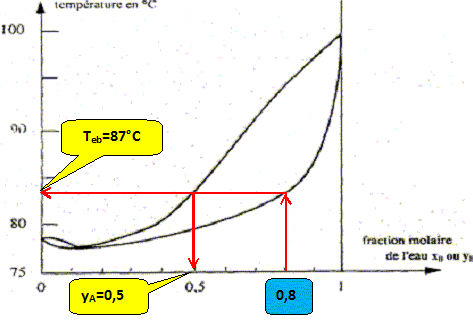
On considŤre une mole de mťlange liquide de fraction molaire xB=0,8, initialement ŗ 20 įC que l'on chauffe sous pression constante P= 1,013 bar. A quelle tempťrature Teb ( įC) l'ťbullition commence t-elle et quelle est la fraction molaire en alcool yA de la premiŤre bulle formťe ?
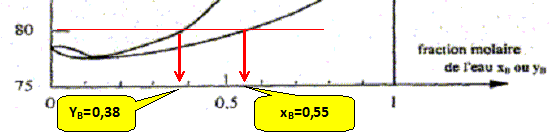
A quelle tempťrature Tev ( įC) la derniŤre de liquide s'ťvapore t-elle et quelle est la fraction molaire en alcool xA de cette derniŤre goutte ? La vapeur s'enrichi en alcool, constituant le plus volatil. Le liquide s'appauvrit en alcool : xB tend vers 1, eau pure, s'ťvaporant ŗ 100įC.
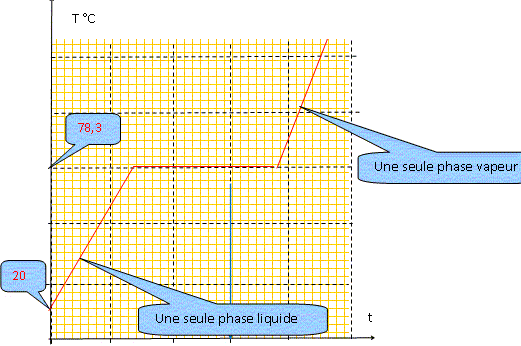
Consťquences pratiques de l'existence de l'azťotrope : - sťparation de l'eau et de l'ťthanol impossible ŗ rťaliser dans une installation de distillation ŗ une colonne : le distillat ŗ la composition de l'azťotrope. La composition de l'azťotrope varie avec la pression. On chauffe progressivement un mťlange eau/ťthanol de fraction molaire xB=0,11 initialement ŗ 20 įC, en enregistrant la tempťrature. Reprťsenter qualitativement la courbe donnant l'ťvolution de la tempťrature en fonction du temps, en faisant apparaÓtre les domaines monophasťs et biphasťs.
A l'azťotrope la phase liquide et la phase vapeur ont la mÍme composition : deux constituants et une relation. Prťsence de deux phases d'oý la variance v = (2-1)+2-2 = 1. La pression ťtant
fixťe, le systŤme est invariant. La
tempťrature d'ťbullition, ŗ
l'azťotrope, est constante.
|
||||||||||||||||||||
|
|
||||||||||||||||||||
|
|