|
Chimie
organique : synthŤse d'un composť odorant, le Florhydral, Bts chimie 2009
En poursuivant votre navigation sur ce site, vous acceptez l’utilisation de Cookies vous proposant des publicitťs adaptťes ŗ vos centres d’intťrÍts. |
||||||||||||||||
| .
. |
||||||||||||||||
|
||||||||||||||||
florale (muguet, jacinthe) ; il est ťgalement utilisť dans les parfums pour des produits de blanchisserie oý une odeur rťsiduelle fraÓche est dťsirťe. Une synthŤse de ce composť est dťcrite ci-dessous. 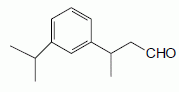 Le crotonaldťhyde est un intermťdiaire qui est utilisť dans la synthŤse du Florhydral. Il est obtenu facilement par un traitement basique de l’ťthanal. Sa formule semi-dťveloppťe est lasuivante : CH 3–CH=CH–CHO. Donner le nom du crotonaldťhyde en nomenclature systťmatique.(2 E)-but-2Ťnal ou (2Z)-but-2-Ťnal Dessiner les diffťrents stťrťoisomŤres du crotonaldťhyde en prťcisant leur stťrťochimie. 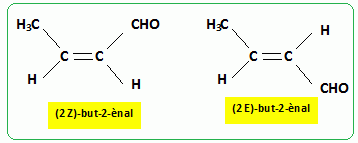 Donner
les ťquations des deux rťactions permettant d’obtenir le crotonaldťhyde
ŗ partir de l’ťthanal. Prťciser le nom de ces rťactions et donner le
mťcanisme de la premiŤre ťtape Condensation aldol de l'ťthanal.
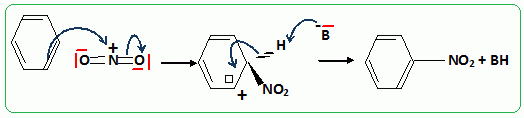
Le substituant ťlectroattracteur -NO2 appauvrit la densitť ťlectronique du noyau benzťnique ; ce dernier est moins rťactif ; Pour une seconde substitution, la position mťta est la moins dťfavorisťe.
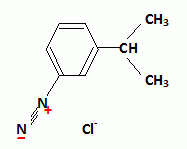
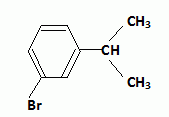
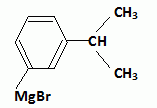
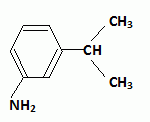
Seconde substitution : Friedels et Craft en prťsence de catalyseur AlBr3. Obtention du Florhydral. Le composť B est rťduit par l’ťtain en prťsence d’acide chlorhydrique. AprŤs passage en milieu basique, on obtient C.C est dissous dans l’acide chlorhydrique. On lui ajoute lentement du nitrite de sodium (NaNO2) tout en maintenant une tempťrature infťrieure ŗ 5 įC. Il se forme un composť D (non isolť). On additionne ŗ D du bromure de sodium ainsi que du bromure de cuivre(I) (CuBr : catalyseur). AprŤs rťaction, on isole un composť E (3-bromoisopropylbenzŤne). On introduit le composť E dans une solution contenant du magnťsium et du THF (tťtrahydrofuranne). On obtient F. Indiquer, dans un tableau, les formules semi-dťveloppťes des molťcules C, D, E et F.
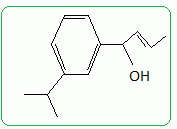
Dans l’ťtape C → D, indiquer le rťactif formť quand on ajoute le nitrite de sodium ŗ l’acide chlorhydrique. Dťtailler le mťcanisme de l’ťtape C → D. 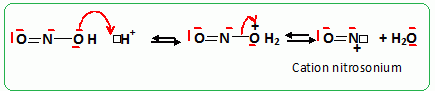 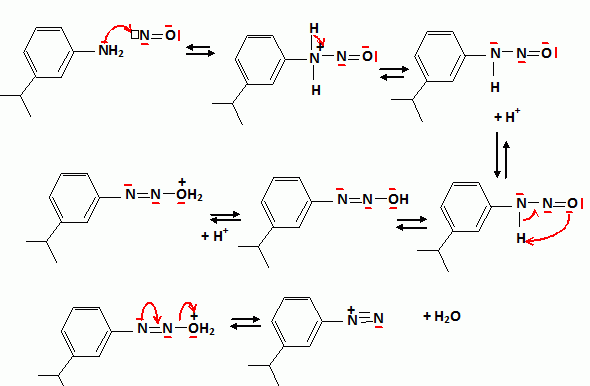 …tude de l’ťtape E → F. On utilise un ťther cyclique : le THF. Prťciser les rŰles de ce composť. Les organomagnťsiens sont des acides de Lewis ; le THF est une base de Lewis dans laquelle les doublets de l'oxygŤne sont trŤs dťgagťs. Un solvant donneur d'ťlectrons stabilise l'organomagnťsien. Le solvant doit Ítre assez polaire pour dissoudre l'organomagnťsien. Expliquer pourquoi il est important de travailler en l’absence d’eau et de dioxyde de carbone. Donner la formule du produit obtenu par rťaction de F avec chacune de ces molťcules. Les organomagnťsiens sont des bases fortes : en prťsence d'eau ils s'hydrolysent suivant : RMgBr + H2O --> RH + ĹMgBr2 + ĹMg(OH)2. On obtient dans ce cas : 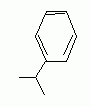 En prťsence de CO2 ils conduisent ŗ un acide carboxylique suivant : RMgBr + CO2 + H2O--> RCOOH + ĹMgBr2 + ĹMg(OH)2. On obtient dans ce cas : 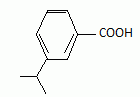
|
||||||||||||||||
|
|
||||||||||||||||
|
|
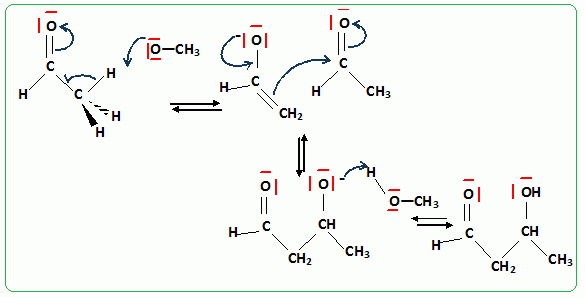
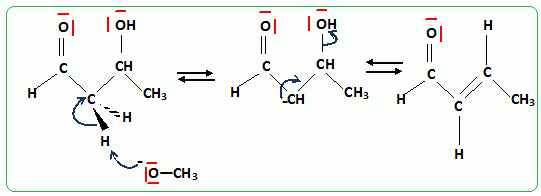
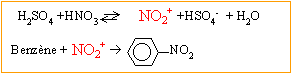
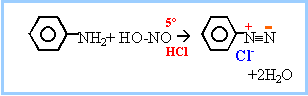 diazotation
diazotation