|
Organomagnťsien et chlorure d'acyle, dťshydratation d'un alcool, effet Kharash, concours Mines 07 En
poursuivant votre navigation sur ce site, vous acceptez l’utilisation
de Cookies vous proposant des publicitťs adaptťes ŗ vos centres
d’intťrÍts. |
|||||||
| .
. |
|||||||
|
|||||||
|
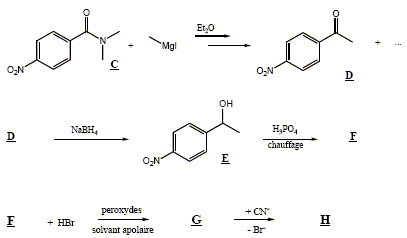
La suite des rťactions est la suivante :
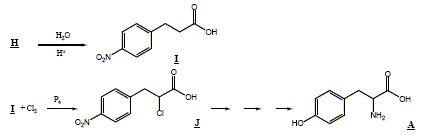
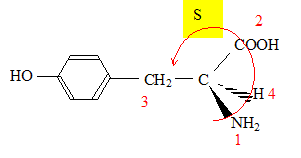
Le descripteur stťrťochimique du carbone asymťtrique de la tyrosine naturelle A est S (sinister). Classement des
substituants par ordre de prioritť
dťcroissante : NH2 ; COOH ;
CH2-C6H4-OH ;
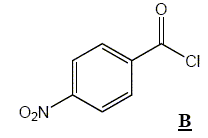
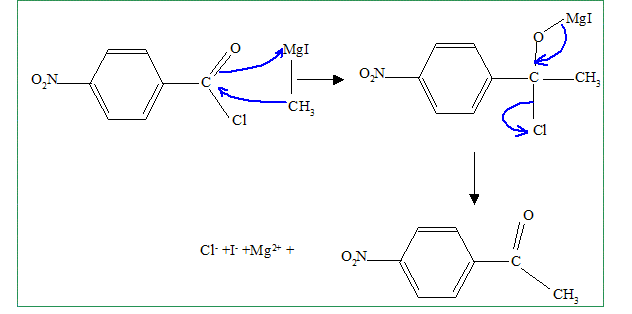
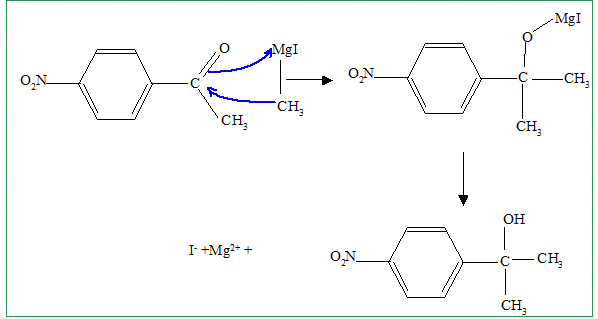
H. La rťaction de synthŤse de l’iodure de mťthylmagnťsium s’effectue dans l’ťther anhydre (ou ťthoxyťthane anhydre). …crire l’ťquation de formation de l’organomagnťsien. CH3I+ Mg (s)= CH3-Mg I Pourquoi cette synthŤse doit-elle Ítre faite dans un solvant anhydre ? Il faut travailler en milieu anhydre, sinon l'organomagnťsien est dťtruit par l'eau ( la rťaction est vive); de plus l'ťther, par ses propriťtťs basiques, stabilise l'organomagnťsien formť. Parmi les solvants disponibles dans le laboratoire, on trouve, outre l’ťther, l’ťthanol, le cyclohexane, l’ťthylamine (ou ťthanamine), l’acide acťtique, le trichloromťthane et le THF. Dire pour chacun de ces solvants, en justifiant votre rťponse, s’il convient ou non en remplacement de l’ťther pour la synthŤse de l’iodure de mťthylmagnťsium. L'organomagnťsien est une base forte susceptible de rťagir avec les solvants protiques : ťthanol, acide ťthanoÔque, ťthylamine sont donc exclus. Le solvant, une base de Lewis, doit stabiliser l'organomagnťsien : cychlohexane exclu. Un organomagnťsien rťagit avec les dťrivťs chlorťs : HCCl3 exclu. Seul le THF convient. Quel serait le produit obtenu, aprŤs hydrolyse acide, en faisant agir l’iodure de mťthylmagnťsium en excŤs, dans l'ťther, sur le chlorure d’acyle B ? Donner le schťma
rťactionnel.
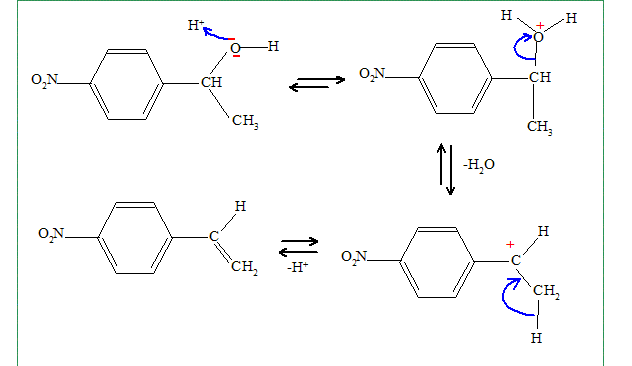
Proposer un mťcanisme pour cette rťaction. Prťciser la formule semi dťveloppťe de F. Quel est le rŰle de l'acide phosphorique ? L'acide phosphorique, acide fort, protone l'oxygŤne du groupe alcool. H+ est rťgťnťrť en fin de rťaction. H+ catalyse la rťaction. H2O est un bon nuclťofuge, d'autant plus que le carbocation plan rťsultant est stabilisť par rťsonance avec le noyau benzŤnique.
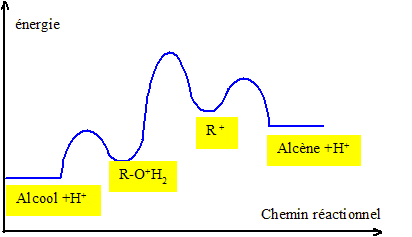
Sachant que la rťaction de dťshydratation est endothermique, tracer le profil ťnergetique de la rťaction.
Proposer un mťcanisme pour la rťaction F-->G. Prťciser la formule semi-dťveloppťe de G. Effet Kharash, addition de HBr sur une double liaison en prťsence de peroxyde R-O-O-R et en milieu apolaire. Initiation : R-O-OR --> 2R-O.. R-O.+HBr --> ROH + Br.. Propagation :
Rupture de chaÓne : 2 Br. --> Br2. Quel serait le produit majoritaire de la rťaction en l'absence de peroxydes et en milieu polaire ? Addition suivant la rŤgle de Markovnikov: on obtient le dťrivť bromť secondaire O2N-C6H4-CHBr-CH3.
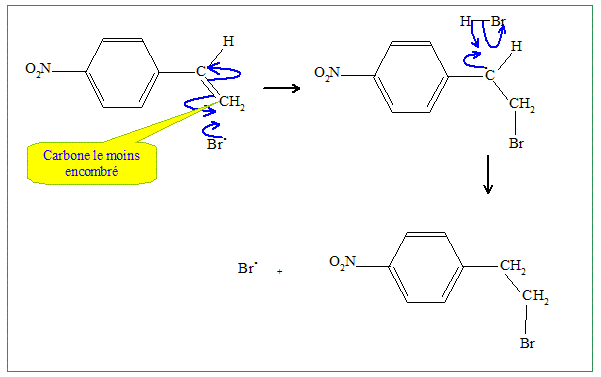
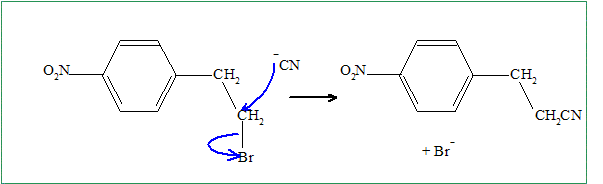
Proposer un mťcanisme pour la rťaction G-->H. Comment se nomme ce type de rťaction ? Sur un dťrivť bromť primaire, on observe une substitution nuclťophile bimolťculaire ( SN2) plutŰt qu'une SN1.
|
|||||||
|
|
|||||||
|
|