|
Dosage des ions chlorures : potentiomťtrie, conductimťtrie capes agricole 2004 En
poursuivant votre navigation sur ce site, vous acceptez l’utilisation
de Cookies vous proposant des publicitťs adaptťes ŗ vos centres
d’intťrÍts. |
|||||||
| .
. |
|||||||
|
|||||||
|
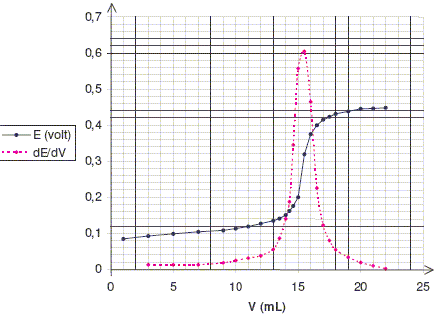
On veut vťrifier la teneur en ions chlorure d’un sťrum physiologique. Pour cela, on ajoute progressivement une solution de nitrate d’argent de concentration C = 0,100 mol.L-1 ŗ un volume V0 = 50,0 mL d’une solution S prťparťe en diluant cinq fois le sťrum ťtudiť et on suit l’ťvolution correspondante de la diffťrence de potentiel E entre une ťlectrode d’argent et une ťlectrode au calomel saturť (notťe E.C.S.). Les rťsultats obtenus sont donnťs ci-dessous :
Donner l’expression du potentiel d’oxydorťduction de l’E.C.S.. Pourquoi est-il constant ŗ tempťrature constante ? L'ťlectrode de rťfťrence utilisťe ici est une ťlectrode au calomel saturťe (ECS), c'est ŗ dire une ťlectrode de platine (Pt) recouverte de mercure (Hg) sur lequel est dťposť du calomel Hg2Cl2. Cette ťlectrode est dite saturťe car la solution dans laquelle plonge l'ťlectrode ainsi constituťe est une solution aqueuse saturťe en chlorure de potassium KCl. couple Hg2Cl2 (s)/ Hg (l) : Hg2Cl2 (s)+ 2e- =2 Hg(l) + 2Cl-. Erťf = Eį[ Hg2Cl2 (s)/ Hg (l)] + 0,03 log 1/[Cl-]2. Erťf = 0,27 -0,06 log [Cl-]. Dans la solution saturťe en KCl : [Cl-] = 4,7 mol/L ŗ 25 įC. E rťf = 0,27 -0,06 *log 4,7 = 0,23 V.
Les ions argent, en contact au niveau du verre
frittť (paroi poreuse ŗ
l’extrťmitť de
l’ťlectrode) avec les ions chlorure de
l’ECS,donne un prťcipitť de
chlorure d’argent. Ce dernier bouche le verre
frittť ; l'ťlectrode devient
inutilisable. On ajoute ŗ l’E.C.S une allonge en
verre remplie d’une solution de nitrate de
potassium. La conduction ťlectrique demeure
; il n'y a plus contact direct entre les ions
chlorure de l'ťlectrode et la solution
contenant les ions Ag+. Dťterminer la concentration molaire volumique des ions chlorure dans la solution S puis dans le sťrum. Ag+(aq) + Cl-(aq) = AgCl(s). A l'ťquivalence les quantitťs de rťactifs mis en prťsence sont en proportions stoechiomťtriques : C Vťq = V0 CS avec Vťq = 15,5 mL ( lecture graphe) ; V0 = 50,0 mL ; C= 0,100 mol/L. CS = 0,100*15,5/50,0 = 3,10 10-2 mol/L. Csťrum = 5 CS =5* 3,10 10-2 = 0,155 mol/L. Comparer ŗ l’indication portťe sur l’ťtiquette du sťrum : 0,9 % en masse de chlorure de sodium. Masse molaire NaCl : M= 35,5+23 = 58,5 g/mol. M*Csťrum =58,5*0,155 = 9,07 g/L La densitť du sťrum est ťgale ŗ 1 : 0,907 g de NaCl dans 100 g de sťrum ou 0,91%. Valeur en accord avec celle de l'ťtiquette.
CSV0-CV1 = 0,031*50-0,1*10 = 0,55 mmol ; [Cl-(aq)] = 0,55 / (V0+V1 ) = 0,55 / 60 = 9,16 10-3 mol/L. Repport dans (1) : 0,115 = Eį(AgCl(s)/Ag(s)-EECS -0,06 log 9,16 10-3 ; Eį(AgCl(s)/Ag(s)-EECS = 0,115+0,06 log 9,16 10-3 = -7,3 10-3.(2)
V2 = 20 mL ajoutť : aprŤs l'ťquivalence, l'ion argent est en excŤs de : C(Vťq-V1 ) =0,1*(20-15,5) = 0,45 mmol ; [Ag+(aq)] = 0,45 / (V0+V2 ) = 0,45 / 70 = 6,43 10-3 mol/L. (1) et (2) donnent : 0,445 = -7,3 10-3 -0,06 log [Cl-(aq)] ; log [Cl-(aq)] = (-7,3 10-3 -0,445)/ 0,06 = -7,54 ; [Cl-(aq)] = 2,9 10-8 mol/L Ks = [Cl-(aq)] [Ag+(aq)] = 2,9 10-8* 6,43 10-3 ; Ks =1,86 10-10. Dťterminer la valeur du potentiel standard d’oxydorťduction du couple Ag+(aq) / Ag(s). (2) donne : Eį(Ag+(aq) / Ag(s)) + 0,06 log Ks -EECS = -7,3 10-3. Eį(Ag+(aq) / Ag(s)) = -7,3 10-3- 0,06 log 1,86 10-10 +EECS= -7,3 10-3 + 0,583 +0,23 Eį(Ag+(aq) / Ag(s)) =0,80 V. Conductimťtrie. Le dosage prťcťdent peut ťgalement Ítre suivi par conductimťtrie. Faire un schťma clair d’une cellule de conductimťtrie. Quelle est la grandeur qui est alors effectivement mesurťe ? La cellule conductimťtrique est constituťe de deux plaques rectangulaires de platine platinťs, de surface S, parallŤles ŗ une distance l sur un support en verre. On mesure la rťsistance R ( ohm) du volume de liquide dťlimitť par les plaques ; la cellule indique la conductance G = 1/R ( siemens ). En quoi consiste l’ťtalonnage d’un conductimŤtre ? Le fabricants fournit une table de la conductivitť d’une solution de chlorure de potassium ŗ 0,1 mol /L pour toutes les tempťratures allant de 15,0 ŗ 30,0įC. On mesure alors la conductance de cette solution de chlorure de potassium et la tempťrature de la solution. Les conductimťtres sont munis d’un potentiomťtre d’ťtalonnage qui permet d’ajuster la valeur lue ŗ la valeur donnťe par la table du fabricant. Est-il utile d’ťtalonner un conductimŤtre pour rťaliser un dosage conductimťtrique ? Non : afin de dťterminer le volume ťquivalent, on recherche l'intersection de deux droites. Quelles sont les conditions nťcessaires pour obtenir des portions de droites lors d’un dosage conductimťtrique ? Le volume de la solution du bťcher doit Ítre paratiquement constant : utiliser un grand volume de solution ŗ titrer ( ajouter de l'eau distillťe) et ajouter ŗ la burette graduťe, un petit volume de solution titrante ( donc beaucoup plus concentrťe que la solution ŗ titrer).
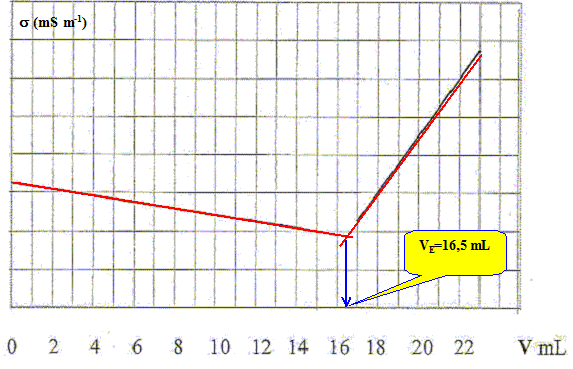
Les conductivitťs molaires ioniques limites ( mS.m2.mol-1) de quelques ions sont indiquťes ci-dessous : lį Na+ = 5,01 ; lį Cl- = 7,63 ; lį Ag+ = 6,19 ; lį NO3-= 7,14. Indiquer l’allure de la courbe donnant les variations du produit : ęconductivitť . VolumesolutionĽ
Pour justifier le tracť ainsi rťalisť, donner l’expression et la valeur des pentes des portions de droites obtenues. Equation de la rťaction associťe ŗ ce dosage : Ag+ aq + Cl- aq ---> AgCl solide. Avant l'ťquivalence : L'ion argent est en dťfaut ; l'ion chlorure est en excŤs ; les ions nitrate et sodium sont spectateurs. ( les ions oxonium et hydroxyde sont minoritaires) s = lNa+[Na+] + lCl-[Cl-] + lNO3-[NO3-] On ajoute x = CV mol d'ion argent ( qui demeure en dťfaut ) et x = CV mol d'ion nitrate. x mol d'ion chlorure disparaissent : du point de vue de la conductivitť, tout se passe comme si on remplaÁait l'ion chlorure par l'ion nitrate. Or lCl- > lNO3- donc la conductivitť de la solution diminue. On note V0 le volume de la solution dans le becher et V le volume de nitrate d'argent ajoutť ŗ la burette. On note C la concentration du nitrate d'argent et CS celle du chlorure de sodium. [Na+] =V0 CS / (V0+V) ; [Cl-] =(V0 CS -C V)/ (V0+V) ; [NO3-] =CV/ (V0+V) s = [lNa+V0 CS + lCl-(V0 CS -C V)+ lNO3-CV]/ (V0+V) s = [(lNa+ + lCl-) V0 CS + ( lNO3- -lCl-)CV]/ (V0+V) s (V0+V) = (lNa+ + lCl-) V0 CS + ( lNO3- -lCl-)CV On trace s (V0+V) = f(V) : droite de pente : ( lNO3- -lCl-)C = (7,14-7,63)*0,1 = -0,049 S m-1.
AprŤs l'ťquivalence : L'ion chlorure est en dťfaut ; l'ion argent est en excŤs ; les ions nitrate et sodium sont spectateurs. ( les ions oxonium et hydroxyde sont minoritaires) s = lNa+[Na+] + lAg+[Ag+] + lNO3-[NO3-] on ajoute x = CV mol d'ion argent ( qui est en excŤs de C(V-VE) ) et x = CV mol d'ion nitrate. L'ajout d'ions en solution se traduit par une augmentation de la conductivitť de la solution. [Na+] =V0 CS / (V0+V) ; [Ag+] =C(V-VE)/ (V0+V) ; [NO3-] =CV/ (V0+V) s = [lNa+V0 CS + lAg+C(V-VE)+ lNO3-CV]/ (V0+V) s = [lNa+V0 CS - lAg+C VE + ( lNO3- +lAg+)CV]/ (V0+V) ; or V0 CS = C VE s (V0+V) = (lNa+ - lAg+ ) VE C + ( lNO3- +lAg+)CV On trace s (V0+V) = f(V) : droite de pente :( lNO3- +lAg+)C = (7,14+6,19)*0,1 = +1,33 S m-1. |
|||||||
|
|
|||||||
|
|