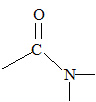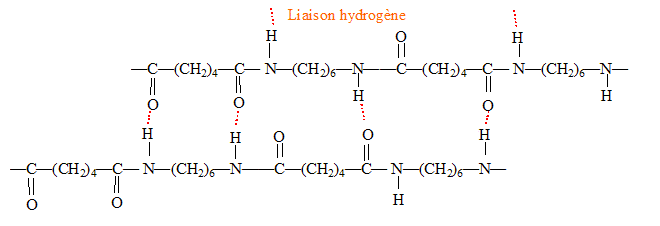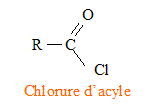|
enseignement, concours, caplp interne 2006 : ą propos des matičres plastiques En poursuivant votre navigation sur ce site, vous acceptez l’utilisation de Cookies vous proposant des publicités adaptés ą vos centres d’intérźts. |
|||||||||
| .
. |
|||||||||
|
|||||||||
|
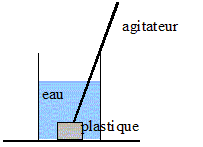
Thermoplastiques : fondent de maničre réversible en les chauffant. Polyéthylčne (PE) ; Polypropylčne (PP) ; Polychlorure de vinyle (PVC) ; Polystyrčne (PS). Thermodurcissables : durcissent de faēon irréversible, permanente en les chauffant. Triacétate de cellulose (films) ; résines phénoliques ; résine urée et mélamine-formaldéhyde ; résines époxydes ; Un premier classement des matičres plastiques peut źtre fait par un test de combustion ; on les classe alors en « auto-extinguibles » ou « non auto-extinguibles ». Auto-extinguibles : la combustion ne se propage pas si on enflamme le matériau plastique [ PVC ; Polytétrafluoroéthylčne (PTFE)] Non auto-extinguibles : ( combustibles ou inflammables) La combustion se propage si on enflamme le matériau plastique (PE ; PP ; PS ; Polyoxyméthylčnes ) Pour repérer ce caractčre, on définit l’ « Indice de Dioxygčne Limite » (IOL) par : IOL =[O2] / ([O2]+[N2]). Dans l’air, la valeur de l’IOL qui détermine la limite entre « auto-extinguible » et « non auto- extinguible » vaut : 21 % de dioxygčne en volume ;d'oł IOL =0,21. Une combustion nécessitant peu de dioxygčne ( IOL<0,21 ), se propagera : le plastique sera classé "non auto-extinguibles " Une combustion nécessitant beaucoup de dioxygčne ( IOL>0,21 ), ne se propagera pas, sans apport d'air extérieur : le plastique sera classé " auto-extinguibles "
Afin de déterminer l’appartenance ą une famille, on dispose d’autres tests :
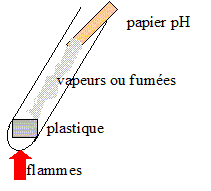
On dispose de quatre échantillons de matičres plastiques supposés appartenir ą des familles différentes : - l’échantillon A est supposé źtre un polystyrčne (PS) : il réagit, se ramollit en présence d'acétone. - l’échantillon B est supposé appartenir ą la famille des polyamides (PA) : le test au papier pH indique des fumées basiques, pH>7. - l’échantillon C est supposé źtre un polychlorure de vinyle (PVC) : c'est un produit chloré, le test de Belstein est positif. - l’échantillon D est supposé źtre une polyoléfine (matériaux résultant de la polymérisation de monomčres hydrocarbonés insaturés, de densité comprise entre 0,91 et 0,96). exemple : polyéthylčne --[CH2--CH2]n-- ; le monomčre et l'éthylčne CH2=CH2. Le test de densité est positif ( le matériau va flotter)
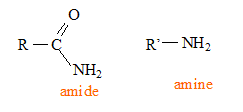
On s’intéresse maintenant aux polymčres de la famille des polyamides. La fonction amide se
caractérise par la présence du groupement
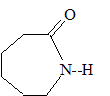
fonctionnel : Les différents polymčres de cette famille peuvent źtre obtenus soit par polyaddition, soit par polycondensation. polyaddition : addition de plusieurs centaines de molécules identiques les unes aux autres. polycondensation : réaction chimique entre deux molécules différentes ; on observe l'élimination d'eau ou de chlorure d'hydrogčne. Le PA 6, encore appelé nylon 6, s’obtient par polyaddition d’un monomčre, le caprolactame C6H11NO.
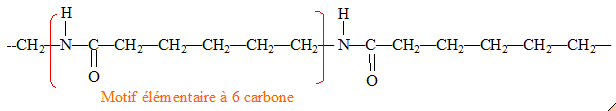
Représentation d'un fragment de structure de la macromolécule obtenue par polyaddition en identifiant le motif élémentaire de la chaīne :
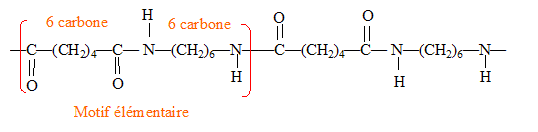
HOOC-(CH2)4-COOH et d’une diamine de formule H2N-(CH2)6-NH2. ( avec élimination de H2O) Représentation d'un fragment de structure du nylon 6-6 en identifiant le motif élémentaire de la chaīne :
Les polyamides ont des points de fusion élevés et de bonnes propriétés mécaniques : présence de liaison hydrogčne entre les chaīnes.
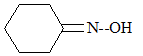
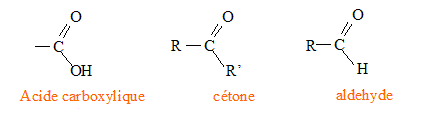
De nombreux autres composés contiennent dans leur molécule le groupement carbonyle, tels que les acides carboxyliques, les cétones ou les aldéhydes.
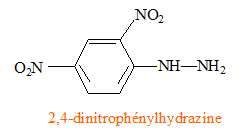
R et R' sont des chaīnes carbonnées. La DNPH, dont le nom est 2,4-dinitrophénylhydrazyne, permet de mettre en évidence la présence d’une cétone ou d’un aldéhyde. Il se forme un précipité jaune. Représentation de la formule
semi développée de la molécule de DNPH
: Comment différencier un aldéhyde d’une cétone ? Un aldehyde est un réducteur
( pas la cétone) : un aldehyde réagit avec le
nitrate d'argent ammoniacal, ( réactif de Tollens) et
avec la liqueur de Fehling.
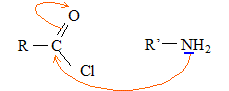
Le mécanisme de la réaction débute par l’attaque du centre nucléophile de l’une des molécules sur le centre électrophyle de l’autre. Le carbone fonctionnel du chlorure d'acyle est déficitaire en électrons ( du fait du caractčre électronégatif des atomes de chlore et d'oxygčne) : ce carbone constitue un site électrophile. L'atome d'azote de l'amine porte un doublet libre et constitue un site nucléophile.
|
|||||||||
|
|
|||||||||
|
|