|
Agrťgation 2006 : la molťcule de dioxygŤne ; diagramme binaire O2-N2. En poursuivant votre navigation sur ce site, vous acceptez l’utilisation de Cookies vous proposant des publicitťs adaptťs ŗ vos centres d’intťrÍts. |
|||||||
| .
. |
|||||||
|
|||||||
|
Configuration ťlectronique fondamentale de l'oygŤne : Z=8 soit 1s2, 2s2, 2p4. RŤgles d'ťlaboration des diagrammes molťculaires : Les orbitale atomiques de mÍme symťtrie et d'ťnergie proche sont combinťes. Il en rťsulte un nombre d'orbitale molťculaire (OM) ťgal au nombre d'orbitale atomique ( OA) de dťpart. * placer les OA des deux atomes de part et d'autre d'un espace destinť au tracť des OM. Si deux atomes ne sont pas identiques, les OA n'ont pas la mÍme ťnergie : l'atome le plus ťlectronťgatif est celui dont les OA sont situťes le plus bas. * connaÓtre les liaisons :
* trouver les positions des OM par rapport aux OA :
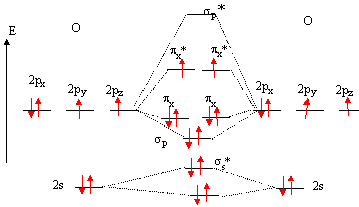
Diagramme d'orbitales molťculaires de la molťcule O2 :
RŤgles ŗ respecter pour placer les ťlectrons sur ce diagramme : Placer les ťlectrons dans les niveaux de plus basse ťnergie. Remplir le maximum d'orbitales dťgťnťrťes avec un ťlectron, puis constituer des doublets. propriťtťs
paramagnťtiques de O2 : deux
ťlectrons non appariťs sont prťsents
d'aprŤs ce diagramme.
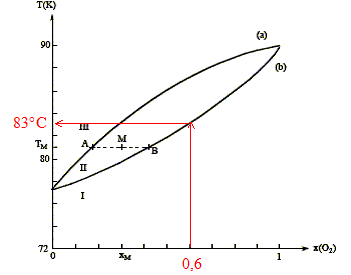
Distillation fractionnťe de l'air liquide : Le changement d'ťtat des mťlanges binaires O2 - N2 s'ťtudie gr‚ce au diagramme isobare ( P= 1 bar) d'ťquilibre liquide-vapeur suivant :
Mťlanges binaires idťaux : Microscopiquement la solution se comporte comme un liquide pur : les interactions entre molťcules diffťrentes et molťcules identiques sont ťgales. Il faut pour cela que les molťcules soient assez semblables ( exemple O2 et N2). On observe un diagramme en fuseau ou diagramme isotherme idťal pour des liquides totalement miscibles. Phases en prťsence dans les domaines I, II, III : ŗ pression constante, quand la tempťrature s'ťlŤve, on passe de l'ťtat liquide ŗ l'ťtat vapeur. donc : I : liquide ; II : liquide et vapeur en ťquilibre ; III : vapeur courbe a : courbe de rosťe, ensemble des points oý apparaÓt la premiŤre goutte de liquide lorsqu'on refroidit de la vapeur. courbe b : courbe de
d'ťbullition, ensemble des points oý
apparaÓt la premiŤre goutte de vapeur lorsqu'on
chauffe le liquide.
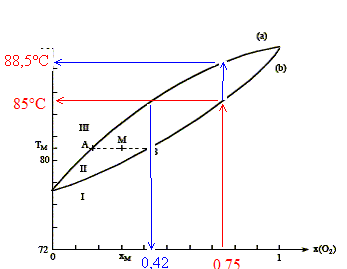
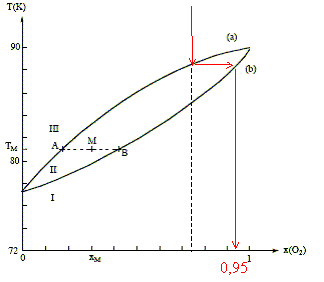
On considŤre n moles d'un mťlange de composition xM, portť ŗ la tempťrature TM. Le point M ŗ l'intťrieur du fuseau indique que nous sommes en prťsence du mťlange liquide + vapeur ; il nous renseigne aussi sur les proportions respectives du liquide et de la vapeur. notations : xL fraction molaire de O2 ŗ l'ťtat liquide ; xV fraction molaire de O2 ŗ l'ťtat vapeur ; xM fraction molaire en O2. nL : nombre de moles de mťlange ŗ l'ťtat liquide ; nV : nombre de moles de mťlange ŗ l'ťtat vapeur. nL + nV = n (1) La conservation du dioxygŤne s'ťcrit : nL(O2) + nV(O2)= n(O2). soit xLnL + xV nV = xM n (2) (1) et (2) donne : xLnL + xV (n-nL)= xM n nL(xL-xV) = n(xM-xV) ; nLAB = n AM. Rectification de l'air liquide :
|
|||||||
|
|
|||||||
|
|