|
Agrťgation 2005 : la mťtallurgie du titane ; diagramme d'Ellingham ; avancement, pression partielle En poursuivant votre navigation sur ce site, vous acceptez l’utilisation de Cookies vous proposant des publicitťs adaptťs ŗ vos centres d’intťrÍts. |
||||||||||||||||||||||||||||||||||||||||||||||||||||||
| .
. |
||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
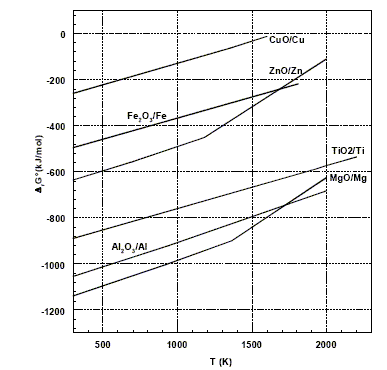
(1) TiO2(s) + 2Cl2(g) + 2C(s) = 2CO(g) + TiCl4(g) ŗ 900įC (2) TiCl4(g) + 2Mg(l) = Ti(s)+ 2MgCl2(l) ŗ 800įC On obtient ainsi le mťtal titane sous la forme d'ťponge qui est ensuite refondue pour obtenir des lingots. La figure ci-dessous donne le diagramme d'Ellingham, rapportť ŗ 1 mol de dioxygŤne, pour quelques composťs.
Principe de construction du diagramme d'Ellingham : On reprťsente l'enthalpie libre DrGį(T) de la rťaction suivante en fonction de la tempťrature. 2x/y M+ 1 O2 =2/y MxOy. L'entropie DrSį et l'enthalpie DrHį ťtant supposťes indťpendantes de la tempťrature, les courbes d'ťquation DrGį(T) = DrHį - T DrSį sont des segments de droites. Les ruptures de pente correspondent ŗ des changements d'ťtats physiques. Prťvision du sens d'ťvolution d'une rťaction chimique ŗ l'aide des couples Fe2O3/Fe et Al2O3/Al : 4/3 Al + O2 = 2/3Al2O3 (1) DrGį1. 4/3 Fe + O2 = 2/3Fe2O3 (2) DrGį2. 1, 5 fois (1) - 1,5 fois (2) donne : Fe2O3 + 2Al = 2Fe + Al2O3 DrGį avec DrGį = 1,5 ( DrGį1-DrGį2) Dans le domaine de tempťrature proposť, la droite relative ŗ Al2O3/Al est situťe au dessous de la droite relative ŗ Fe2O3/Fe : en
consťquence : DrGį1<DrGį2
et DrGį
<0, la rťaction ťvolue dans le sens direct,
rťduction de Fe2O3.
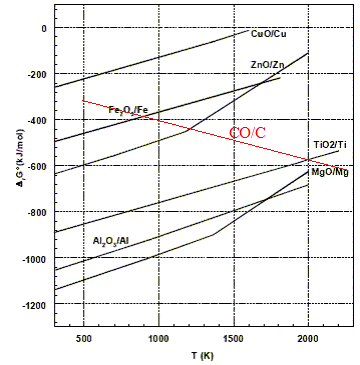
Courbe d'Ellingham pour ce couple dans le domaine de tempťrature 500-2000 K ajoutťe sur la figure ci-dessus : DrHį = 2DrHį(CO)-DrHį(O2(g))-2DrHį(C graphite ) = -221 kJ/mol DrSį = 2DrSį(CO)-DrSį(O2(g))-2DrSį(C graphite ) = 2*197,6 -2*5,7-205 = 178,8 J mol-1 K-1. DrG į=DrHį -TDrSį = -221 -0,1788 T en kJ/mol. DrG į(500) = -310 kJ/mol ; DrG į(2000) = -579 kJ/mol ;
La rťduction de
TiO2 par C est possible si la tempťrature
est supťrieure ŗ 2000 K (
tempťrature d'inversion de
cette rťaction).
(1) TiO2(s) + 2Cl2(g) + 2C(s) = 2CO(g) + TiCl4(g) ŗ 900įC En utilisant l'approximation d'Ellingham, montrons que cet ťquilibre est favorisť dans le sens direct quelque soit la tempťrature.
DrHį = -763 -2*110,5 +945 = -39 kJ/mol DrSį = DrSį(TiCl4) +2DrSį(CO)-2DrSį(Cl2(g)-2DrSį(C graphite )- DrSį(TiO2) DrSį = 354,8+2*197,6 -2*223-2*5,7 -50,3= 242 J mol-1 K-1. DrG į=DrHį -TDrSį = -39 -0,242 T en kJ/mol. DrG į<0 quelque soit T : l'ťquilibre (1) est favorisť dans le sens direct. On une tempťrature de 900įC, qui est une tempťrature intermťdiaire en mťtallurgie car : - La tempťrature est un facteur cinťtique favorable. - La rťaction ťtant exothermique, ŗ plus haute tempťrature, l'ťquilibre serait dťplacť dans le sens indirect. On peut sťparer le chlorure de titane du mťlange rťactionnel ŗ la suite de cette premiŤre ťtape en abaissant la tempťrature ŗ une valeur infťrieure ŗ 136 įC, tempťrature d'ťbullition de TiCl4. Les autres constituants du mťlanges ťtant soit solide, soit gazeux.
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
(3) TiCl4(g) + O2(g) = TiO2(s) + 2Cl2(g) ŗ 1400įC On ťtudie cet ťquilibre ŗ la tempťrature de 1400įC ŗ laquelle la constante d'ťquilibre vaut K' = 230. Le volume total de l'enceinte est de 100 L. On part d'un mťlange formť de 2 mol de chacun des rťactifs TiCl4 et O2. Quantitťs de matiŤre
de tous les constituants ainsi que les pressions partielles
des gaz ŗ l'ťquilibre : xťq
= 1,77 mol 0,23 0,23 1,77 3,54 A l'ťquilibre : nombre total de mol de gaz N= 4 fractions molaires des gaz : x(TiCl4) = x(O2) =(2-xťq)/N ; x(Cl2) =2xťq /N Les pression partielles sont proportionnelles aux fractions molaires ; P: pression totale. P(TiCl4) =P(O2)= (2-xťq)P/N ; P(Cl2) =2xťq P/N d'oý K'= [(2xťq) / (2-xťq)]2 = 230 ; (2xťq) / (2-xťq) = 230Ĺ =15,16 2xťq = 15,16(2-xťq) ; xťq = 1,77 mol. P= NRT/V = 4*8,314*(1400+273) / 0,1 =5,56 105 Pa = 5,56 bars. P(TiCl4) =P(O2)= (2-xťq)P/N = 0,23*5,56/4 = 0,32 bar P(Cl2) =2xťq
P/N =2*1,77*5,56/4 =4,91
bars
Composition du systŤme lorsqu'il n'ťvolue plus.
A l'ťquilibre : nombre total de mol de gaz N= 20 fractions molaires des gaz : x(TiCl4) = x(O2) =xťq/N ; x(Cl2) =(20-2xťq) /N Les pression partielles sont proportionnelles aux fractions molaires ; P: pression totale. P(TiCl4) =P(O2)= xťqP/N ; P(Cl2) =(20-2xťq) P/N d'oý K'= [(20-2xťq) / xťq]2 = 230 ; (20-2xťq) / xťq = 230Ĺ =15,16 15,16 xťq = 20-2xťq ; xťq = 1,16 mol. xťq ne peut pas Ítre supťrieur ŗ xmax =1 ; il n'y a pas d'ťquilibre, la rťaction est totale. Effet d'une variation de pression totale, ŗ composition constante et tempťrature constante, sur l'ťquilibre (3) : Dans l'expression de K', la
pression n'apparaÓt pas, seul l'avancement y figure :
une variation de pression ne modifie pas l'ťquilibre.
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
|