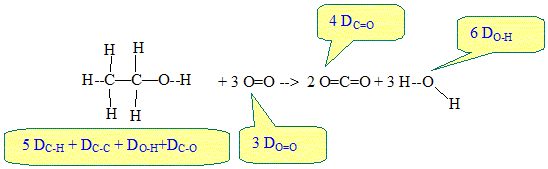|
Ethanol : biocarburant ; classes d'alcools ; oxydation ; combustion ; pouvoir calorifique concours gťnťral physique 2007 En poursuivant votre navigation sur ce site, vous acceptez l’utilisation de Cookies vous proposant des publicitťs adaptťs ŗ vos centres d’intťrÍts. |
|||||||||||||||||||||||||||||||||||||||
| .
. |
|||||||||||||||||||||||||||||||||||||||
|
|||||||||||||||||||||||||||||||||||||||
|
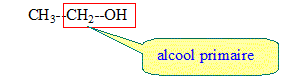
L'ťthanol est un alcool primaire issu de la culture de betteraves ou de blť aprŤs fermentation des sucres.
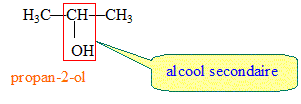
Exemple d'un alcool secondaire :
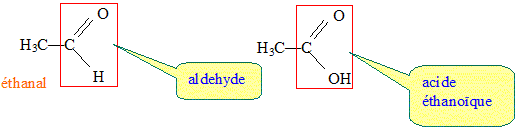
Par oxydation mťnagťe l'ťthanol conduit ŗ l'ťthanal, puis ŗ l'acide ťthanoÔque, prťsent dans le vinaigre.
Combustion de l'ťthanol dans le dioxygŤne de l'air La combustion complŤte donne de l'eau et du dioxyde de carbone. C2H6O + 3O2 = 2CO2 + 3H2O. La combustion incomplŤte ( oxygŤne en dťfaut) donne de l'eau, du monoxyde de carbone et des particules noires de carbone. C2H6O + 2O2 = 2CO + 3H2O. Le monoxyde de carbone, gaz incolore et inodore est toxique : il bloque les ťchanges de dioxygŤne au niveau des poumons avec le sang. ( il bloque les ťchanges de dioxygŤne avec l'hťmoglobine en se fixant dessus sans pouvoir Ítre libťrť) Ce qui n'est pas le cas pour CO2 (aussi inodore et incolore) mais qui peut Ítre libťrť lui.
Energie libťrťe par cette rťaction de combustion : Soit une molťcule contenant des liaisons A--B entre les atomes A et B. Par dťfinition l'ťnergie de liaison DA-B est l'ťnergie qu'il faut fournir pour dissocier une mole de liaisons A--B et ainsi sťparer les atomes A et B ŗ l'ťtat gazeux. C'est ťgalement l'ťnergie libťrťe lors de la formation d'une mole de liaison A-B ŗ partir des atomes A et B pris sťparťment ŗ l'ťtat gazeux.
q1 = 5DC-H + DC-C + DC-O + DO-H = 5*410+348+356+460 = 3,21 103 kJ/mol. Energie q libťrťe par la combustion complŤte d'une mole d'ťthanol ( pouvoir calorifique ) : q = [ 5DC-H + DC-C + DC-O + DO-H + 3DO=O] - [ 4DC=O +6DO-H q=[ 5*410+348+356+460 + 3*494 ] -[4*795 +6*460] q= 4696 -5940= -1,24 103 kJ/mol. q est nťgatif : de l'ťnergie est libťrťe vers l'extťrieur ; la combustion est exothermique.
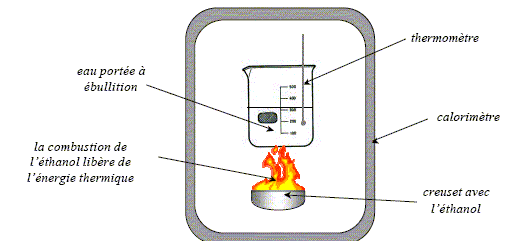
On considŤre l'expťrience suivante qui consiste ŗ brŻler une masse m= 5,0 g d'ťthanol. l'ťnergie libťrťe par la combustion permet de chauffer une masse Mi=50 g d'eau placťe dans un bťcher, de la tempťrature ambiante q0 = 20 įC ŗ la tempťrature d'ťbullition de l'eau q ťb = 100įC sous la pression atmosphťrique. L'eau bout et s'ťchappe en partie sous forme de vapeur. Une fois que tout l'ťthanol ŗ brŻlť, on mesure la masse Mf =42 g d'eau qui reste dans le bťcher. On rťalise l'expťrience dans un calorimŤtre, c'est ŗ dire que l'on nťglige dans un premier temps toute perte d'ťnergie vers l'extťrieur. Capacitť thermique massique de l'eau : ceau = 4,18 kJ kg-1 K-1 ; capacitť thermique du calorimŤtre : C= 1,20 kJ K-1 ; chaleur massique de vaporisation de l'eau : Lv= 2,25 103 kJ kg-1 ( ŗ 100 įC)
Energie thermique Q1 nťcessaire pour augmenter la tempťrature de l'eau et du calorimŤtre : Q1 = Mi ceau (q ťb -q 0 ) + C(q ťb -q 0 ) = ( Mi ceau+C)(q ťb -q 0 ) Q1 = (0,05 * 4,18 +1,2) (100-20) = 1,1 102 kJ ( 112,7 ) . Energie thermique Q2 nťcessaire pour vaporiser l'eau ŗ 100įC : Q1 =( Mi - Mf ) Lv= 8 10-3 * 2,25 103 =18 kJ ( 17,6 ) Pouvoir calorifique de
l'ťthanol : q =
112,7 + 17,6 = 1,3
102 kJ (130,3 ).
Le tableau suivant rassemble le
pouvoir calorifique massique moyen de quelques combustibles
courants : La combustion de 5,0 g libŤre 1,3 102 kJ qm = 1,3 102 / 5,0 10-3 = 26 103 kJ kg-1. Du mÍme ordre de grandeur que celui du charbon, 1,5 fois plus faible que celui de l'essence. Le CO2 rejetť par la combustion de l'ťthanol, contribue trŤs peu ŗ l'effet de serre : en effet, lors de sa croissance, la plante a absorbť une certaine quantitť de dioxyde de carbone. |
|||||||||||||||||||||||||||||||||||||||
|
|
|||||||||||||||||||||||||||||||||||||||
|
|