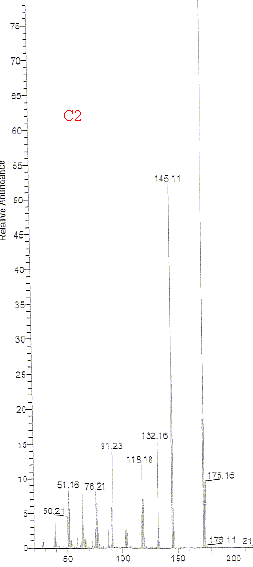|
analyse d'un explosif concours police scientifique 2005 En poursuivant votre navigation sur ce site, vous acceptez l’utilisation de Cookies vous proposant des publicitťs adaptťs ŗ vos centres d’intťrÍts. |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| .
. |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
Trois prises d'essai d'environ 2 g de cette p‚te sont analysťes. Verrerie : - verre de montre utilisť pour le pesťes - becher en verre de 100 mL utilisť pour la solubilisation dans le cyclohexane. - entonnoir en verre, filtre en papier - cristallisoir de 150 mL pour recueillir les filtrats. Mode opťratoire : Mise en solution de chaque prise d'essai dans 20 mL de cyclohexane. Filtration sur papier filtre aprŤs avoir otť le plus gros de la partie insoluble. Remise en solution de la fraction insoluble dans 20 mL de cyclohexane puis filtration sur le filtre ayant servi lors de la prťcťdente filtration. Effectuer plusieurs remises en solution et filtrations successives jusqu'ŗ obtenir 100 mL de cyclohexane. Rassembler les fractions insolubles, sťchage de cette fraction et du filtre et pesťes ŗ poids constant. Evaporation totale des 100 mL de cyclohexane ŗ l'air libre et pesťes ŗ poids constant. Les pesťes des prises d'essai (PE1, PE2, PE3) ainsi que les rťsultats des pesťes des fractions insolubles et solubles sont donnťes : Fractions insolubles :
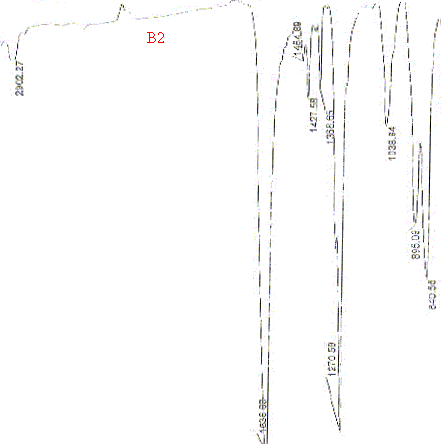
On donne les spectres d'analyse de la fraction insoluble (B1) ainsi que de composťs tťmoins ( B2 ŗ B5). Quelles conclusions tirez-vous de l'analyse de la fraction insoluble ? Identifier la mťthode utilisťe pour l'analyse de cette fraction. Quel type d'identification permet -elle ? Masse de la fraction soluble = masse ťchantillon + masse becher et filtre avant traitement - masse becher et filtre aprŤs traitement. Masse de la fraction insoluble = masse ťchantillon - masse de la fraction soluble. La fraction insoluble reprťsente 88,6% de PE1, 88,8 % de PE2 et 88,2 % de PE3 soit en moyenne 88, 5% de la p‚te. La fraction insoluble est analysťe par spectromťtrie infrarouge. Une molťcule illuminťe par des radiations dans l'infrarouge peut absorber certaines d'entre elles ŗ des longueurs d'onde qui correspondent aux frťquences de vibration des groupements chimiques la constituant. L’infrarouge moyen (entre 1000 et 6000 cm-1) dispense suffisamment d’ťnergie pour stimuler les vibrations molťculaires ŗ des niveaux d’ťnergie supťrieurs. La mesure de l'intensitť de lumiŤre absorbťe ŗ chaque longueur d'onde l conduit ŗ un spectre caractťristique du produit ťtudiť. Les analyses sont le plus souvent effectuťes en transmission. Le spectre obtenu reprťsente I/I0 = f(t) avec I = intensitť absorbťe, I0= intensitť initiale, t nombre d'onde = 1/l exprimť en cm-1. Le bromure de potassium (KBr) est
transparent aux rayonnements IR dans la zone 4000
cm-1 ŗ 700 cm-1
Les spectres correspondants possŤdent des pics identiques aux nombres d'onde suivants :. 3024 ; 2911 ; 1473 ; 1395 ; 1285 ; 1037 ; 1001 ; 849 ; 762 ; 701.
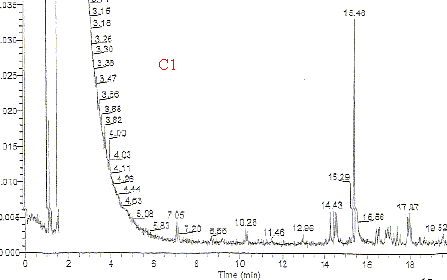
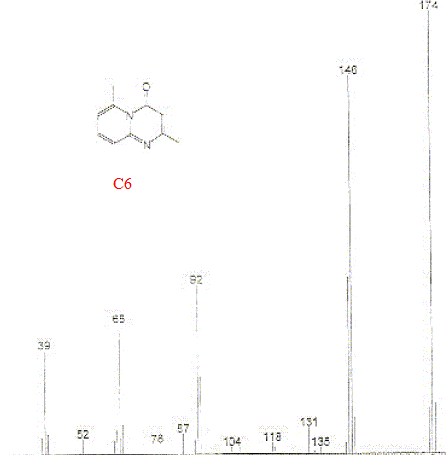
La fraction soluble a ťtť analysťe par chromatographie en phase gazeuse couplťe ŗ un spectromŤtre de masse. Le chromatogramme obtenu est notť C1. Le pic dont le temps de rťtention est 15,46 min est reprťsentť sur le document C2. Des spectres de composťs tťmoins sont donnťs C3 ŗ C7.
Le chromatogramme C1 met en ťvidence une dizaine de constituants : l'un, correspondant ŗ tR= 15,46 min est le constituant principal. Quel est le principe de cette mťthode CPG-SM ? principe gťnťral de la chromatographie : La chromatographie est une mťthode de sťparation et d'identification des constituants d'un mťlange. La chromatographie est basťe sur la diffťrence de solubilitť d'une substance dans deux phases non miscibles:la phase stationnaire liťe au support et la phase mobile ou solvant. Plus une substance est soluble dans la phase mobile, plus elle est entraÓnťe par cette phase; inversement, une substance peu soluble dans la phase mobile migre peu. Un fluide appelť phase mobile parcourt un tube appelť colonne. Cette colonne peut contenir des "granulťs" poreux (colonne remplie) ou Ítre recouverte ŗ l'intťrieur d'un film mince (colonne capillaire). Dans les deux cas, la colonne est appelťe phase stationnaire. A l'instant initial, le mťlange ŗ sťparer est injectť ŗ l'entrťe de la colonne oý il se dilue dans la phase mobile qui l'entraÓne ŗ travers la colonne. Si la phase stationnaire a ťtť bien choisie, les constituants du mťlange, appelťs gťnťralement les solutťs, sont inťgalement retenus lors de la traversťe de la colonne. De ce phťnomŤne appelť rťtention il rťsulte que les constituants du mťlange injectť se dťplacent tous moins vite que la phase mobile et que leurs vitesses de dťplacement sont diffťrentes. Ils sont ainsi ťluťs de la colonne les uns aprŤs les autres et donc sťparťs. Un dťtecteur placť ŗ la sortie de la colonne couplť ŗ un enregistreur permet d'obtenir un tracť appelť chromatogramme. En effet, il dirige sur un enregistreur un signal constant appelť ligne de base en prťsence du fluide porteur seul ; au passage de chaque solutť sťparť il conduit dans le temps ŗ l'enregistrement d'un pic. Dans des conditions chromatographiques donnťes, le "temps de rťtention" (temps au bout duquel un composť est ťluť de la colonne et dťtectť), caractťrise qualitativement une substance. L'amplitude de ces pics, ou encore l'aire limitťe par ces pics et la prolongation de la ligne de base permet de mesurer la concentration de chaque solutť dans le mťlange injectť. C'est en jouant sur la nature de l'ťluant (et dans une moindre mesure sur la nature du support) que l'on parvient ŗ sťparer les constituants d'un mťlange.
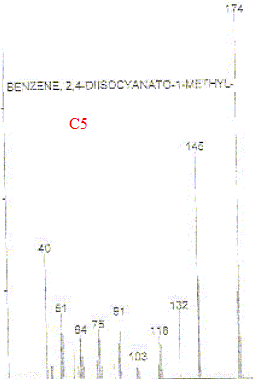
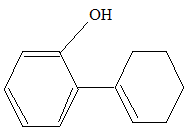
Son principe : sťparation en phase gazeuse de molťcules chargťes d'aprŤs leur rapport masse/charge (m/z). L'impact ťlectronique fourni de nombreux fragments et le spectre compte un trŤs grand nombre de raies. On identifie un composť en comparant son spectre de masse ŗ des banques de spectres de masse de composťs connus. On peut identifier C2 ŗ C5 : les spectres correspondants prťsentants de grandes analogies. Formule semi-dťveloppťe correspondant ŗ C3 :
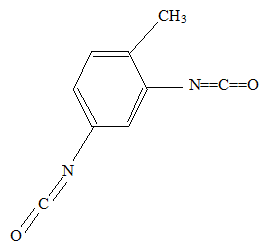
Formule semi-dťveloppťe correspondant ŗ C5 :
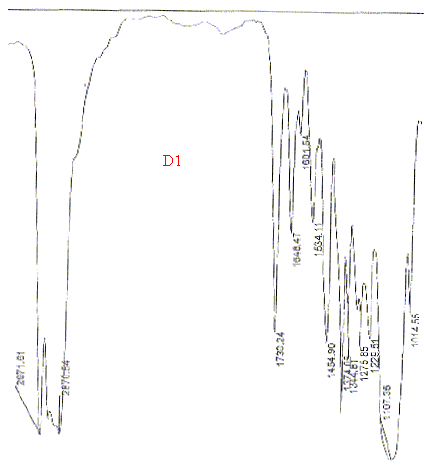
A quelle fonction correspond la bande situťe ŗ 1730 cm-1 ?
Le groupe C=O donne une bande intense, de largeur moyenne, situťe dans la rťgion entre 1820 et 1660 cm-1. La prťsence des bandes vers 2870 indique la prťsence du groupe OH. |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||