|
Aide technique laboratoire ( d'aprŤs concours 2006) synthŤse de l'essence d'estragon ; spectrophotomťtrie. En poursuivant votre navigation sur ce site, vous acceptez l’utilisation de Cookies vous proposant des publicitťs adaptťs ŗ vos centres d’intťrÍts. |
||||||||||||||||
| .
. |
||||||||||||||||
|
||||||||||||||||
|
L'estragole est une substance utilisťe en parfumerie, elle entre ťgalement dans la composition d'arŰmes pour aliments et boissons. L'estragole est prťsente dans les essences d'estragon ( 70 ŗ 75 %) obtenues par hydrodistillation des feuilles d'estragon. Mode
opťratoire
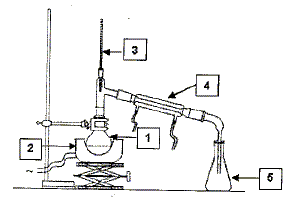
: Dans un ballon de 500 mL, on introduit 200 mL d'eau distillťe ainsi que des feuilles fines d'estragon et quelques grains de pierre ponce. On rťalise le montage d'hydrodidtillation ci-dessus et on porte ŗ ťbullition le mťlange contenu dans le ballon. On arrÍte l'hydrodistillation aprŤs obtention de 40 mL de distillat.
corrigť 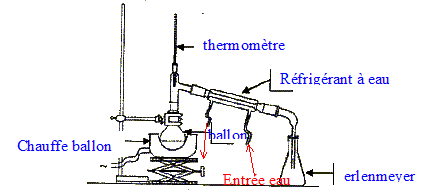
Principe d'une
hydrodistillation : les vapeurs d'estragole sont
entrainťes par la vapeur d'eau ; celles-ci se
condensent dans le rťfrigťrant ŗ
eau. Extraction : L'estragole est pratiquement
insoluble dans l'eau salťe.
RŰle du sulfate de magnťsium anhydre : ťlimine toute trace d'eau de la phase organique Chromatographie sur couche mince CCM : Principe d'une chromatographie sur couche mince : Sťparer et identifier les constituants d'un
mťlange en utilisant leur diffťrence de
solubilitť entre une phase fixe ( support de silice )
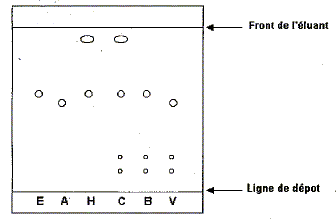
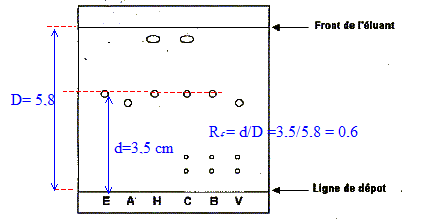
et mobile ( l'ťluant) E et A sont des corps purs de rťfťrence. H, C, B et V sont des mťlanges. H, C et B contiennent de l'estragole E ; V contient de l'anťthole A Rapport frontal Rf de l'estragole :
|
||||||||||||||||
|
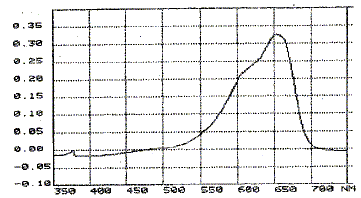
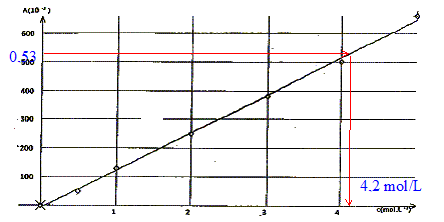
On souhaite dťterminer la concentration molaire inconnue du bleu d'indigo en utilisant un spectrophotomŤtre. On dispose d'une solution S0 d'indigo de concentration massique c0 = 12 mg/L.
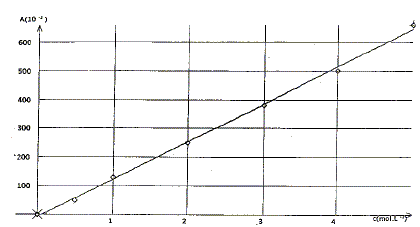
facteur de dilution : F= 12/2,4 = 5 prťlever 50 / 5 = 10,0 mL de S0 ŗ l'aide d'une pipette jaugťe + pipeteur. Placer dans une fiole jaugťe de 50 mL et complťter avec de l'eau distilťe jusqu'au trait de jauge. Agiter pour rendre homogŤne. La valeur de la longueur d'onde doit correspondre au maximum d'absorption del'indigo soit l =650 nm. Il faut faire un rťglage du "zťro d'absorbance " en plaÁant dans la cuve le solvant pur.
|
||||||||||||||||
|
|
||||||||||||||||
|
|