|
Agrťgation physique chimie ( concours 2006 ) : pile de concentration stoechiomťtrie et la constante globale de formation bn du complexe Ag(NH3)2+ en solution aqueuse En
poursuivant votre navigation sur ce site, vous acceptez l’utilisation
de Cookies vous proposant des publicitťs adaptťes ŗ vos centres
d’intťrÍts. |
|||||||||||||||||||||||||||||||||
| .
. |
|||||||||||||||||||||||||||||||||
|
|||||||||||||||||||||||||||||||||
|
|
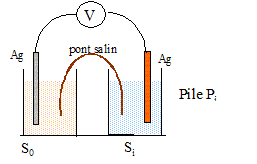
But : dťterminer la stoechiomťtrie et la constante globale de formation bn du complexe Ag(NH3)n+ en solution aqueuse. On considŤre les solutions Si ( i=0, 1, 2, 3) prťparťes de la maniŤre suivante : dans une fiole jaugťe de 100 mL, on place un volume v0 = 20 mL d'une solution de nitrate d'argent ŗ c0=1,0 10-2 mol/L et un volume vi (mL) d'une solution d'ammoniac ŗ 1 mol/L puis on complŤte au trait de jauge avec de l'eau distillťe.
|
||||||||||||||||||||||||||||||||
|
|||||||||||||||||||||||||||||||||
|
corrigť Equation bilan de la rťaction globale de formation du complexe Ag(NH3)n+ dans la solution Si : Ag+ + n NH3 = Ag(NH3)n+ ; bn = [Ag(NH3)n+] / ([Ag+ ][NH3]n) Expression des concentrations ŗ l'ťquilibre [Ag(NH3)n+]i et [NH3]i :
[NH3]i =( vi - nxťq) / 100 ; [Ag(NH3)n+]i = xťq / 100 ; or vi >> 0,2 ; (solution d'ammoniac concentrťe) en consťquence : l'excŤs d'un rťactif dťplace l'ťquilibre vers la droite ( sens direct) et la rťaction peut Ítre considťrťe comme totale; de plus il se forme le complexe avec n le plus ťlevť. xťq = 0,2 mmol ; [Ag(NH3)n+]i
=0,2 / 100 = 2 10-3
mol/L ; [NH3]i
=( vi - 0,2 n) / 100 proche de 0,01vi
mol/L avec vi en mL.
E = Eį(Ag+/Ag) + 0,06 log [Ag+]. pour la solution S0 : E0 = Eį(Ag+/Ag) + 0,06 log [Ag+]0. pour la solution Si : Ei = Eį(Ag+/Ag) + 0,06 log [Ag+]i. DEi= Ei-E0 = 0,06 log ( [Ag+]i / [Ag+]0) DEi est nťgatif car dans la solution Si, l'ion argent est sous forme complexe. [Ag+]i < [Ag+]0. avec [Ag+]0 = c0/5 = 2,0 10-3 mol/L ; bn = [Ag(NH3)n+]i / ([Ag+ ]i[NH3]in) soit [Ag+]i = [Ag(NH3)n+]i / (bn[NH3]in) voisin de 2 10-3/(bn(0,01 vi)n) DEi= -0,06 log (bn(0,01 vi)n) = -0,06 log bn - 0,06n log (0,01 vi) DEi permet de dťterminer les valeur de n et bn : on trace la droite d'ťquation DEi= f(log (0,01 vi)
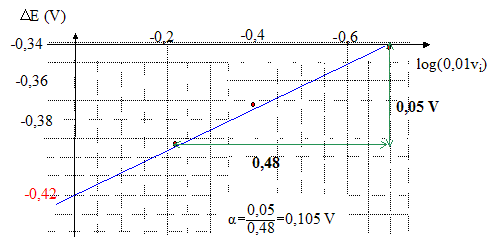
le coefficient directeur donne : 0,06n =0,105 et l'ordonnťe ŗ l'origine donne -0,06 log bn = -0,42 V d'oý n = 0,105/0,06 = 1,73 ( n ťtant entier, on prend n=
2) et log bn
= 0,42/0,06 = 7 ; bn
=107.
Montrons que dans les conditions de l'expťrience on peut nťgliger la formation de ce complexe b1 = [Ag(NH3)+]i / ([Ag+ ]i[NH3]i) ; [Ag(NH3)+]i = b1[Ag+ ]i[NH3]i avec [Ag+ ]i = 2 10-3/(b2(0,01 vi)2) = 2 10-6 / vi2 ; [NH3]i = 0,01 vi ; [Ag(NH3)+]i = 103,4* 2 10-8 / vi = 2 10-4,6 / vi =5 10-5 / vi. on trouve des valeurs voisines de 10-6 mol/L , alors que [Ag(NH3)2+]i = 2 10-3 mol/L.
|
|||||||||||||||||||||||||||||||||
|
|
|||||||||||||||||||||||||||||||||